Clear Sky Science · es
La represión de miR-29 vía MYC conduce a un aumento de la señalización CD40 en el linfoma folicular transformado
Cuando la comunicación célula a célula se vuelve peligrosa
El linfoma folicular es un cáncer sanguíneo de crecimiento lento que puede mantenerse latente durante años; sin embargo, en algunos pacientes cambia de manera abrupta y se convierte en una enfermedad agresiva y potencialmente mortal. Este estudio plantea una pregunta sencilla pero crucial: ¿qué cambios se producen dentro de estas células cancerosas y en su vecindario celular para provocar ese cambio de marcha? Al seguir tanto los genes de las células tumorales como los pequeños reguladores de ARN durante esta transición, los investigadores descubren un circuito de control oculto que modula la intensidad con la que las células tumorales responden a la ayuda de las células inmunitarias cercanas —y muestran que cuando este circuito falla, el cáncer se vuelve más difícil de tratar.
Un cáncer silencioso que a veces acelera
El linfoma folicular se origina en los linfocitos B, las células inmunitarias que normalmente producen anticuerpos. La mayoría de los pacientes convive con una forma indolente, o de crecimiento lento, de la enfermedad, pero cada año una fracción de los casos se transforma en un linfoma agresivo que se comporta de manera similar al linfoma difuso de células B grandes. Se habían relacionado mutaciones genéticas con este cambio, pero no explicaban toda la historia. Las células tumorales viven en un microambiente rico en células T colaboradores y otros aliados inmunitarios, intercambiando señales de forma continua. Los autores sospecharon que pequeñas moléculas regulatorias llamadas microARN, que ajustan finamente el uso de los genes, podrían ser clave para que las células cancerosas se adapten a este vecindario cambiante y den el salto a un estado más peligroso.
Frenos de ARN pequeños que desaparecen
Para poner a prueba esta idea, el equipo realizó el primer perfil emparejado de ARN mensajero y microARN en muestras pareadas tomadas de los mismos pacientes antes y después de la transformación. Al comparar 11 muestras de linfoma folicular con sus 11 contrapartes transformadas, encontraron más de mil genes y 19 microARN que cambiaron. Una familia destacó: los tres miembros de la familia miR-29 estaban sistemáticamente reducidos en los tumores transformados. En trabajos anteriores en otras neoplasias hematológicas, miR-29 había actuado como un freno del crecimiento y la supervivencia celular. Aquí, su pérdida emergió como una firma de la transformación, sugiriendo que la disminución de esta familia de microARN podría liberar vías promotoras del crecimiento en las células del linfoma.
Una señal aumentada desde las células colaboradoras
Al profundizar en los datos de expresión génica, los investigadores descubrieron que los tumores transformados mostraban un fuerte aumento en la actividad de la vía CD40, una ruta de señalización que se activa cuando una célula T colaboradora se comunica con una célula B. En ganglios linfáticos sanos y en el linfoma folicular indolente, esta interacción ayuda a que las células B crezcan y sobrevivan de forma controlada. Sorprendentemente, en las muestras transformadas, los genes relacionados con CD40 estaban activados en cerca del 90 por ciento de los casos, aunque el número total de células T en las áreas tumorales era en realidad menor. Los análisis unicelulares confirmaron que un subconjunto de células T seguía proporcionando la señal activadora de CD40, pero las propias células del linfoma parecían haberse vuelto mucho más sensibles a esa señal.
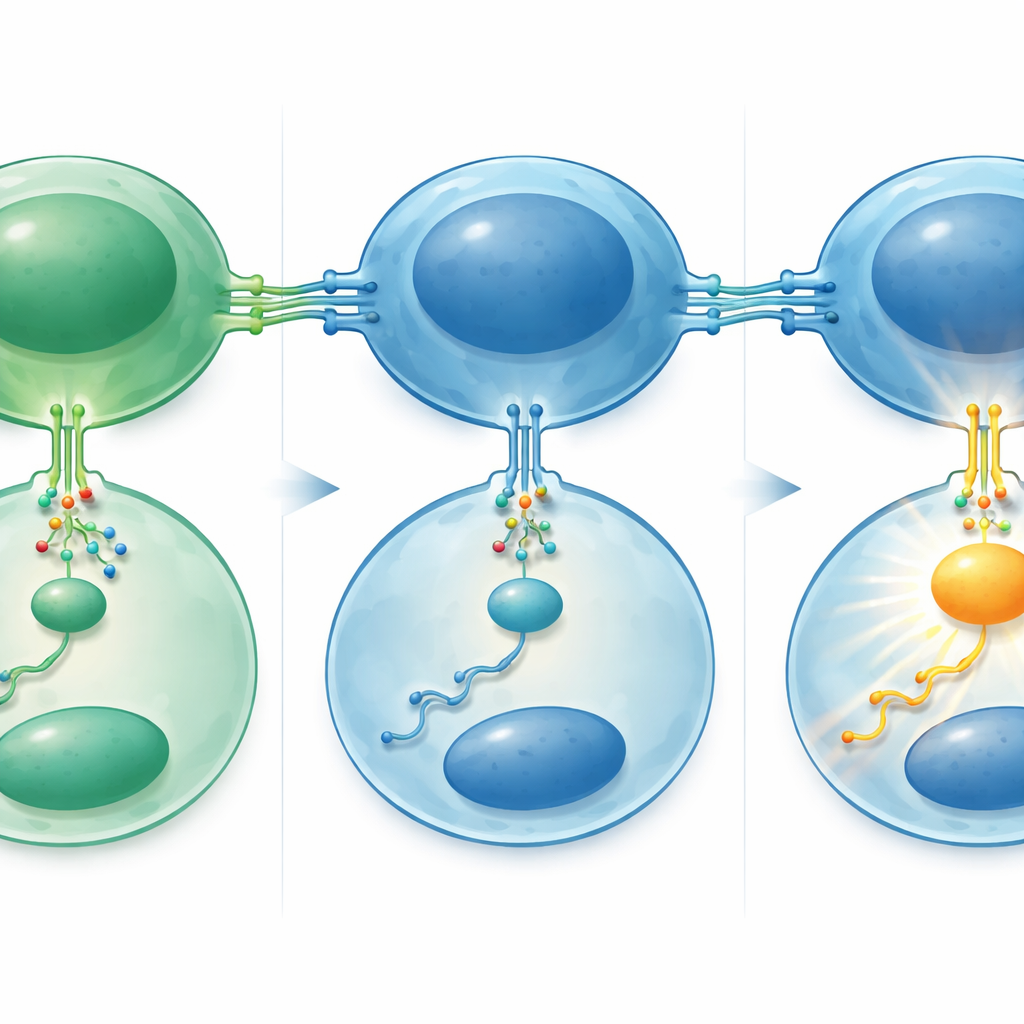
Cómo un circuito de tres pasos amplifica el crecimiento
Los autores luego reunieron el circuito molecular detrás de esta mayor sensibilidad. Experimentos de laboratorio mostraron que miR-29 normalmente mantiene controlados los niveles de una proteína llamada TRAF4 dentro de las células B; TRAF4 es un adaptador interno que ayuda a transmitir la señal de CD40 hacia el interior de la célula. Cuando los niveles de miR-29 se aumentaron experimentalmente en líneas celulares de linfoma, los niveles de TRAF4 disminuyeron y las células respondieron con menor intensidad a la estimulación por CD40, con una activación más débil de la señalización aguas abajo y una proliferación más lenta. En las muestras de pacientes apareció el patrón opuesto: los tumores transformados y los linfomas foliculares de mayor grado presentaban más TRAF4 y mayores tasas de división celular. Otro actor importante, la conocida proteína promotora del cáncer MYC, se situó aguas arriba. Los niveles y la actividad de MYC aumentaron durante la transformación, y se mostró que MYC se une directamente a las regiones de ADN que controlan miR-29, actuando como un interruptor que apaga esta familia de microARN.
Qué significa esto para los pacientes
Al unir estas piezas, el estudio delimita una cadena de tres pasos: la activación de MYC suprime miR-29, la pérdida de miR-29 levanta el freno sobre TRAF4, y el exceso de TRAF4 hace que las células del linfoma sean hiperresponsivas a las señales CD40 procedentes de las pocas células T colaboradoras restantes. Esta “ayuda” amplificada impulsa un mayor crecimiento y supervivencia, contribuyendo a la transformación. A nivel clínico, los pacientes cuyos tumores mostraban niveles más bajos de miR-29 —especialmente el miembro miR-29c— tendieron a tener una supervivencia más corta y recaídas más rápidas, hallazgos confirmados en un ensayo de tratamiento independiente. Dado que miR-29 puede medirse de forma fiable incluso en muestras de biopsia antiguas y conservadas, y porque ya se exploran fármacos que mimetizan miR-29 o bloquean la señalización CD40, este trabajo señala nuevas vías para identificar pacientes de linfoma folicular de alto riesgo y para diseñar tratamientos que interrumpan la peligrosa conversación entre las células tumorales y sus vecinas inmunitarias.
Cita: Filip, D., Litzmanova, K., Michaelou, A. et al. Repression of miR-29 via MYC leads to increased CD40 signaling in transformed follicular lymphoma. Leukemia 40, 759–772 (2026). https://doi.org/10.1038/s41375-026-02868-8
Palabras clave: linfoma folicular, microARN, señalización CD40, MYC, microambiente tumoral