Clear Sky Science · es
JAK2V617F reprograma al Factor Inducible por Hipoxia‑1 para inducir un regulón hipóxico no canónico en neoplasias mieloproliferativas
Por qué importa esto para el cáncer de sangre
Algunos cánceres de la sangre de crecimiento lento, conocidos como neoplasias mieloproliferativas, pueden arder de forma silenciosa durante años antes de transformarse de forma repentina en una leucemia agresiva. Este estudio plantea una pregunta simple pero crucial: ¿cómo secuestra una mutación cancerígena común el sistema intrínseco de la célula para detectar oxígeno, y puede ese secuestro atacarse específicamente sin dañar las células sanas? Las respuestas podrían abrir una vía nueva para tratar a pacientes de alto riesgo mientras se preservan los tejidos normales que también dependen de las señales de detección de oxígeno.
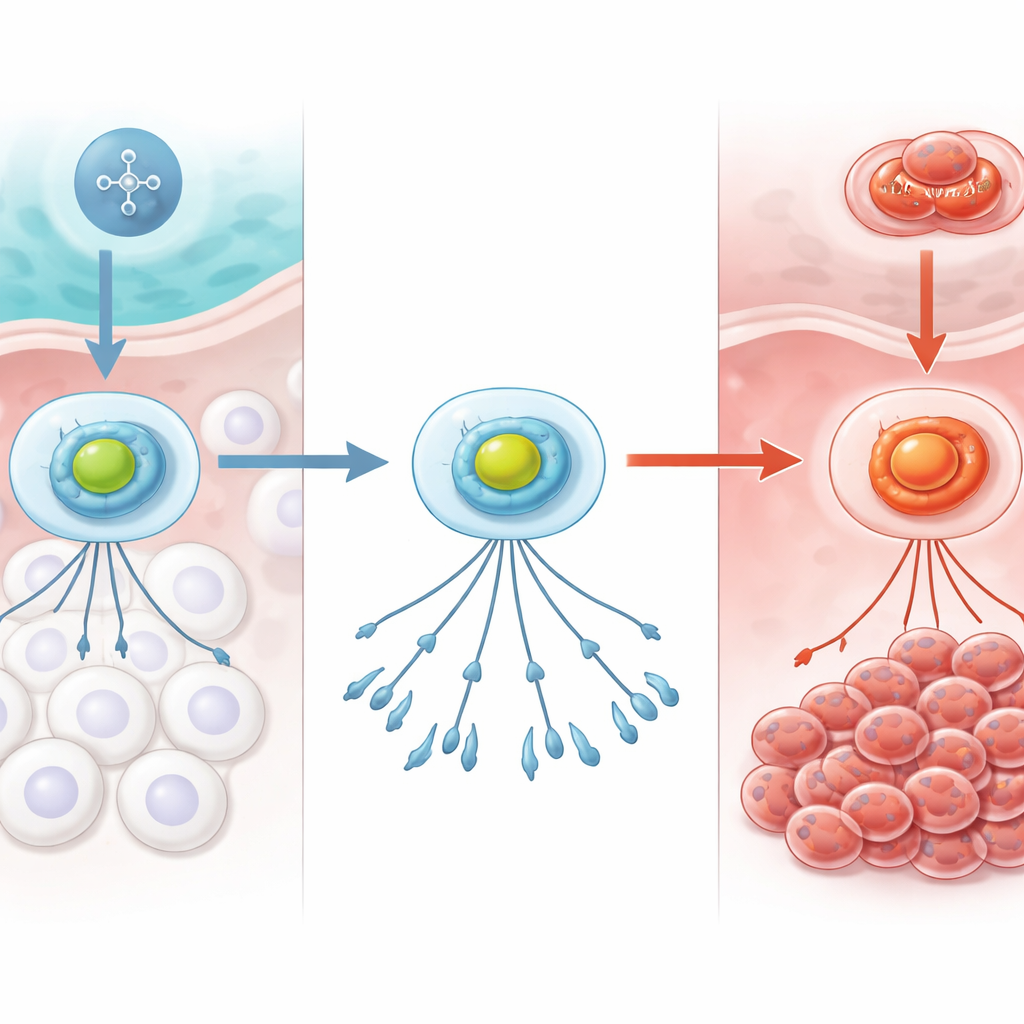
El sistema de alarma de oxígeno del organismo
Las células vigilan constantemente cuánta oxigenación hay disponible. En el centro de este sistema hay un complejo proteico llamado HIF‑1, que funciona como una alarma de oxígeno. En condiciones normales y bien oxigenadas, una subunidad de HIF‑1 se degrada rápidamente, manteniendo la alarma apagada. Cuando el oxígeno disminuye, esa degradación se detiene, HIF‑1 se estabiliza, se traslada al ADN de la célula y activa genes que ayudan a adaptarse, por ejemplo cambiando el uso de la energía o promoviendo el crecimiento de nuevos vasos sanguíneos. En el cáncer, este mismo sistema puede volverse en beneficio del tumor, ayudando a las células malignas a soportar entornos estresantes como la médula ósea de bajo oxígeno.
Cuando una mutación recablea la alarma
Los investigadores se centraron en una mutación llamada JAK2V617F, muy común en las neoplasias mieloproliferativas. Trabajos previos mostraron que esta mutación mantiene la alarma HIF‑1 encendida incluso cuando el oxígeno es abundante. Usando líneas celulares modificadas, el equipo comparó el HIF‑1 unido al ADN en dos condiciones: hipoxia real y oxigenación normal en presencia de la mutación JAK2V617F. Encontraron que en las células mutadas HIF‑1 se une a menos regiones del genoma, responde menos a los cambios en oxígeno e interactúa con un conjunto distinto de proteínas asociadas, muchas implicadas en el procesamiento del ARN. En otras palabras, la mutación no limita su efecto a dejar HIF‑1 permanentemente “encendido”: recalibra la alarma hacia un conjunto distinto de objetivos.
Un programa génico específico del cáncer
A partir de estos experimentos, los autores definieron varios conjuntos de genes dependientes de HIF‑1, incluido uno que denominaron la firma hipóxica JAK2V617F. Luego evaluaron cuánto se activaban estas firmas en células sanguíneas de 172 pacientes con neoplasias mieloproliferativas positivas para JAK2V617F. Sorprendentemente, los programas génicos habituales asociados a baja oxigenación de HIF‑1 no predijeron la gravedad de la enfermedad ni la supervivencia. En contraste, la firma hipóxica específica de la mutación separó claramente a los pacientes con enfermedad más grave y se asoció con peor supervivencia global. Muchos de los genes de este conjunto estaban especialmente activos en progenitores megacariocíticos, las células de la médula ósea que proliferan excesivamente y causan la fibrosis en estos trastornos, y algunos participaban en la reparación del daño del ADN, un proceso que puede ayudar a las células cancerosas a sobrevivir a tensiones nocivas.
Pistas sobre el empeoramiento súbito de la enfermedad
Un temor importante para los pacientes es la transformación repentina de la enfermedad crónica a una leucemia agresiva en “fase blástica”. Al analizar muestras emparejadas de pacientes antes y después de este cambio, el equipo destiló un subconjunto más pequeño de 13 genes, bautizado como la firma HIF1‑MPN‑BP, que aumentaba o disminuía con la transformación. Este subconjunto se asoció fuertemente con puntuaciones de riesgo más altas, peor supervivencia y mayor fibrosis medular. Importante, este patrón pareció ser específico de la enfermedad impulsada por JAK2V617F, más que una característica genérica de todas las leucemias. Muchos genes de este subconjunto son objetivos farmacológicos plausibles, lo que sugiere una lista enfocada de candidatos para futuras terapias destinadas a bloquear la progresión.
Encontrar al cómplice oculto de la mutación
¿Cómo mantiene JAK2V617F a HIF‑1 activo independientemente del oxígeno? Mediante enfoques de bioquímica proteica, los autores descubrieron que en las células mutadas HIF‑1 presenta dos marcas químicas (fosforilaciones) previamente desconocidas en una región que normalmente controla su degradación. Rastrearon estos cambios hasta PIM1, una quinasa activada en la vía downstream de la mutación JAK2. Bloquear PIM1 con fármacos experimentales hizo que los niveles de HIF‑1 disminuyeran en las células mutadas, pero dejó en gran medida intacta la respuesta normal a la hipoxia. La inhibición de PIM1 también redujo selectivamente la expresión de los genes de la firma HIF1‑MPN‑BP de riesgo y empujó a las células mutadas hacia la muerte celular, mientras preservaba a sus contrapartes no mutadas.
Qué significa esto para los pacientes
Este trabajo demuestra que la misma proteína sensor de oxígeno, HIF‑1, se comporta de forma muy distinta según cómo sea activada. En las neoplasias mieloproliferativas impulsadas por JAK2V617F, un eje de señalización JAK2–PIM1 estabiliza HIF‑1 de un modo que lo desprende del control normal por oxígeno y estrecha su actividad hacia un programa génico que promueve la enfermedad. Dado que este programa alterado está estrechamente vinculado a la gravedad de la enfermedad y al riesgo de transformación, y puede atenuarse bloqueando PIM1, ofrece una vía prometedora para dirigirse a la actividad maligna de HIF‑1 preservando su papel esencial en los tejidos sanos. Terapias que exploten esta diferencia podrían algún día ayudar a impedir que los cánceres sanguíneos de evolución lenta deriven en leucemias potencialmente mortales.
Cita: Kealy, D., Ellerington, R., Bansal, S. et al. JAK2V617F reprograms Hypoxia Inducible Factor-1 to induce a non-canonical hypoxia regulon in myeloproliferative neoplasms. Leukemia 40, 609–621 (2026). https://doi.org/10.1038/s41375-025-02843-9
Palabras clave: neoplasias mieloproliferativas, JAK2V617F, HIF-1, quinasa PIM1, transformación a fase blastica