Clear Sky Science · es
Alnuctamab, un engajador de células T bivalente que se dirige al antígeno de maduración de células B para pacientes con mieloma múltiple en recaída o refractario: resultados de un estudio de fase 1, primero en humanos
Por qué importa este nuevo fármaco contra el cáncer
Para las personas que viven con mieloma múltiple, un cáncer de la sangre que casi siempre reaparece tras el tratamiento, cada nueva opción puede significar más tiempo y mejor calidad de vida. Este estudio prueba una inmunoterapia de nueva generación llamada alnuctamab, diseñada para ayudar a las propias células defensivas del cuerpo a localizar y eliminar las células de mieloma. La investigación plantea una pregunta práctica que importa tanto a pacientes como a médicos: ¿se puede administrar esta potente terapia como una inyección subcutánea simple, con efectos antitumorales sólidos pero menos efectos secundarios peligrosos?
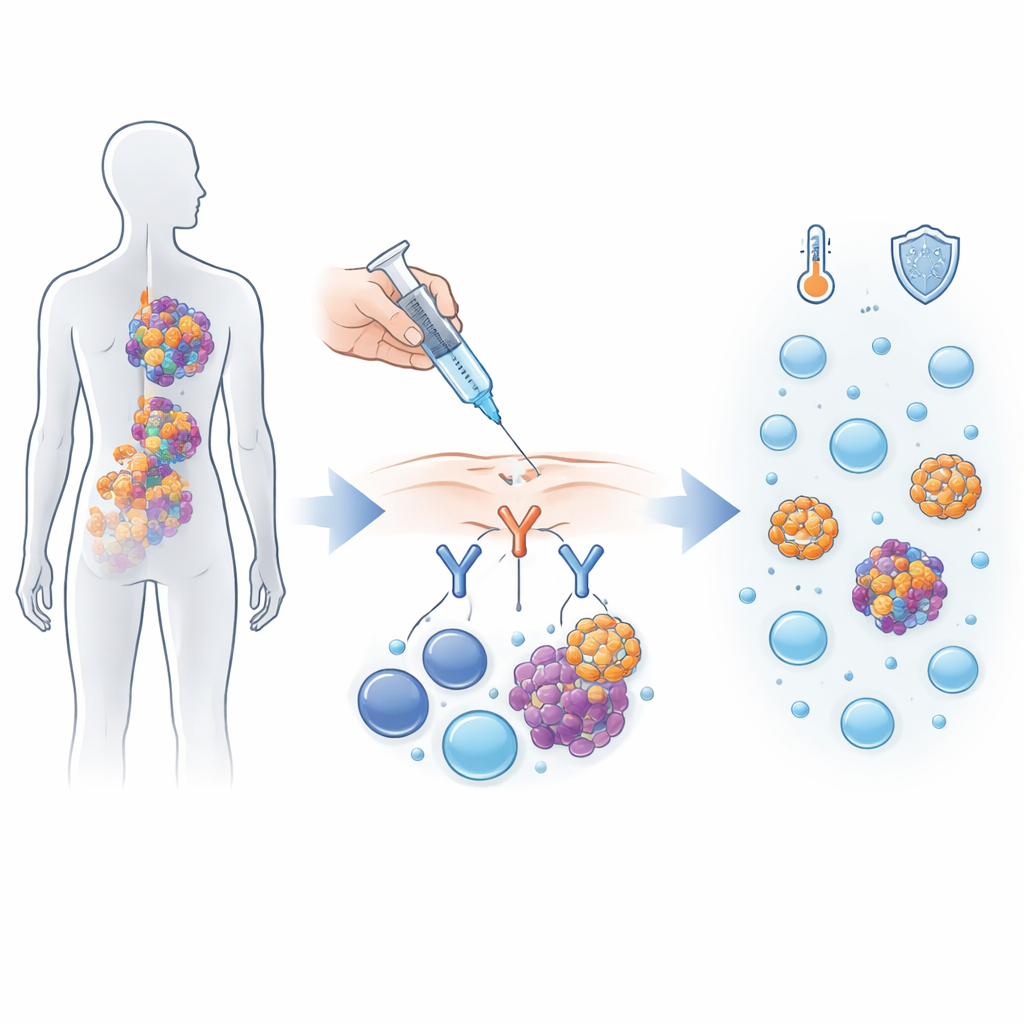
Una forma ingeniosa de redirigir el sistema inmune
Alnuctamab pertenece a una nueva clase de fármacos que actúan como casamenteros moleculares entre las células cancerosas y las células inmunitarias. Las células del mieloma múltiple portan en su superficie un marcador llamado BCMA, mientras que las células T del cuerpo llevan otro marcador, CD3. Alnuctamab está diseñado con dos “brazos” que se unen al BCMA y un brazo que se une al CD3, acercando las células T a las células de mieloma para que puedan atacarlas. En este primer ensayo en humanos, 165 personas con mieloma que había reaparecido tras al menos tres tipos diferentes de tratamiento recibieron alnuctamab, bien por infusión intravenosa o bien por inyección subcutánea bajo la piel.
De la infusión a la inyección
Al principio, el fármaco se administró por vía intravenosa, pero ese enfoque causó reacciones inmunitarias más intensas, incluida una episodio potencialmente letal de una complicación llamada síndrome de liberación de citocinas, en la que el sistema inmune libera de forma abrupta grandes cantidades de señales inflamatorias. Debido a estas preocupaciones de seguridad y a beneficios modestos, el estudio pasó a la dosificación subcutánea, que libera el fármaco de forma más gradual. Noventa y cinco pacientes fueron tratados así usando un esquema de “escalado”: pequeñas dosis iniciales seguidas de dosis objetivo más altas, con la frecuencia de las inyecciones reduciéndose progresivamente con el tiempo, de semanal a una vez cada cuatro semanas si el tratamiento continuaba.
Cómo les fue a los pacientes y a qué se enfrentaron
Entre todos los pacientes que recibieron las inyecciones subcutáneas, aproximadamente un 59% vieron su cáncer reducirse al menos a la mitad, y casi la mitad se convirtió en “negativa para enfermedad mínima residual”, es decir, pruebas muy sensibles ya no podían detectar células de mieloma en la médula ósea. En la dosis recomendada de 30 miligramos, las respuestas fueron incluso más fuertes: alrededor del 71% respondieron y más de la mitad lograron negatividad para enfermedad mínima residual. Muchos pacientes mantuvieron el control de su enfermedad durante cerca de un año o más, incluso cuando el esquema de dosificación se volvió menos intenso. Los efectos secundarios fueron frecuentes pero en su mayoría manejables. Reacciones tipo fiebre ocurrieron en aproximadamente tres de cada cinco pacientes, pero todas fueron leves o moderadas. Se observaron recuentos bajos de glóbulos blancos e infecciones, reflejo tanto de la potencia del fármaco como de la fragilidad del sistema inmune de los pacientes; sin embargo, las infecciones graves fueron menos frecuentes que las reportadas con varios fármacos similares.
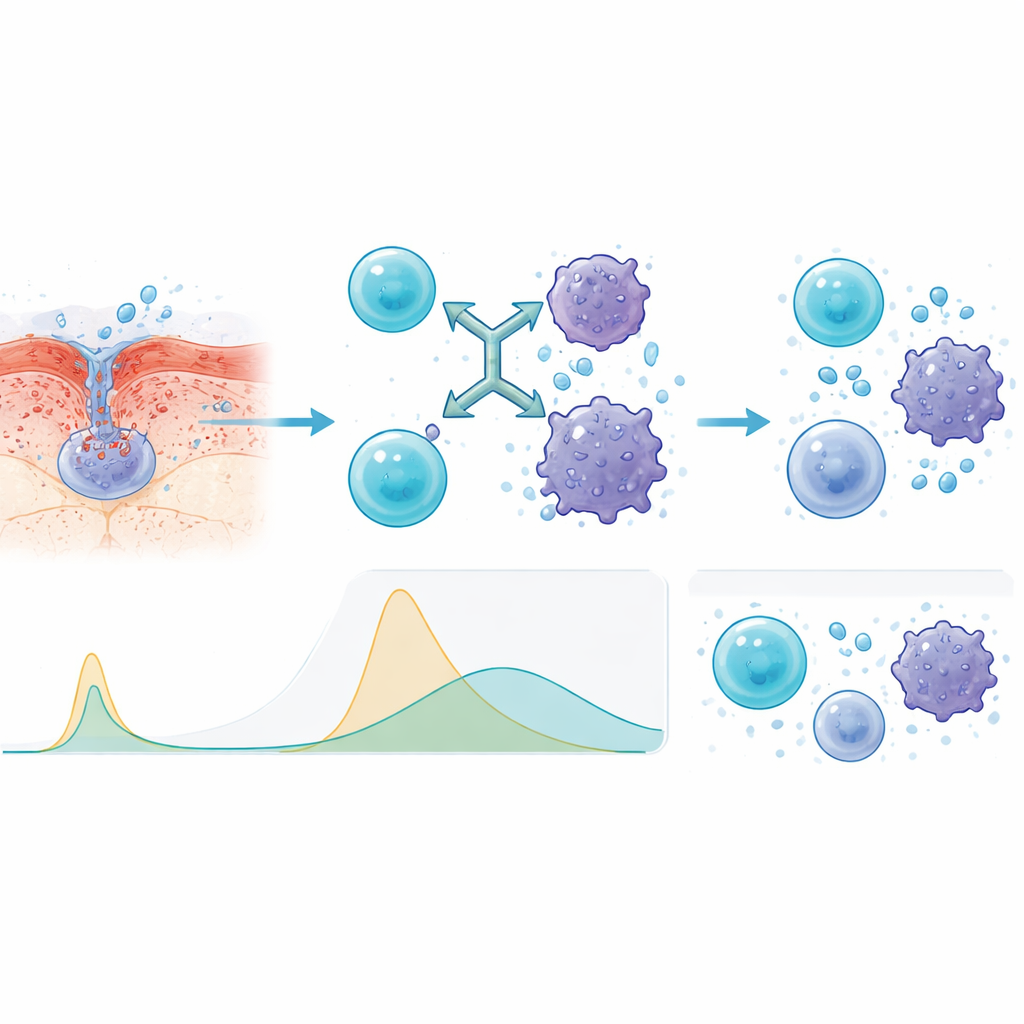
Por qué la vía subcutánea fue más segura
Para entender por qué el método subcutáneo funcionó mejor, los investigadores midieron moléculas de señalización inmune en la sangre. En comparación con la infusión intravenosa, las inyecciones produjeron picos más lentos y más bajos en señales inflamatorias clave como interleucinas y factor de necrosis tumoral. Este perfil más plano significa que el sistema inmune sigue activado contra el cáncer, pero sin la misma oleada súbita que puede poner a los pacientes en peligro. El equipo también encontró que las personas cuyo plasma mostraba niveles más bajos de BCMA desprendido al inicio—un signo de enfermedad menos agresiva o en estadio menos avanzado—tendían a responder mejor y a permanecer en remisión más tiempo.
Qué significa esto para la atención futura del mieloma
Aunque la compañía decidió posteriormente no continuar el desarrollo de alnuctamab por razones estratégicas, las lecciones de este ensayo son importantes. El estudio demuestra que un engajador inmunitario cuidadosamente diseñado puede administrarse como una inyección simple, en un calendario que se vuelve menos exigente con el tiempo, y aun así producir respuestas profundas y duraderas en muchas personas con mieloma de difícil tratamiento. También sugiere que aumentar la dosis de forma paulatina y evitar picos bruscos en la activación inmunitaria puede limitar las reacciones graves sin reducir la potencia anticancerígena. Estos conocimientos probablemente guiarán el diseño de futuras terapias basadas en el sistema inmune, ofreciendo la esperanza de que más pacientes con mieloma en recaída dispongan de tratamientos efectivos que no solo sean potentes, sino también más seguros y fáciles de sobrellevar.
Cita: Bar, N., Martin, T., Hofmeister, C.C. et al. Alnuctamab, a bivalent B-cell maturation antigen-targeting T cell engager for patients with relapsed or refractory multiple myeloma: results from a phase 1, first-in-human study. Leukemia 40, 481–490 (2026). https://doi.org/10.1038/s41375-025-02841-x
Palabras clave: mieloma múltiple, inmunoterapia, anticuerpo bispecífico, BCMA, engajador de células T