Clear Sky Science · es
Un agonista soluble de Notch permite la maduración de ameloblastos humanos y la formación de tejido similar al esmalte para la regeneración dental
Por qué es tan difícil reparar el esmalte dental
El esmalte, la capa blanca vidriosa que recubre nuestros dientes, es el material más duro del cuerpo humano—pero una vez que se pierde, no se regenera. Más del 90 por ciento de los adultos presentan algún grado de pérdida o daño del esmalte, y nuestros dientes carecen de un mecanismo natural para reconstruir esta capa protectora. Este estudio describe una forma de cultivar en el laboratorio células humanas productoras de esmalte, llevarlas a un estado de maduración completo e incluso inducirlas a formar mineral similar al esmalte en animales. El trabajo abre una vía hacia futuras terapias que podrían, algún día, reparar dientes con tejido vivo en lugar de empastes y coronas.
Construir esmalte dental a partir de células madre
El esmalte lo producen células especializadas llamadas ameloblastos, que mueren una vez que un diente erupciona a través de las encías. Sin ellas, los dientes adultos no pueden fabricar esmalte nuevo. Los investigadores usan células madre pluripotentes inducidas humanas—células adultas reprogamadas a un estado flexible parecido al embrionario—para crear “ameloblastos inducidos”. En trabajos previos, estas células cultivadas en laboratorio podían comenzar a parecerse a las naturales capacitadas para fabricar esmalte, pero se detenían antes de alcanzar la madurez completa, y solo funcionaban correctamente cuando crecían en estrecho contacto con odontoblastos, las células que forman la dentina subyacente. Eso planteó una pregunta clave: ¿qué aportan exactamente los odontoblastos que los ameloblastos necesitan para completar su desarrollo?
La conversación que faltaba entre las células dentales
Para descifrar este diálogo celular, el equipo analizó mapas de expresión génica a nivel de célula única de dientes humanos y de ratón en desarrollo. Buscaron vías de señalización que parecieran transmitirse específicamente de odontoblastos a ameloblastos durante la ventana clave en la que se forma el esmalte. Una vía destacó: Notch, un sistema de comunicación directa célula a célula ampliamente usado en el desarrollo embrionario. En estos mapas dentales, los ligandos tipo Delta (especialmente DLL1 y DLL4) se encontraban principalmente en los odontoblastos, mientras que los receptores Notch se concentraban en los ameloblastos en maduración. Cuando los investigadores bloquearon la actividad de Notch con un fármaco en su sistema de cocultivo, los ameloblastos redujeron drásticamente la producción de enamelina, una proteína mayor del esmalte—una evidencia contundente de que la señalización Notch es esencial para que las células formadoras de esmalte maduren. 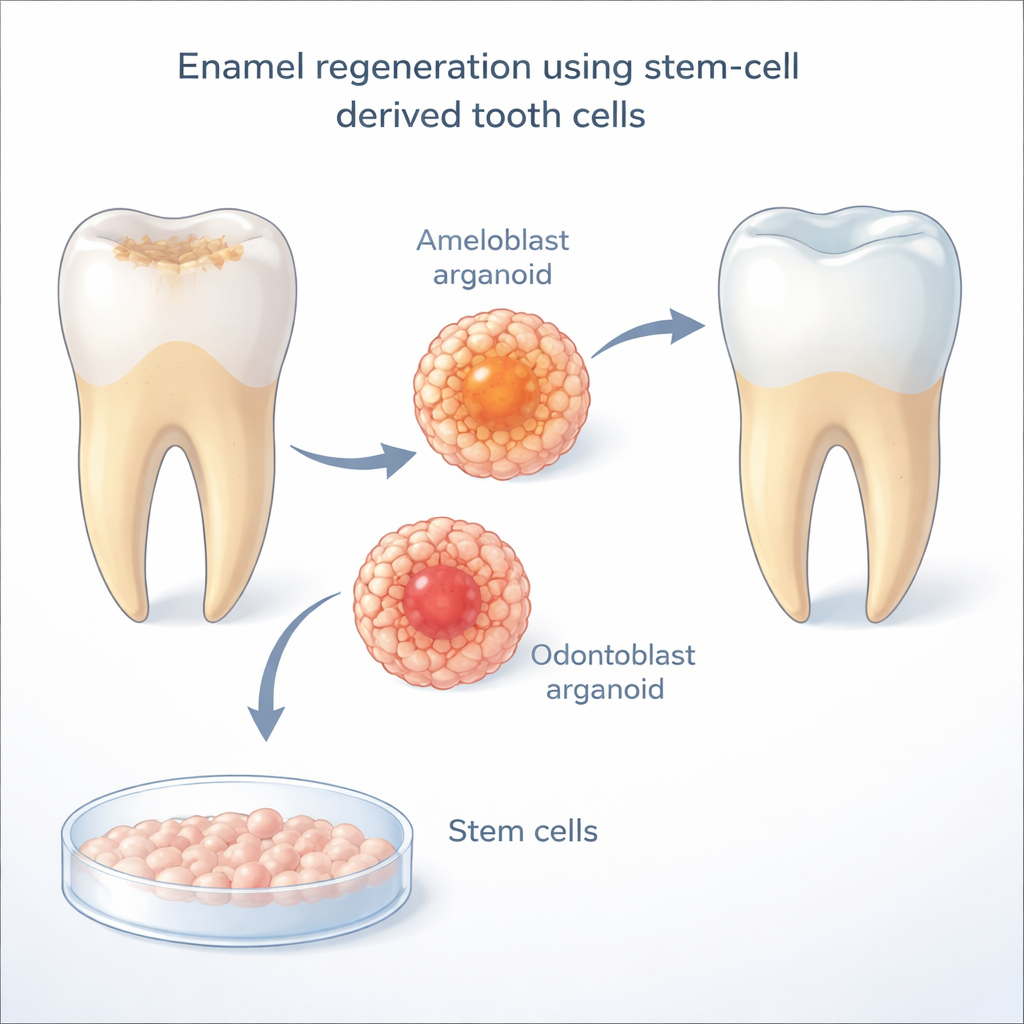
Un interruptor proteico diseñado por IA para las células del esmalte
Para avanzar, el equipo quiso activar Notch de forma precisa y controlable, sin depender de odontoblastos reales. Usaron una proteína artificial llamada C3‑DLL4, diseñada con herramientas computacionales. Esta molécula soluble dispone tres copias del dominio señalizador DLL4 en un armazón rígido de tres brazos, lo que le permite agrupar y activar receptores Notch en las células cercanas de manera análoga a una célula vecina natural. En líneas reporteras, C3‑DLL4 activó con fuerza genes dependientes de Notch. Al añadirse a organoides tempranos de ameloblastos—pequeños cúmulos 3D de células cultivadas a partir de células madre—provocó un cambio amplio en la actividad génica. Los organoides pasaron de un perfil inmaduro hacia uno que coincidía con ameloblastos secretorios y plenamente maduros, activando genes característicos como AMELX, ENAM, MMP20, ODAM, KLK4, TUFT1 y WDR72. La eliminación de la actividad Notch tuvo el efecto contrario: detuvo la maduración y perturbó la producción de proteínas del esmalte.
De organoides a tejido similar al esmalte
De forma notable, cuando estos organoides de ameloblastos activados por Notch se trasplantaron bajo la cápsula renal de ratones inmunodeficientes—un nicho bien vascularizado y seguro ampliamente usado para probar tejidos humanos—comenzaron a depositar material denso y mineralizado. Escaneos micro‑CT de alta resolución y técnicas clásicas de tinción confirmaron la presencia de nódulos calcificados donde normalmente no existe tal tejido. La microscopía mostró capas organizadas y polarizadas de células humanas que expresaban proteínas clave del esmalte y WDR72, un factor vinculado a la mineralización adecuada del esmalte. Aunque este material se describe mejor como “similar al esmalte” y no esmalte natural completo, demuestra que ameloblastos humanos diseñados pueden, en principio, depositar mineral duro en un organismo vivo. 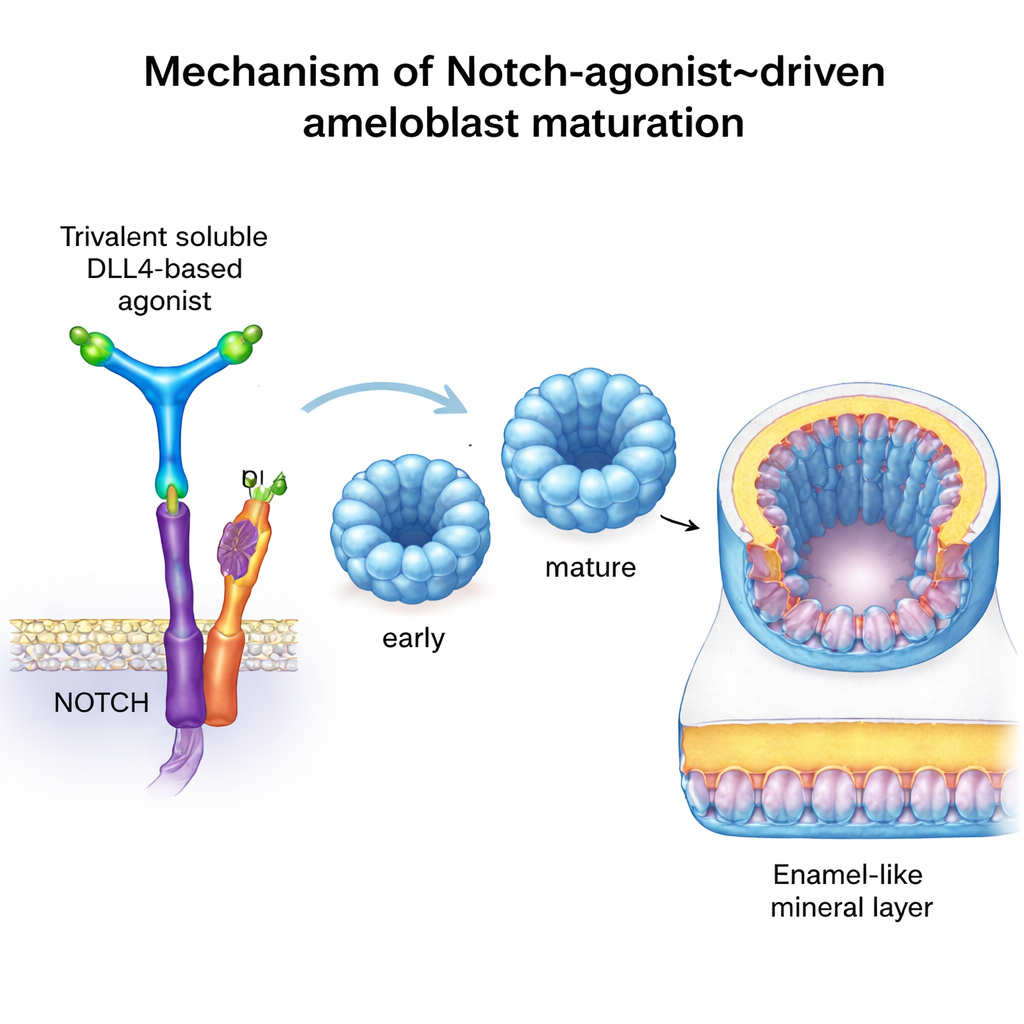
Resolver un misterio genético detrás del esmalte débil
El estudio también aborda un largo enigma en torno al gen DLX3, cuyas mutaciones provocan ciertos defectos hereditarios del esmalte y aumentan el riesgo de caries. DLX3 está activo tanto en ameloblastos como en odontoblastos, lo que dificulta saber qué tipo celular resulta más afectado cuando algo falla. Usando su sistema de organoides libre de odontoblastos y edición génica CRISPR, los investigadores eliminaron DLX3 específicamente en la línea de ameloblastos. Los primeros pasos de la formación de ameloblastos aún ocurrían, pero la fase final de maduración colapsó: proteínas clave del esmalte como enamelina, AMELX, MMP20, KLK4, TUFT1 y WDR72 se redujeron drásticamente tanto a nivel de ARN como de proteína. Esto demuestra que DLX3 es directamente necesario dentro de los ameloblastos humanos para completar el programa de fabricación del esmalte, y ayuda a explicar por qué variantes cerca de este gen se asocian a dientes frágiles y propensos a caries.
Qué podría significar esto para la atención dental futura
En conjunto, estos hallazgos trazan una hoja de ruta paso a paso desde células madre hasta organoides productores de esmalte y tejido parecido al esmalte in vivo, controlada por un “interruptor” Notch ajustable y por el gen DLX3. Aunque la regeneración clínica de dientes aún está lejos, este trabajo proporciona un campo de ensayo potente para entender enfermedades dentales genéticas, probar nuevos tratamientos y afinar estrategias para reconstruir el esmalte perdido con células vivas en lugar de materiales inertes. Para los pacientes, la esperanza a largo plazo es que las visitas al dentista puedan algún día implicar reparar dientes desgastados o cariados con esmalte bioingenierizado que se comporte mucho más como el real.
Cita: Patni, A.P., Mout, R., Alghadeer, A. et al. Soluble Notch agonist enables human ameloblast maturation and enamel-like tissue formation for tooth regeneration. Int J Oral Sci 18, 25 (2026). https://doi.org/10.1038/s41368-026-00429-4
Palabras clave: regeneración del esmalte, organoides de ameloblastos, señalización Notch, DLX3, células madre dentales