Clear Sky Science · es
ANKRD1 sostiene un nicho neurogénico en las CMM y contrarresta el envejecimiento cognitivo
Por qué la mandíbula podría importar para una mente envejecida
La mayoría piensa en el hueso de la mandíbula como algo importante para masticar y la odontología, no para la memoria. Este estudio sugiere un vínculo sorprendente: las células madre escondidas en la médula ósea de la mandíbula podrían ayudar a proteger el cerebro de la pérdida de memoria relacionada con la edad. Los investigadores se centraron en una proteína llamada ANKRD1, mostrando que ayuda a estas células madre procedentes de la mandíbula a conservar su potencial “neural” y, a su vez, respalda la salud cerebral y la memoria espacial en animales envejecidos.
Un nicho oculto favorable a las neuronas en el hueso mandibular
La médula ósea de la mandíbula contiene células estromales mesenquimales—células madre versátiles conocidas sobre todo por generar hueso y cartílago. Dado que la mandíbula se desarrolla a partir de una estructura llamada cresta neural, los autores se preguntaron si sus células madre podrían conservar cierta capacidad formadora de nervios. Mediante secuenciación de ARN a célula única, cartografiaron miles de células madre mandibulares individuales y descubrieron una subpoblación distinta que se parecía a progenitores neurales: altamente proliferativa, rica en genes vinculados al desarrollo neural y predispuesta a convertirse en células de tipo nervioso. Dentro de este nicho, ANKRD1 emergió como un marcador destacado, fuertemente asociado tanto al crecimiento como al potencial neurogénico.
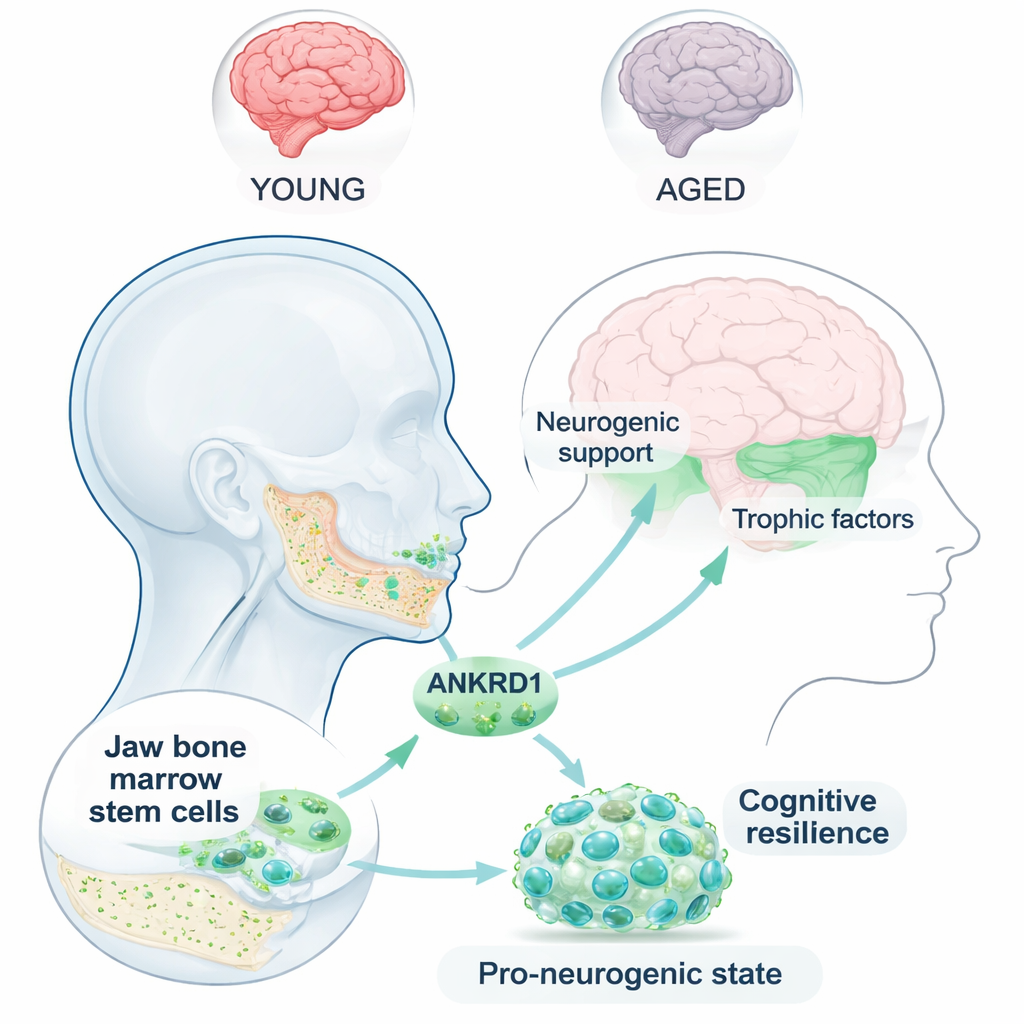
ANKRD1 como guardián contra el envejecimiento y la especialización prematura
Con la edad, muchas células madre pierden su flexibilidad y tienden al agotamiento. El equipo mostró que los niveles de ANKRD1 caen drásticamente en células madre mandibulares de donantes mayores y en células cultivadas en el laboratorio llevadas a un estado senescente, o envejecido. Cuando ANKRD1 se redujo experimentalmente en células jóvenes, aumentaron los marcadores clásicos de envejecimiento y las células comenzaron a comportarse como células viejas. A la inversa, aumentar ANKRD1 en células envejecidas redujo estas señales de senescencia. La proteína también ayudó a impedir que las células se comprometieran demasiado pronto con linajes óseos o adiposos: niveles bajos de ANKRD1 elevaron los marcadores de hueso y grasa, mientras que niveles altos los suprimieron. En términos sencillos, ANKRD1 ayuda a que las células madre mandibulares se mantengan juveniles y versátiles en lugar de agotarse o bloquearse en un destino único.
Manteniendo los genes neurales accesibles a nivel del ADN
Los autores preguntaron entonces cómo ejerce ANKRD1 un control tan amplio. Al perfilar dónde se sitúa ANKRD1 en el genoma, encontraron que se une con fuerza a regiones reguladoras potentes conocidas como súper potenciadores, en especial a las que controlan dos genes clave de células madre neurales, SOX2 y NESTIN. En células jóvenes y no diferenciadas, la ocupación de ANKRD1 en estos sitios coincidía con cromatina abierta y accesible—la arquitectura relajada del ADN que permite activar genes. A medida que las células se diferenciaban o envejecían, la unión de ANKRD1 en regiones de control distantes disminuía, la cromatina se compactaba y las vías neurales se volvían menos activas. Experimentos con reporteros confirmaron que ANKRD1 puede aumentar directamente la actividad de elementos reguladores de SOX2 y NESTIN. Combinado con mapeos 3D del genoma, estos resultados sugieren que ANKRD1 mantiene un “reservorio neurogénico” en las células madre mandibulares al mantener genes neurales clave en una configuración abierta y lista para activarse.
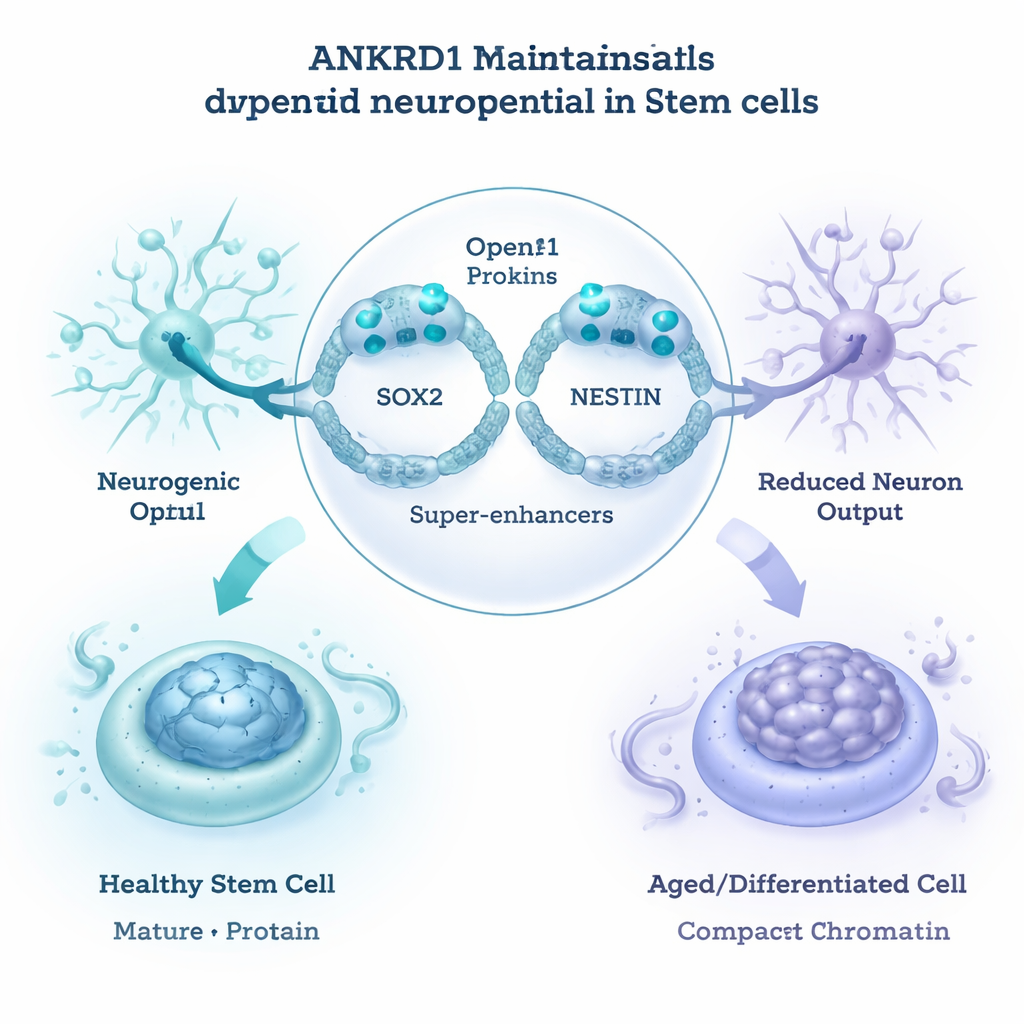
De las células madre mandibulares a mejor memoria en ratones ancianos
Si ANKRD1 mantiene abiertas las opciones neurales en las células madre, ¿puede realmente mejorar la función cerebral? Para probarlo, los investigadores entregaron ANKRD1 específicamente a neuronas de ratones envejecidos de forma natural usando un vector viral diseñado para cruzar la barrera hematoencefálica. El tratamiento no cambió el movimiento ni el comportamiento ansioso, pero mejoró significativamente el rendimiento en el laberinto acuático de Morris, una prueba clásica de aprendizaje y memoria espacial. Los ratones tratados aprendieron más rápido la ubicación de la plataforma y buscaron con más precisión en el cuadrante correcto. En experimentos de laboratorio en paralelo, aumentar los niveles de ANKRD1 hizo que las células madre mandibulares expresaran más marcadores neuronales, adoptaran formas similares a las de neuronas y secretaran mayores cantidades de factores de apoyo cerebral como NGF y BDNF, lo que sugiere un beneficio doble: mejor capacidad neurogénica intrínseca y un entorno de apoyo más rico.
Reconfigurando patrones de actividad cerebral en regiones clave de la memoria
Para ver cómo ANKRD1 remodela la función cerebral, el equipo mapeó la actividad neuronal en todo el cerebro del ratón usando c-Fos, una proteína que se ilumina en células recientemente activas. Los ratones tratados con ANKRD1 mostraron una activación más intensa en regiones cruciales para la cognición, incluida la formación hipocampal, el hipotálamo y la corteza cerebral externa. Estas áreas no solo se volvieron más activas, sino también más sincronizadas entre sí, cambiando de patrones fragmentados hacia redes más integradas y correlacionadas positivamente. Se piensa que este patrón de activación coordinada favorece un procesamiento de la información más eficiente y podría sustentar la mejora de la memoria observada en las pruebas conductuales.
Qué significa esto para la salud cerebral futura
En conjunto, el estudio presenta a ANKRD1 como un interruptor molecular clave que preserva la capacidad formadora de neuronas en las células madre de la médula ósea mandibular y ayuda a estabilizar las redes cerebrales durante el envejecimiento. Al mantener genes neurales cruciales accesibles y fomentar tanto la producción de neuronas como la liberación de factores protectores, ANKRD1 respalda la resiliencia de los circuitos de la memoria. Si bien la traducción a humanos requerirá cautela, el trabajo abre la puerta a terapias que aprovechen los orígenes de desarrollo únicos de las células madre mandibulares y su “memoria” de cromatina para contrarrestar el envejecimiento cognitivo.
Cita: Wang, Z., Liu, X., Zhen, W. et al. ANKRD1 sustains a neurogenic BMSC niche and counters cognitive aging. Int J Oral Sci 18, 23 (2026). https://doi.org/10.1038/s41368-026-00428-5
Palabras clave: envejecimiento cognitivo, células madre de médula ósea de la mandíbula, ANKRD1, neurogénesis, memoria espacial