Clear Sky Science · es
Atlas transcripcional unicelular revela mecanismos distintos de comunicación inmuno-condrocito en la artrosis de la articulación temporomandibular inducida por diferentes tipos de desorden oclusal
Por qué importa tu articulación mandibular
Las pequeñas articulaciones delante de tus orejas, llamadas articulaciones temporomandibulares (ATM), te permiten hablar, masticar, bostezar y reír. Cuando desarrollan artrosis, las acciones cotidianas pueden volverse dolorosas y difíciles. Este estudio utiliza análisis genético unicelular de vanguardia en ratones para explorar estas articulaciones célula por célula, revelando cómo diferentes problemas de mordida desencadenan distintos tipos de daño —y cómo eso podría orientar tratamientos más precisos.
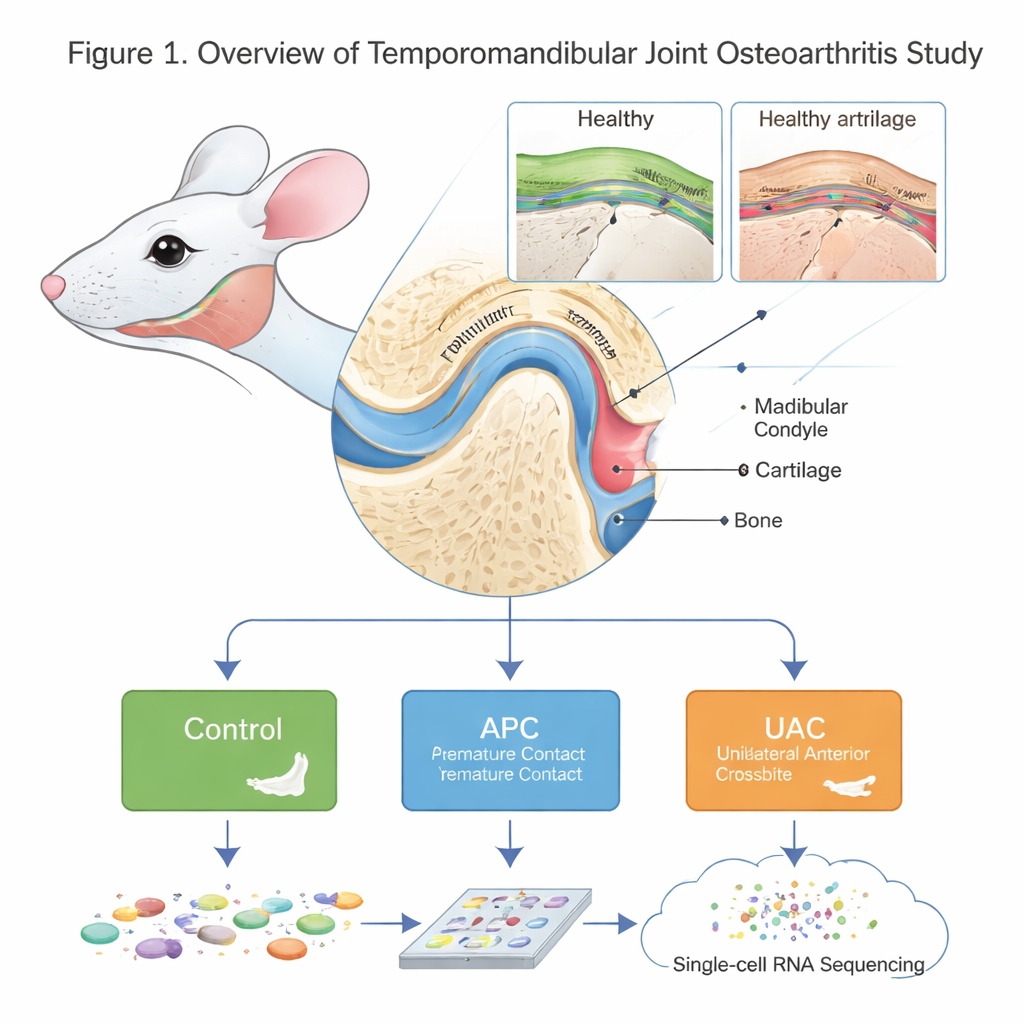
Examinando de cerca una articulación pequeña pero compleja
La ATM no es una simple bisagra. Su extremo redondeado, el cóndilo mandibular, está cubierto por un tipo especial de cartílago y apoyado por hueso subyacente. La artrosis en esta articulación (ATMO) provoca dolor, rigidez y pérdida de función, pero sus causas microscópicas y moleculares han sido difíciles de desentrañar. Los autores crearon un detallado “atlas celular” del cóndilo de ratón en salud y enfermedad usando secuenciación de ARN unicelular, una técnica que lee qué genes están activos en miles de células individuales. Compararon ratones sanos con dos modelos de desequilibrio de la mordida: contacto prematuro anterior (CPA), donde los dientes frontales se encuentran demasiado pronto, y mordida cruzada anterior unilateral (MCAU), donde un lado de los dientes frontales muerde de forma incorrecta, ambos conocidos por sobrecargar la articulación mandibular.
Muchos tipos de células del cartílago, no solo una
Tradicionalmente, el cartílago condilar se ha descrito en capas amplias: células proliferativas, maduras e hipertróficas. Este estudio muestra que la realidad es mucho más variada. El equipo identificó múltiples subtipos de condrocitos, cada uno con su propio perfil de expresión génica y probable función. Había células progenitoras cerca de la superficie que actúan como reserva reparadora, condrocitos fibróticos implicados en una matriz similar a cicatriz y en la reparación, condrocitos asociados a la inflamación que producen señales inflamatorias, condrocitos asociados a la mineralización e hipertróficos que facilitan la transformación del cartílago en hueso, y células reparativas que atenúan el estrés y la inflamación. En articulaciones sanas, estos subtipos se disponen en un patrón espacial ordenado y siguen una “trayectoria” de desarrollo suave desde progenitores hacia estados más maduros.
Cuando los problemas de mordida alteran el orden celular de la articulación
Tanto los modelos CPA como MCAU condujeron a un cartílago más fino, rugosidad superficial y lesiones típicas de artrosis en el cóndilo. A nivel celular, disminuyó la proporción de condrocitos mientras aumentaron las células inmunitarias. En CPA hubo un aumento marcado de ciertos condrocitos mineralizantes e hipertróficos y una alteración de la progresión normal de progenitor a células maduras. En MCAU también se incrementaron los condrocitos fibróticos y reparativos, lo que sugiere un intento de reparación y remodelado más intenso. La microscopía confirmó que las células perdieron sus capas ordenadas y se volvieron compactas y desorganizadas en el cartílago enfermo, coincidiendo con las trayectorias de desarrollo perturbadas inferidas a partir de los datos de expresión génica.
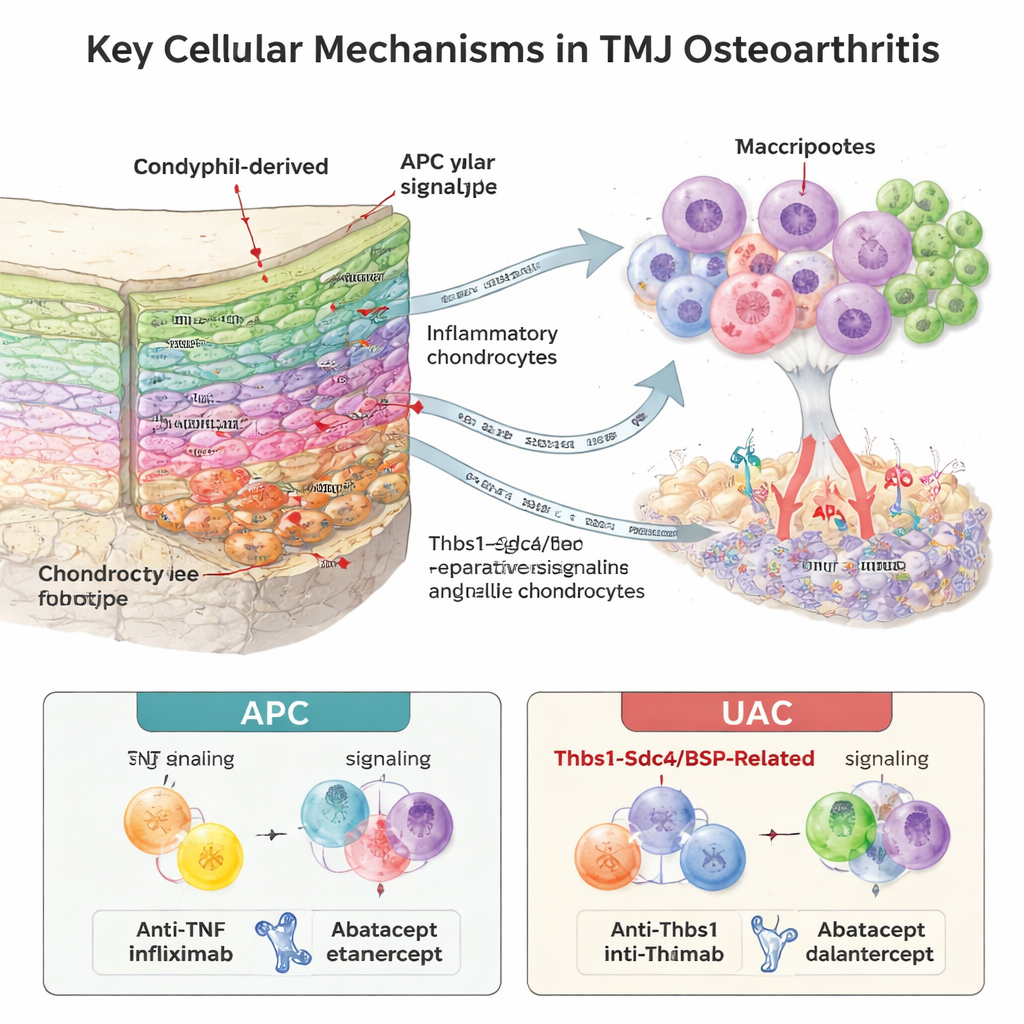
Las células inmunitarias, los vasos sanguíneos y el cartílago se comunican entre sí
El hueso y la médula que soportan el cóndilo albergaron un entorno inmunitario sorprendentemente rico. Los investigadores encontraron nueve tipos de células inmunitarias, con una expansión marcada de neutrófilos (un glóbulo blanco de acción rápida) en las articulaciones enfermas, especialmente en una etapa de maduración concreta. Mediante el análisis de qué moléculas de señalización y receptores se coexpresaban, inferieron una intensa “comunicación” entre células inmunitarias y condrocitos. En el modelo CPA, los neutrófilos se convirtieron en la principal fuente de TNF‑alfa, una potente señal inflamatoria, enviando mensajes dañinos al cartílago. En el modelo MCAU emergió un patrón diferente: señales vinculadas al hueso y al cartílago que implican la sialoproteína ósea (BSP) y la vía Thbs1–Sdc4 fueron más prominentes, y estas se relacionaron estrechamente con el crecimiento de nuevos vasos en el borde cartílago–hueso. Las áreas ricas en BSP se superpusieron con marcadores de angiogénesis, lo que sugiere que los vasos invasores y las células inmunitarias reclutadas impulsan conjuntamente la erosión del cartílago.
Tratamientos a medida según el tipo de estrés en la articulación
Para comprobar si estas señales distintas realmente importan, el equipo trató a los ratones durante el desarrollo de la enfermedad con fármacos que bloquean vías específicas. En la ATMO inducida por CPA, bloquear TNF‑alfa con el fármaco etanercept protegió claramente el cartílago, mientras que un fármaco dirigido a receptores que atraen neutrófilos (Navarixin) tuvo poco efecto. En contraste, en la ATMO inducida por MCAU, Navarixin alivió de forma significativa el daño del cartílago, coherente con un proceso patológico más dependiente de la invasión vascular y el remodelado impulsados por neutrófilos, mientras que etanercept tuvo un efecto más débil. Estos hallazgos sugieren que la artrosis de la ATM no es una sola enfermedad, sino un conjunto de condiciones relacionadas determinadas por cómo se somete la articulación al estrés, y que las terapias efectivas podrían necesitar adaptarse a los patrones mecánicos y celulares específicos de cada paciente.
Qué significa esto para las personas con dolor mandibular
Para quien padece chasquidos mandibulares, dolor o limitación en la apertura, esta investigación subraya dos ideas clave. Primero, la articulación mandibular está mantenida por una comunidad diversa de células del cartílago e inmunitarias que pueden proteger o dañar el tejido según cómo se activen. Segundo, distintos problemas de mordida pueden empujar a esta comunidad hacia vías dañinas diferentes: una más impulsada por la inflamación clásica y otra por el crecimiento anómalo de vasos sanguíneos y el remodelado hueso‑cartílago. A largo plazo, este tipo de cartografía unicelular podría ayudar a dentistas y médicos a ir más allá de tratamientos uniformes y avanzar hacia enfoques que combinen la corrección de la mordida con fármacos dirigidos elegidos según el patrón específico de daño articular del paciente.
Cita: Wang, K., Li, Y., Xiang, S. et al. Single-cell transcriptional atlas reveals distinct immune-chondrocyte crosstalk mechanisms in temporomandibular joint osteoarthritis induced by different types of occlusal disorder. Int J Oral Sci 18, 22 (2026). https://doi.org/10.1038/s41368-025-00424-1
Palabras clave: artrosis de la articulación temporomandibular, secuenciación de ARN unicelular, condrocitos, neutrófilos, desorden oclusal