Clear Sky Science · es
La implantación activa el potencial osteogénico periimplante a través de la transducción mecánica mediada por el eje Snx5‑EGFR
Por qué es importante conservar el hueso mandibular tras la pérdida de un diente
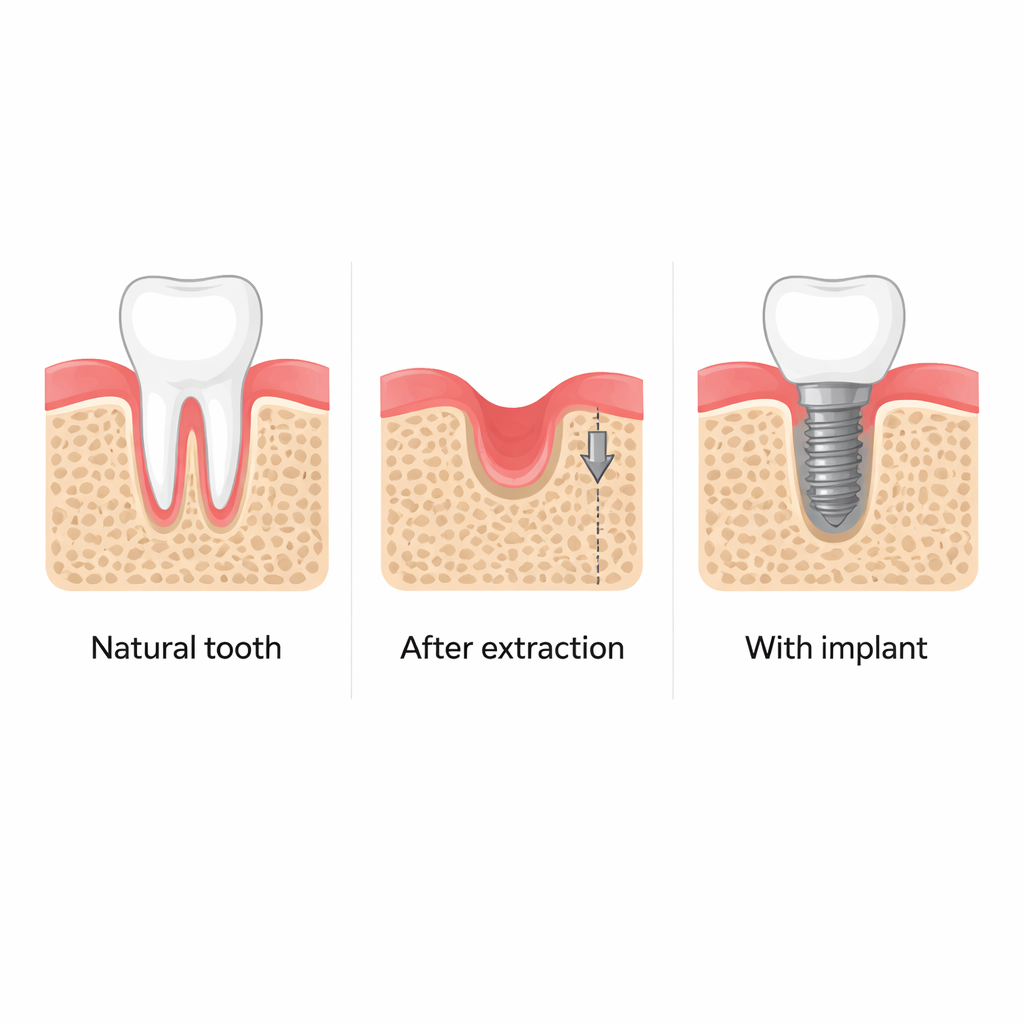
Cuando se extrae un diente, el hueso circundante de la mandíbula a menudo se reabsorbe, lo que dificulta la colocación de implantes dentales estables más adelante y afecta la apariencia facial. Los dentistas han observado durante mucho tiempo que simplemente colocar un implante en el alveolo recién extraído parece ayudar a preservar ese hueso, incluso antes de que el implante se utilice para masticar. Este estudio plantea una pregunta simple pero importante: ¿cómo el acto de colocar el implante «despierta» el sistema de reparación ósea, y podemos aprovechar ese proceso para mejorar la regeneración mandibular?
Implantes como protectores silenciosos del hueso
Escaneos clínicos de pacientes y experimentos detallados en ratones confirman que colocar un implante dental poco después de la extracción ayuda a mantener la altura y el grosor del hueso mandibular circundante. En contraste, los alveolos dejados para sanar por sí solos pierden una cantidad considerable de hueso a lo largo de varios meses. Alrededor de los implantes, los investigadores encontraron más células inmaduras formadoras de hueso (osteoprogenitoras), lo que indica que el tejido junto al poste metálico es biológicamente más activo. Esta actividad aumentada parece deberse no a las fuerzas de la masticación, sino a las tensiones mecánicas inusuales que se crean cuando un implante ajustado se atornilla en un hueso ligeramente de menor tamaño.
Un interruptor oculto dentro de las células madre óseas
El equipo se centró en un grupo especial de células madre de la médula ósea marcadas por una proteína llamada LepR, conocidas por ser proveedoras clave de nuevo hueso en adultos. Al comparar la actividad génica en estas células procedentes de hueso normal, hueso adyacente al implante y células sometidas a estrés en el laboratorio, identificaron una molécula, sorting nexin 5 (Snx5), cuyos niveles disminuían de forma consistente cuando estaban presentes señales mecánicas. En las zonas alrededor de los implantes, las células LepR con baja expresión de Snx5 eran más propensas a portar marcadores de células formadoras de hueso tempranas, lo que sugiere que la reducción de Snx5 ayuda a empujar a estas células madre silenciosas hacia un estado activo de formación ósea.
Cuando el interruptor está roto, el hueso no percibe bien la fuerza
Para probar qué hace realmente Snx5, los investigadores utilizaron ratones y células madre carentes de esta proteína. Sin Snx5, las células madre mostraron una fuerte tendencia intrínseca a formar hueso, incluso sin estimulación adicional. Pero cuando los científicos aplicaron estiramiento mecánico —imitando las deformaciones cerca de un implante—, las células normales aumentaron su actividad formadora de hueso, mientras que las células deficientes en Snx5 apenas respondieron. En ratones vivos, los implantes en animales normales provocaron un claro crecimiento de hueso nuevo alrededor del poste de titanio. En contraste, los ratones sin Snx5 no ganaron hueso adicional tras la implantación, lo que revela que Snx5 es crucial para convertir las señales mecánicas en reparación ósea adicional, más que para la formación ósea basal en sí.
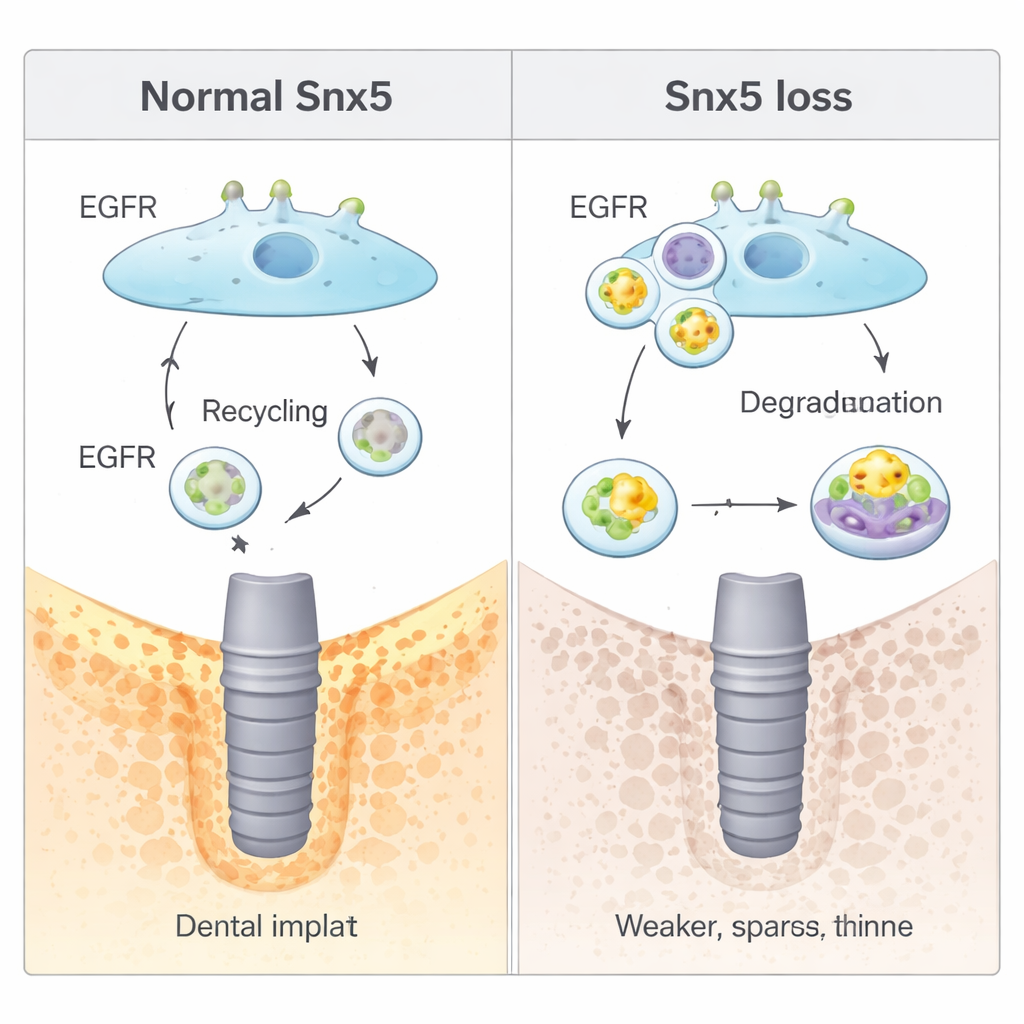
Cómo una vía de reciclaje controla las señales óseas
El estudio reveló luego cómo funciona Snx5 a nivel molecular. Muchas señales de crecimiento en las células viajan a través de receptores en la superficie celular que son continuamente internalizados y luego reciclados o destruidos. Snx5 pertenece a una familia de proteínas de «clasificación» que guían este tráfico. Aquí, se demostró que Snx5 dirige al receptor del factor de crecimiento epidérmico (EGFR) —un regulador clave del crecimiento celular y la diferenciación ósea— de vuelta a la membrana celular después de su internalización. Cuando faltaba Snx5, más EGFR se desviaba hacia compartimentos «digestivos» celulares (lisosomas) y se degradaba. Esto reducía la señalización de EGFR, lo que de manera inesperada aumentaba la formación ósea basal pero dejaba a las células menos capaces de ajustar su comportamiento cuando cambiaban las fuerzas mecánicas. Fármacos que activaban artificialmente EGFR atenuaban la formación ósea extra observada sin Snx5, mientras que fármacos que bloqueaban la degradación lisosomal restauraban las señales de EGFR y de nuevo reducían la formación ósea.
Qué significa esto para los futuros pacientes con implantes
Para el público general, estos hallazgos sugieren que la mandíbula contiene un sistema incorporado que puede detectar el sutil empuje y tirón creado cuando se coloca un implante y traducirlo en crecimiento óseo adicional. Snx5 actúa como un controlador de tráfico que mantiene un receptor de crecimiento clave, EGFR, circulando al nivel justo para que las células madre óseas puedan «oír» y responder a esos susurros mecánicos. Cuando este controlador se altera, el hueso puede formarse más fácilmente en reposo, pero pierde su respuesta fina a la fuerza. Entender este eje Snx5–EGFR abre la puerta a nuevos tratamientos —fármacos o recubrimientos para la superficie de los implantes— que podrían ajustar la sensibilidad mecánica del hueso, ayudando a preservar la mandíbula y a mejorar el éxito de los implantes en situaciones clínicas difíciles.
Cita: Jiang, X., Weng, Y., Feng, Y. et al. Implantation awakens peri-implant osteogenic potential via Snx5-EGFR axis-mediated mechanical transduction. Int J Oral Sci 18, 18 (2026). https://doi.org/10.1038/s41368-025-00423-2
Palabras clave: implantes dentales, regeneración del hueso mandibular, mecanotransducción, células madre óseas, señalización EGFR