Clear Sky Science · es
La vía glicolítica KDM6B/Pdk1 que impulsa la lactilación de ZEB2 promueve la formación de cemento celular
Por qué proteger las raíces dentales importa
La enfermedad de las encías, o periodontitis, es una de las principales causas de pérdida dental en adultos. A medida que avanza la enfermedad, erosiona silenciosamente los tejidos que anclan los dientes al maxilar. Uno de los más importantes es el cemento, una capa delgada y similar al hueso que recubre la superficie de la raíz y permite que el diente se "ate" al ligamento y al hueso circundantes. Una vez que se pierde el cemento, los dientes se aflojan y pueden acabar cayéndose. Este estudio plantea una pregunta sencilla pero potente: ¿podemos entender, en detalle molecular, cómo se construye el cemento para que algún día podamos ayudar al cuerpo a reconstruirlo y mantener los dientes en su lugar de por vida?
De las células que sostienen el diente a un objetivo terapéutico
El cemento lo producen células especializadas llamadas cementoblastos, que se sitúan en la superficie de la raíz y depositan nuevo mineral. Estas células se comportan de forma similar a las formadoras de hueso, pero las señales que les indican cuándo y cómo construir cemento se conocían poco. Los investigadores se centraron en una molécula llamada KDM6B, una enzima que edita etiquetas químicas en las proteínas que empaquetan el ADN y puede activar genes. Estudiando dientes de ratón a distintas edades y cementoblastos cultivados en el laboratorio, encontraron que los niveles de KDM6B aumentan durante la fase activa de formación de cemento y disminuyen cuando el crecimiento se ralentiza. Cuando bloquearon KDM6B en células o en ratones, la actividad de los cementoblastos descendió y la porción “celular” del cemento —la parte más gruesa y viva cerca del extremo de la raíz— se volvió más delgada, lo que sugiere que KDM6B es un promotor clave del crecimiento saludable del cemento.
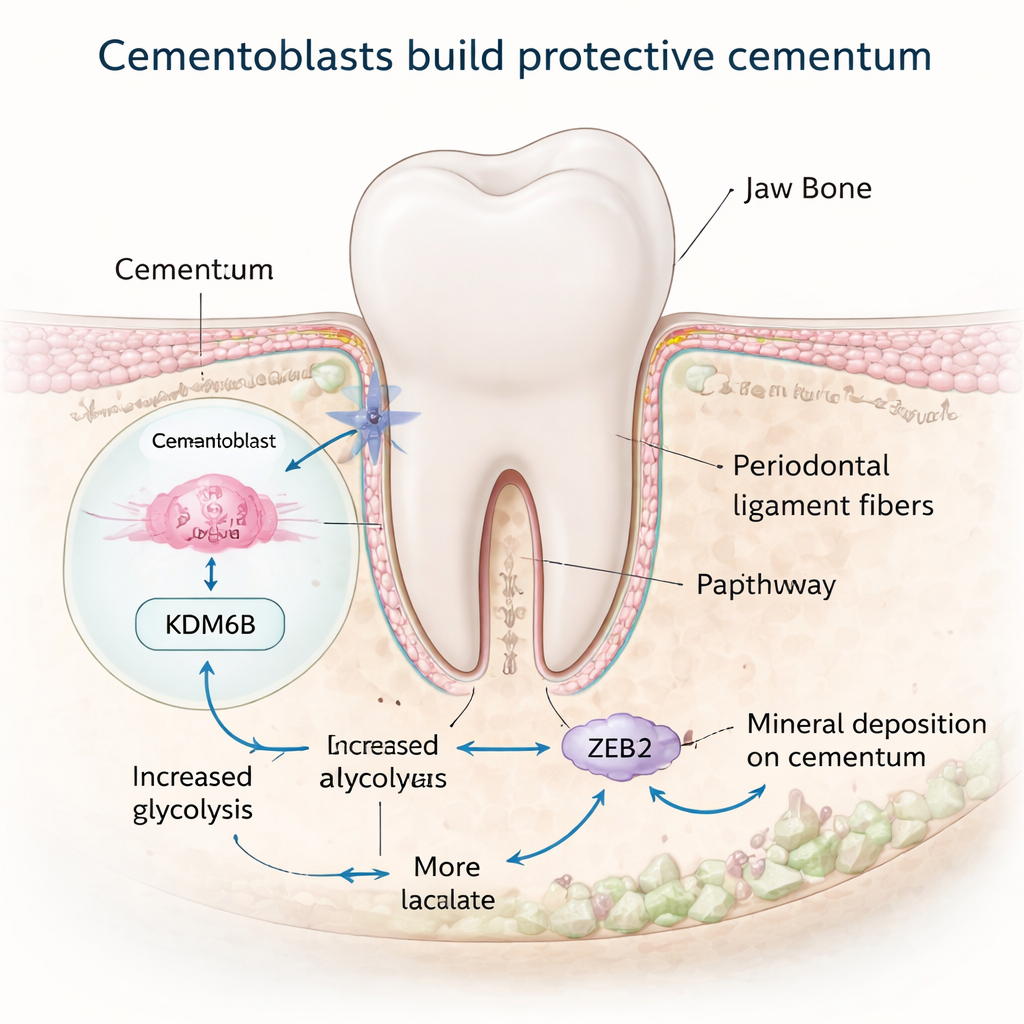
Reconfigurar el metabolismo celular para construir mineral
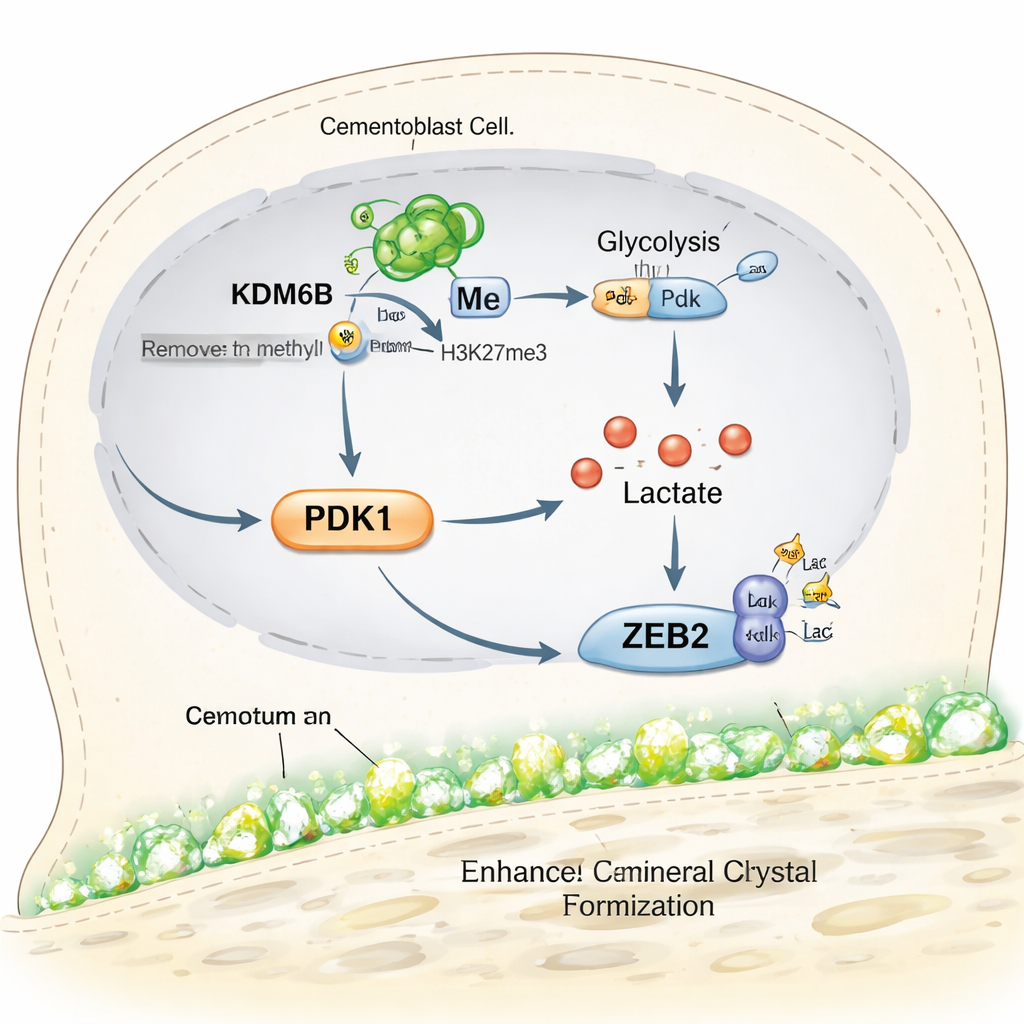
Construir tejido mineralizado requiere mucha energía, y muchas células cambian su metabolismo a un estado de alta producción mientras lo hacen. El equipo descubrió que KDM6B ayuda a los cementoblastos a reprogramar el uso de la glucosa. Normalmente, estas células favorecen una vía llamada glucólisis, que descompone rápidamente la glucosa y produce lactato. Cuando KDM6B se redujo, los genes implicados en la glucólisis se silenciaron, mientras que los asociados a una producción de energía más lenta y dependiente del oxígeno se mantuvieron o aumentaron, y las células generaron menos energía en general. Un actor central en este cambio fue la enzima PDK1. Mediante herramientas de mapeo del genoma, los investigadores mostraron que KDM6B elimina físicamente una marca represora de la región del ADN que controla el gen Pdk1, permitiendo que aumenten los niveles de PDK1. Restaurar PDK1 en células deficientes en KDM6B recuperó muchos marcadores de formación de mineral, revelando un interruptor metabólico KDM6B–PDK1 que potencia los cementoblastos.
Convertir el lactato de desecho en una señal útil
El lactato a menudo se considera un producto de desecho de músculos trabajosos, pero trabajos recientes han mostrado que también puede actuar como señal que modifica proteínas. Aquí, una mayor glucólisis impulsada por KDM6B y PDK1 aumentó la producción de lactato en cementoblastos. Los investigadores rastrearon entonces un tipo más reciente de modificación de proteínas llamada lactilación, en la que se añaden etiquetas derivadas del lactato a sitios específicos de las proteínas. Encontraron que los niveles de lactilación en los cementoblastos aumentaban durante los periodos de formación activa de cemento y disminuían en ratones envejecidos y en células deficientes en KDM6B. Añadir lactato sódico simple al sistema incrementó la lactilación, reactivó genes relacionados con el mineral y restauró la formación de nódulos minerales tanto en cultivos como en un modelo de ratón, incluso cuando KDM6B estaba bloqueado. Esto sugiere que el propio lactato puede ayudar a rescatar la actividad debilitada de construcción de cemento.
Un impulso molecular para un regulador clave del cemento
El equipo se preguntó entonces qué proteínas estaban siendo “decoradas” por lactato de forma relevante para el cemento. Se centraron en ZEB2, una proteína reguladora génica ya conocida por promover la mineralización de cementoblastos. Usando técnicas de mapeo proteico, identificaron sitios específicos en ZEB2 que presentan marcas de lactilación y mostraron que alterar un sitio crítico debilitaba la capacidad de la célula para activar genes de mineralización. Experimentos adicionales demostraron que la vía KDM6B–PDK1 potencia la lactilación de ZEB2 y que suministrar lactato extra puede restaurar la actividad de ZEB2 cuando PDK1 es bajo. En esencia, el metabolismo y el control génico están vinculados: la descomposición de azúcares alimenta la producción de lactato, que a su vez ajusta finamente a ZEB2 para mantener activos los programas de formación de cemento.
Qué significa esto para futuras terapias para salvar dientes
En pocas palabras, el estudio revela una cadena de acontecimientos dentro de las células formadoras de cemento: la enzima KDM6B abre el gen Pdk1, PDK1 empuja a las células hacia un uso rápido de azúcares, ese metabolismo genera lactato, y el lactato ajusta químicamente la proteína ZEB2 para impulsar la deposición de mineral. Cuando se bloquea cualquier paso de esta cadena, el crecimiento del cemento falla, pero añadir lactato con cuidado puede restaurarlo en parte. Para los pacientes, este trabajo aún no se traduce en un tratamiento clínico, pero destaca nuevos y precisos objetivos para fármacos o biomateriales diseñados para regenerar el cemento y estabilizar dientes en la periodontitis avanzada. También sugiere que interruptores metabólicos similares podrían aprovecharse para fomentar la reparación ósea en otras partes del cuerpo.
Cita: Yang, Z., Wang, H., Xiao, J. et al. KDM6B/Pdk1 glycolytic pathway-driven ZEB2 lactylation promotes cellular cementum formation. Int J Oral Sci 18, 21 (2026). https://doi.org/10.1038/s41368-025-00420-5
Palabras clave: regeneración del cemento, periodontitis, metabolismo de cementoblastos, desmetilasa de histonas KDM6B, lactilación de proteínas