Clear Sky Science · es
Información estructural sobre mutaciones asociadas a enfermedades en la maquinaria de procesamiento de microARN
Cómo las pequeñas tijeras de ARN moldean la salud y la enfermedad
Dentro de cada célula existe un sistema de edición oculto que recorta mensajes genéticos antes de que se lean. Este sistema depende de diminutos fragmentos de ARN llamados microARN, que actúan como perillas de afinación para miles de genes a la vez. Cuando las "máquinas" moleculares que producen microARN funcionan correctamente, las células crecen, se dividen y se especializan de forma controlada. Pero cuando estas máquinas se dañan por mutaciones, el equilibrio de la actividad génica puede inclinarse hacia el cáncer, trastornos hematológicos o problemas en el desarrollo cerebral. Este artículo explica cómo entender las formas tridimensionales de estas máquinas ayuda a los científicos a identificar qué falla y cómo podría repararse.
La caja de herramientas de la célula para atenuar genes
Los microARN son fragmentos cortos de ARN, de unos 22 nucleótidos, que no codifican proteínas por sí mismos. En lugar de eso, se unen a ARN mensajero más largos y los marcan para su destrucción o impiden su traducción, atenuando la expresión génica en vez de apagarla por completo. Para fabricar estos microARN, las células pasan precursores de ARN más largos por una línea de ensamblaje cuidadosamente escalonada. Primero, la enzima DROSHA recorta los transcritos primarios voluminosos en el núcleo celular en piezas más cortas con forma de horquilla. Estas piezas se desplazan luego al citoplasma, donde otra enzima, DICER, mide y corta para obtener dímeros del tamaño de microARN. Finalmente, una de las hebras de cada dímero se carga en una proteína llamada Argonaute 2 (AGO2), que usa el microARN como guía para encontrar mensajes coincidentes y silenciarlos. 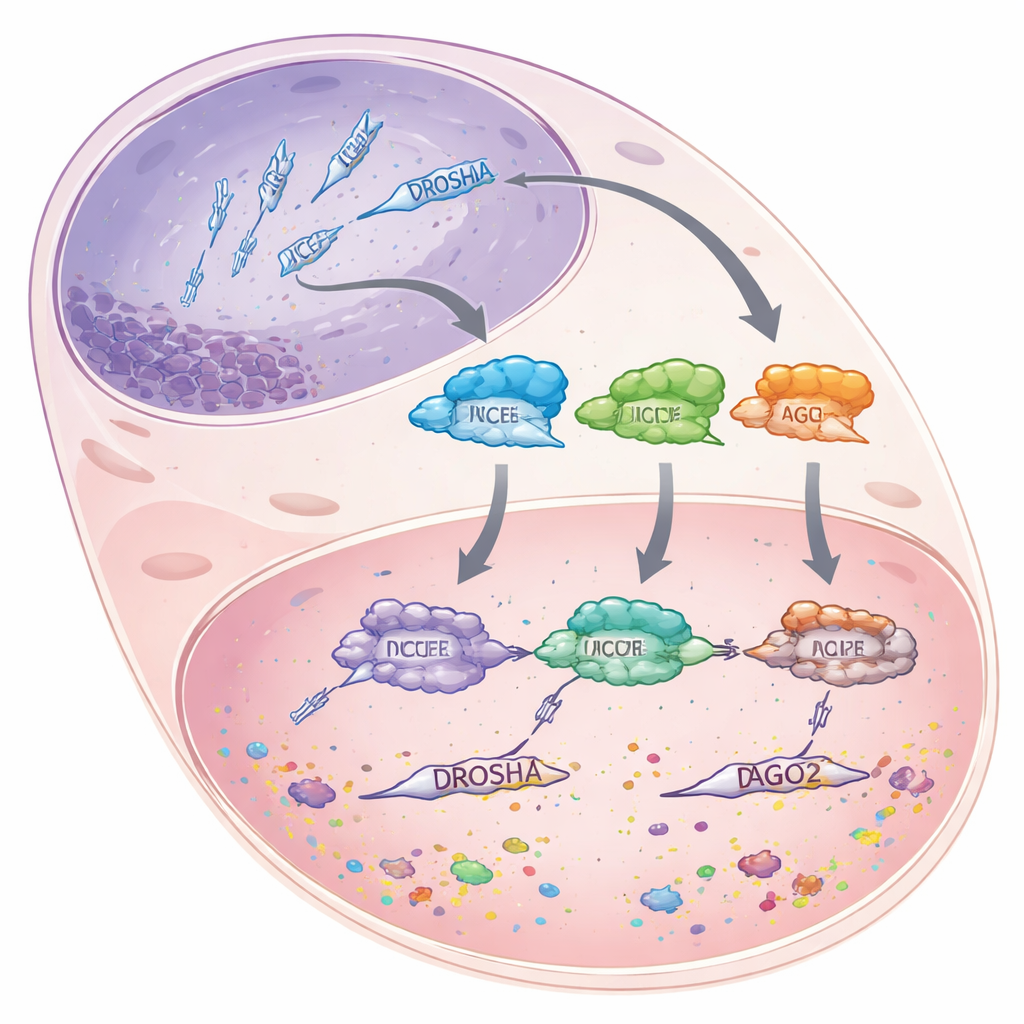
Formas delicadas con funciones precisas
DROSHA, DICER y AGO2 no son simples tijeras; cada una está formada por varias partes que interactúan y deben moverse de forma coreografiada. DROSHA trabaja junto con una proteína compañera, DGCR8, para sujetar los extremos de la horquilla del microARN primario y determinar exactamente dónde cortar. DICER emplea una especie de regla incorporada formada por sus dominios para fijar una distancia constante entre el punto donde sujeta el extremo de la horquilla y donde su centro catalítico realiza el corte. AGO2 envuelve una sola hebra de microARN de modo que su región «seed» quede perfectamente expuesta para reconocer los mensajes diana, mientras iones metálicos y aminoácidos clave en su núcleo se alinean para cortar esos objetivos cuando el apareamiento es suficientemente fuerte. En las tres proteínas, surcos con carga positiva y conectores flexibles guían las hebras de ARN hacia su lugar, mientras que bolsillos de unión a metales y residuos catalíticos llevan a cabo los cortes químicos.
Cuando las tijeras están torcidas o embotadas
Estudios genéticos en pacientes con cáncer, enfermedades de la sangre y síndromes del neurodesarrollo han descubierto cúmulos de mutaciones en estas máquinas de microARN. Muchos de los cambios más dañinos se localizan directamente en centros catalíticos o en superficies de agarre de ARN muy ajustadas. En DROSHA, por ejemplo, sustituciones como E1147K y D1219G se sitúan en el núcleo del sitio de corte y alteran la capacidad de retener iones metálicos esenciales, dejando a la enzima incapaz de procesar los microARN primarios. Otras mutaciones en DROSHA, como truncaciones que eliminan la región de corte o modificaciones que desestabilizan sus hélices de soporte, debilitan todo el complejo y causan caídas globales en los niveles de microARN en el tumor de Wilms, trastornos de la médula ósea y enfermedades del sistema nervioso. En DICER, mutaciones recurrentes se agrupan en uno de sus dos dominios de corte, sesgando la producción de modo que se pierde un brazo del dímero de microARN, lo que desplaza el equilibrio entre señales que promueven o suprimen el crecimiento. 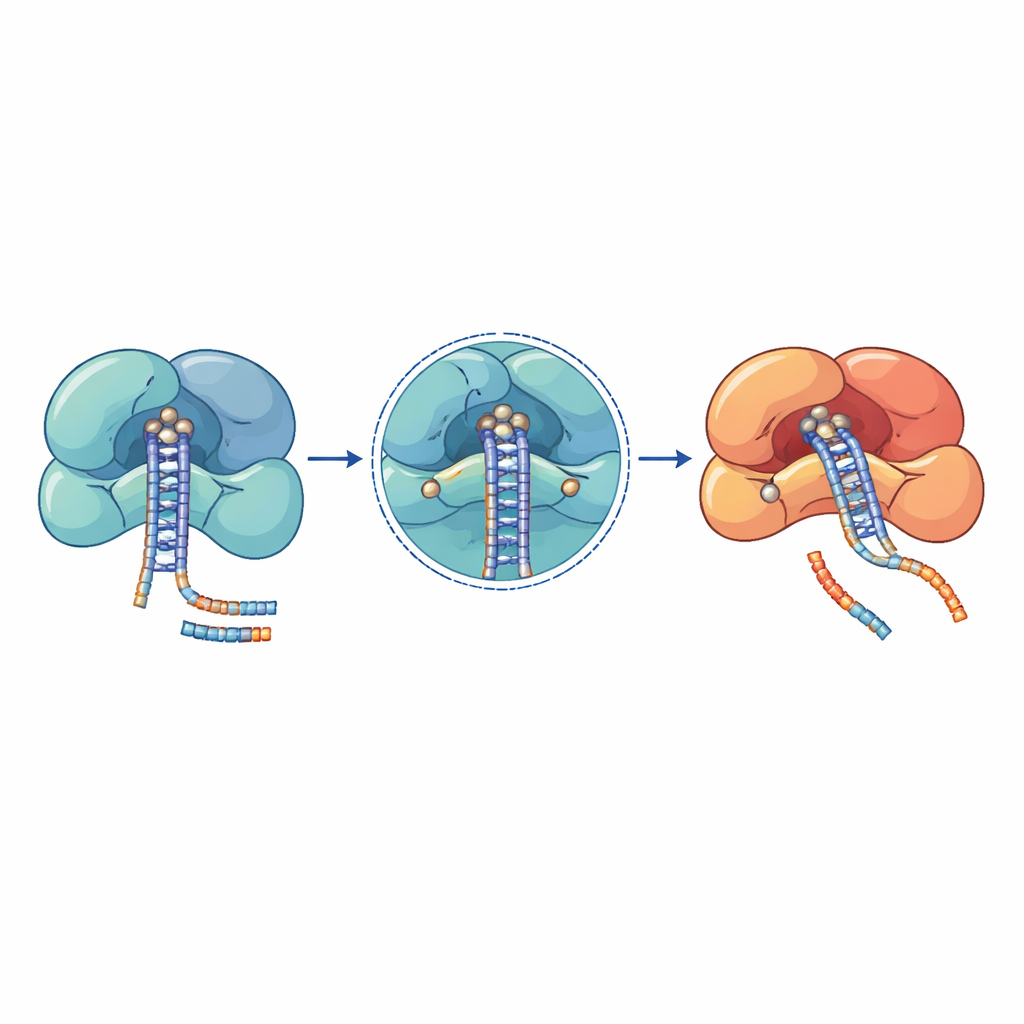
Guías desalineadas en el cerebro y más allá
Las mutaciones en AGO2 cuentan una historia distinta pero relacionada. Golpes directos a su núcleo catalítico son raros, probablemente porque serían letales en etapas tempranas del desarrollo. En su lugar, las variantes asociadas a enfermedad tienden a aparecer en regiones de conectores flexibles y en las uniones de dominio que mantienen la forma de AGO2. En el síndrome de Lessel–Kreienkamp, una condición del neurodesarrollo, mutaciones en estos conectores y superficies circundantes retuercen sutilmente cómo se empaquetan y mueven las partes PAZ, MID y PIWI de AGO2. Esto puede desalinear la microARN guía o debilitar su sujeción a los ARN diana, difuminando la precisión del silenciamiento génico durante el desarrollo cerebral. Cambios estructurales similares en cualquier punto de la vía de microARN —ya sea en DROSHA, DICER o AGO2— pueden propagarse, alterando redes enteras de genes implicados en el crecimiento celular, la formación de la sangre o el cableado neuronal.
Convertir pistas estructurales en tratamientos futuros
Al superponer mutaciones asociadas a enfermedad sobre mapas 3D de alta resolución de estas proteínas, los investigadores pueden clasificar con precisión cómo cada cambio provoca problemas—si es embotando el filo de corte, aflojando contactos críticos con proteínas compañeras o doblando hélices clave fuera de su alineación. Estas ideas estructurales abren la puerta a intervenciones concretas: pequeñas moléculas que estabilizan interfaces debilitadas, ARN diseñados que reorienten enzimas parcialmente funcionales hacia los sustratos correctos, o compuestos alostéricos que empujen a proteínas mutantes hacia conformaciones más activas. Para un lector no especializado, la conclusión es que pequeños ajustes estructurales en las tijeras de ARN de la célula pueden tener efectos desproporcionados en la salud, pero también ofrecen puntos de apoyo precisos para diseñar terapias de nueva generación informadas por la mutación.
Cita: Lee, H., Lee, J. & Roh, SH. Structural insights into disease-associated mutations in the microRNA processing machinery. Exp Mol Med 58, 639–649 (2026). https://doi.org/10.1038/s12276-026-01669-4
Palabras clave: microARN, interferencia por ARN, DROSHA DICER AGO2, genética del cáncer, trastornos del neurodesarrollo