Clear Sky Science · es
Mecanismos reguladores de la estabilidad de la proteína Snail: sistema ubiquitina–proteasoma y autofagia mediada por chaperonas
Por qué la diseminación del cáncer depende de una proteína frágil
El cáncer se vuelve verdaderamente peligroso cuando las células se desprenden del tumor original y viajan a órganos distantes. Esta diseminación, o metástasis, depende en parte de una potente proteína “interruptora maestra” llamada Snail, que ayuda a las células a aflojar sus uniones y volverse más móviles. Este artículo explica cómo nuestras células normalmente mantienen a Snail bajo control al degradarla rápidamente mediante dos grandes sistemas de eliminación de desechos. Comprender este equilibrio ofrece nuevas ideas para ralentizar o prevenir la metástasis.
De células compactas a invasores errantes
En los tejidos sanos, las células epiteliales forman capas ordenadas, como ladrillos, que permanecen en su sitio y se adhieren firmemente a sus vecinas. Para que una célula tumoral escape, a menudo sufre una transformación llamada transición epitelio–mesénquima, o TEM, en la que pierde sus contactos estrechos y adquiere la capacidad de moverse e invadir. Snail es un impulsor clave de esta transformación: cuando está presente en el núcleo celular, apaga genes que mantienen la adhesión entre células y activa genes que favorecen el movimiento y la invasión. Niveles altos de Snail se asocian con cánceres agresivos y peores resultados para los pacientes, por lo que las células han desarrollado formas de mantener a Snail escaso y de vida corta en condiciones normales.
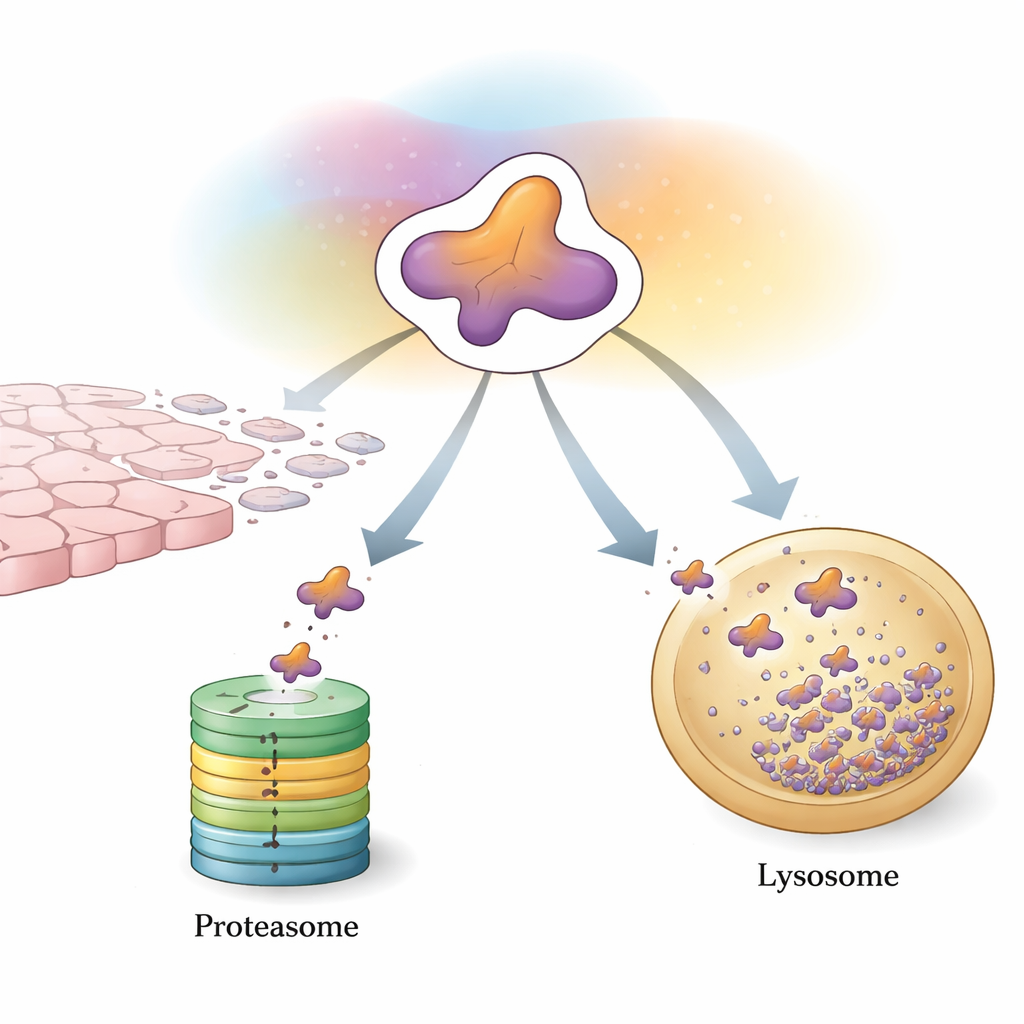
La primera línea de control celular: marcar y triturar
Una forma principal en que las células controlan a Snail es mediante el sistema ubiquitina–proteasoma, una máquina de marcar y triturar proteínas no deseadas. Enzimas especializadas añaden pequeñas “banderas” formadas por una proteína llamada ubiquitina sobre Snail. Cuando suficientes de estas banderas se acumulan en un patrón determinado, Snail se dirige al proteasoma, un complejo en forma de barril que lo descompone en fragmentos. Un amplio elenco de proteínas auxiliares afina este proceso. Algunas enzimas añaden cadenas que promueven la degradación y envían rápidamente a Snail al triturador, ayudando a frenar el crecimiento y la diseminación tumoral. Otras añaden cadenas que estabilizan a Snail o aumentan indirectamente su producción génica, inclinando el equilibrio hacia la TEM y la metástasis. Modificaciones químicas como la fosforilación y la acetilación actúan como interruptores adicionales, controlando qué auxiliares pueden unirse a Snail y si será destruido o perdonado.
Quitar los frenos: enzimas que rescatan a Snail
La historia no termina con marcar a Snail para su destrucción. Otro grupo de enzimas, llamadas desubiquitinadas (deubiquitinilas), pueden arrancar las banderas de ubiquitina, rescatando a Snail del proteasoma. Muchas de estas enzimas se activan o se fortalecen en los cánceres, lo que permite que Snail escape a la degradación y persista en el núcleo. Sus acciones dependen en gran medida del contexto celular: en algunos entornos estabilizan directamente a Snail, mientras que en otros influyen en la localización de Snail dentro de la célula o en cómo interactúa con proteínas asociadas. Señales de vías relacionadas con el cáncer, como factores de crecimiento y respuestas al estrés, alimentan esta red y deciden si Snail será eliminado rápidamente o se le permitirá impulsar el programa de TEM.
Una segunda red de seguridad: entrega selectiva al centro de reciclaje celular
Más allá del proteasoma, las células dependen de la autofagia, un conjunto de vías que transportan proteínas a compartimentos ácidos llamados lisosomas para su degradación. Esta revisión destaca una forma altamente selectiva conocida como autofagia mediada por chaperonas (CMA) como una segunda ruta importante para controlar a Snail. La CMA reconoce una secuencia corta dentro de Snail y, con la ayuda de proteínas escortas, entrega a Snail citoplasmático a los lisosomas para su destrucción. En células de cáncer de mama menos agresivas, este sistema mantiene a Snail mayormente fuera del núcleo y susceptible a la eliminación lisosomal. En cánceres de mama más agresivos y triple negativos, Snail tiende a acumularse en el núcleo y eludir la CMA, fortaleciendo su capacidad para desencadenar la TEM y la metástasis.
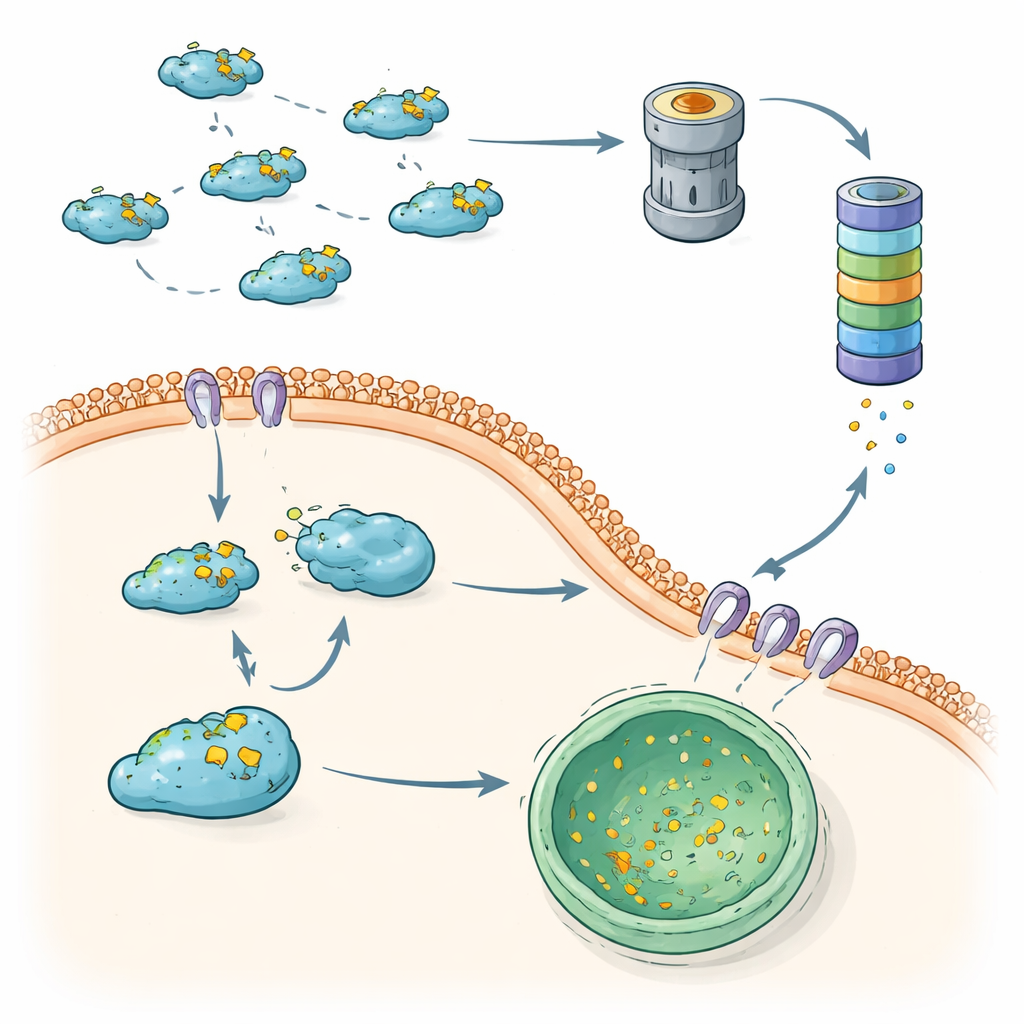
Cuando el control de calidad falla, la metástasis avanza
En conjunto, estos hallazgos revelan que las células usan dos ejes complementarios de “control de calidad” para contener a Snail: la vía ubiquitina–proteasoma y la degradación lisosomal basada en CMA. Cuando ambos funcionan correctamente, Snail se recicla rápidamente, limitando la TEM y ayudando a prevenir la diseminación de las células tumorales. Cuando cualquiera de los ejes se debilita —por cambios en las enzimas de marcado, en las desubiquitinilas o en los componentes de la CMA— Snail se vuelve más estable, se acumula en el núcleo y promueve con fuerza el comportamiento invasivo. Al cartografiar estas rutas interconectadas de degradación, el artículo describe nuevas posibilidades terapéuticas: fármacos que restauren o potencien la degradación de Snail, o que lo dirijan de nuevo hacia la CMA o la destrucción proteasomal, podrían ayudar a volver a aplicar los frenos sobre la metástasis sin cerrar por completo estos sistemas esenciales de reciclaje proteico.
Cita: Kim, M., Hong, KS., Kim, T. et al. Regulatory mechanisms for Snail protein stability: ubiquitin–proteasome system and chaperone-mediated autophagy. Exp Mol Med 58, 408–415 (2026). https://doi.org/10.1038/s12276-026-01667-6
Palabras clave: metástasis del cáncer, transición epitelio–mesénquima, proteína Snail, degradación proteica, autofagia