Clear Sky Science · es
Fallo del eje metabólico eritropoyesis–inosina subyacente a la neurodegeneración retiniana en el glaucoma: nuevos diagnósticos y terapias
Por qué esto importa para la visión y la salud
El glaucoma suele describirse como un problema de presión dentro del ojo que roba la vista lentamente. Este estudio sostiene que la historia comienza mucho antes y lejos del globo ocular: en la médula ósea y en nuestros glóbulos rojos. Los autores muestran que una falla en cómo producimos y alimentamos los glóbulos rojos deja a la retina sin suficiente oxígeno y energía, pero además revela una sorprendente molécula ayudante—la inosina—que podría tanto diagnosticar como tratar el glaucoma.
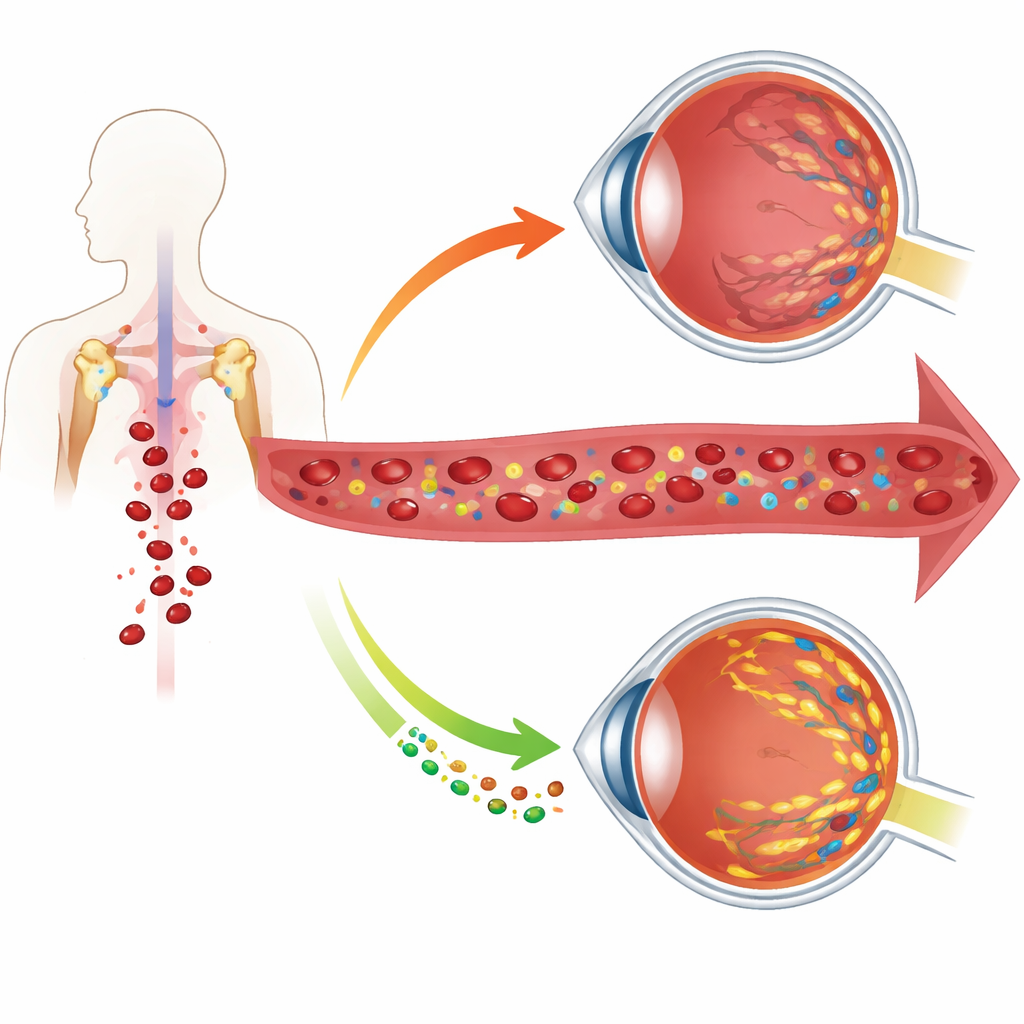
Cuando la enfermedad ocular empieza en la sangre
Usando datos de más de 127.000 personas del UK Biobank y una cohorte hospitalaria independiente, los investigadores hallaron que las personas con glaucoma presentan de manera consistente menos glóbulos rojos, hemoglobina más baja y menor volumen corpuscular total. Estos cambios se observaron en las dos principales formas clínicas de glaucoma y se asociaron con mayor presión intraocular, capas nerviosas retinianas más delgadas y campos visuales peores. En otras palabras, los pacientes con glaucoma tienden a tener un déficit leve pero relevante en las propias células que transportan oxígeno por todo el cuerpo, incluido el ojo.
Glóbulos rojos bajo estrés metabólico
Los glóbulos rojos en el glaucoma no solo eran menos numerosos: estaban bioquímicamente agotados. Un perfil químico detallado mostró que su combustible habitual, la glucosa, no se utilizaba de forma eficiente. Las células llevaban más glucosa fuera que dentro, su principal transportador de azúcar en la membrana estaba reducido y las vías energéticas clave funcionaban a bajo rendimiento. Al mismo tiempo, estas células presentaban mayor estrés oxidativo y reservas reducidas de moléculas energéticas como el ATP. Como medida paliativa, cambiaron a quemar otra molécula pequeña, la inosina, para generar intermedios que facilitan la liberación de oxígeno por la hemoglobina. Este cambio de emergencia, impulsado por una enzima sensor de energía llamada AMPK, mejora temporalmente la entrega de oxígeno pero agota progresivamente las reservas sistémicas de inosina.
De la falla de la médula ósea al daño retiniano
Puesto que los glóbulos rojos constituyen la mayoría de las células de nuestro cuerpo, su mayor demanda de inosina tiene consecuencias en otros tejidos. Experimentos en ratones en los que se eliminó genéticamente el principal transportador de inosina en los glóbulos rojos (ENT1) mostraron que estos animales desarrollaron glaucoma relacionado con la edad: su presión ocular aumentó, sus células ganglionares retinianas murieron y sus glóbulos rojos liberaron oxígeno deficientemente mientras generaban más especies reactivas de oxígeno. Estudios de médula ósea revelaron que la falta de señalización por inosina en los precursores sanguíneos tempranos impedía la producción de nuevos glóbulos rojos, forzando al bazo a asumir funciones de emergencia hematopoyéticas. En conjunto, estos hallazgos respaldan una cadena de eventos en la que una eritropoyesis defectuosa y glóbulos rojos maladaptados crean una escasez crónica de oxígeno que acaba dañando la retina.
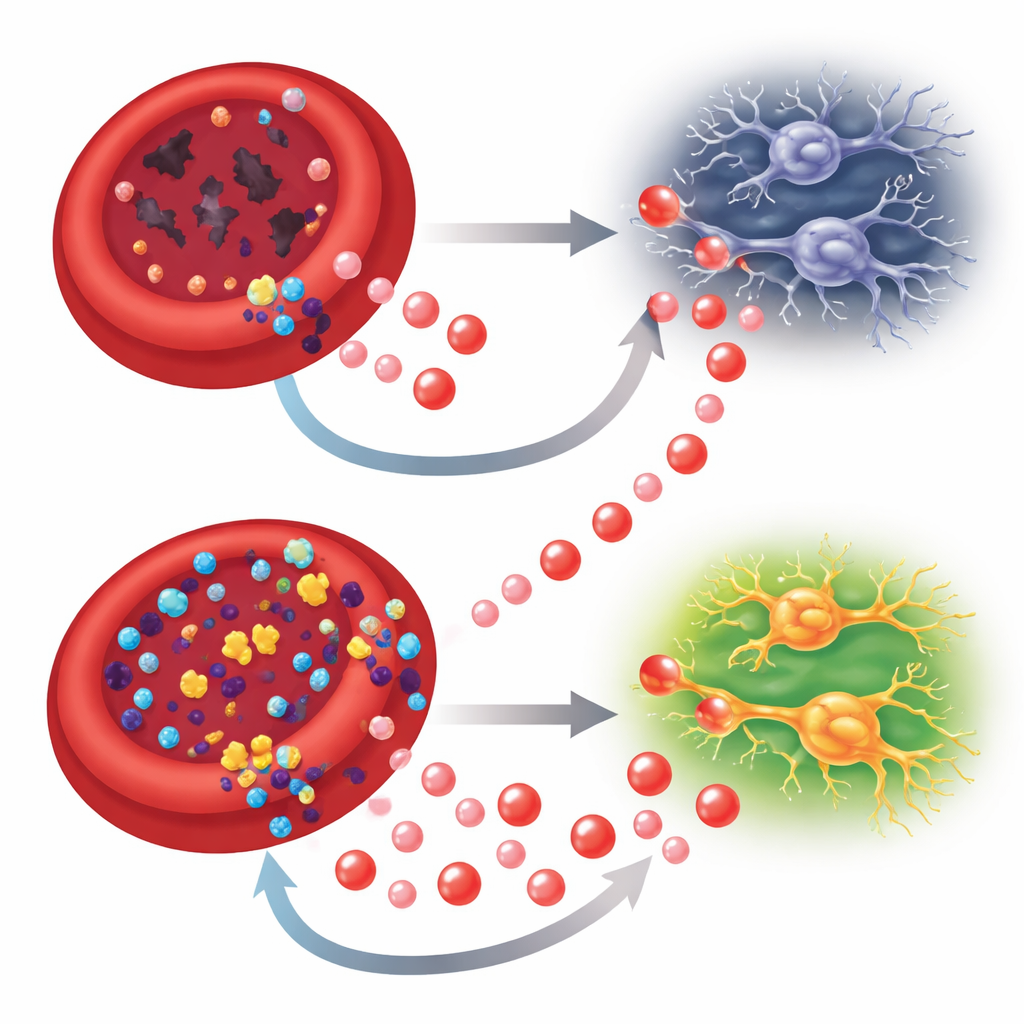
La inosina como línea de vida metabólica
El equipo preguntó entonces si suministrar inosina adicional podría romper este círculo vicioso. En un modelo de ratón de glaucoma inducido por un aumento transitorio de la presión ocular, inyecciones diarias de inosina mejoraron la capacidad de los glóbulos rojos para liberar oxígeno, redujeron el estrés oxidativo y restauraron los recuentos de glóbulos rojos y los niveles de hemoglobina—sin acortar la vida útil de las células rojas. En la médula ósea, la inosina impulsó a las células madre y progenitoras hacia la línea de los glóbulos rojos y normalizó las etapas tardías de maduración de estas células. Al mismo tiempo, los ratones tratados mostraron mejor oxigenación retiniana, capas nerviosas más gruesas, más células ganglionares retinianas supervivientes y medidas eléctricas y conductuales de la visión más fuertes. En neuronas retinianas cultivadas expuestas a baja oxigenación y ausencia de glucosa, la propia inosina sirvió como combustible de reserva, entrando en varias vías energéticas, aumentando los niveles de ATP y reduciendo el daño oxidativo.
Nuevas formas de detectar y tratar el glaucoma
Al unir datos humanos a gran escala con experimentos animales y celulares detallados, este trabajo replantea el glaucoma como un trastorno metabólico sistémico sangre–retina más que como una enfermedad ocular puramente local. Una firma de diez metabolitos en los glóbulos rojos, centrada en la inosina y sus productos de degradación, discriminó a los pacientes con glaucoma de los sujetos sanos con una precisión comparable a las pruebas oculares estándar, lo que sugiere un futuro papel para el cribado basado en sangre. Al mismo tiempo, la inosina emerge como un factor de rescate multipropósito: apoya la producción de glóbulos rojos, mejora su entrega de oxígeno y alimenta directamente a las neuronas retinianas estresadas. Si bien serán necesarios ensayos clínicos para evaluar seguridad y eficacia en humanos, el estudio señala al metabolismo de la inosina como un prometedor nuevo objetivo para diagnosticar y frenar la neurodegeneración impulsada por hipoxia en el glaucoma.
Cita: Chou, Y., Liu, W., Li, Y. et al. Erythropoiesis–inosine metabolic axis failure underlying retinal neurodegeneration in glaucoma: novel diagnoses and therapies. Exp Mol Med 58, 562–578 (2026). https://doi.org/10.1038/s12276-026-01654-x
Palabras clave: glaucoma, glóbulos rojos, células ganglionares retinianas, metabolismo de la inosina, hipoxia ocular