Clear Sky Science · es
Un circuito neuroinflamatorio cornea–trigémino dependiente del receptor transitorio potencial vaniloide 1 promueve la neuropatía corneal
Ojos sensibles y dolor persistente
Muchas personas con ojos secos e irritados se sorprenden al descubrir que sus síntomas más graves no provienen tanto de la superficie ocular, sino de los nervios que detectan la irritación y el dolor. Este estudio en ratones revela un bucle de retroalimentación oculto entre el ojo y el centro sensorial del cerebro que ayuda a explicar por qué el dolor ocular puede volverse persistente y por qué a veces afecta a ambos ojos aunque solo uno parezca seco. Al identificar un regulador molecular específico en este circuito, el trabajo apunta a nuevas formas de calmar ojos dolorosos sin limitarse a añadir más lágrimas.

Cuando el sistema de alarma del ojo falla
La ventana frontal transparente del ojo, la córnea, está densamente poblada de terminaciones nerviosas que vigilan continuamente la humedad, la temperatura y la composición química de las lágrimas. En la enfermedad del ojo seco, las lágrimas se reducen o se vuelven demasiado salinas, y los pacientes con frecuencia desarrollan ardor, escozor o incluso dolor incapacitante. Los autores se centraron en un sensor molecular de las fibras de dolor corneales llamado TRPV1, conocido por ser el receptor del compuesto picante de los chiles, la capsaicina. Este sensor responde al calor y a señales liberadas durante el estrés tisular. El equipo preguntó si la sobreactivación de TRPV1 por la sequedad y el daño podría provocar no solo irritación local, sino también cambios más profundos en los nervios que conectan el ojo con el cerebro.
Un circuito nervio–inmunidad que enlaza ojo y cerebro
Empleando modelos de ratón en los que la producción de lágrimas se reduce quirúrgicamente, los investigadores demostraron que el ojo seco activa intensamente las fibras nerviosas corneales que expresan TRPV1. Esto, a su vez, altera la actividad génica y el comportamiento inmunitario en el ganglio trigémino, un cúmulo nervioso que alberga los somas de las neuronas sensoriales corneales. En ratones normales, la sequedad provocó un aumento de genes inflamatorios y relacionados con la inmunidad allí y modificó el estado de macrófagos cercanos, células inmunitarias que envuelven a las neuronas sensoriales. Al mismo tiempo, los ojos secos mostraron células inmunitarias activadas en la superficie, reducción de la densidad nerviosa y sensibilidad anómala: la córnea se volvió menos sensible al tacto mecánico y a algunos estímulos químicos, pero más reactiva a la estimulación de TRPV1, lo que sugiere que este sensor en particular se había sensibilizado.
Cómo un ojo afectado puede influir en el otro
Para separar los efectos directos de la sequedad de las señales nerviosas más remotas, el equipo creó un «ojo seco unilateral» extirpando una glándula lagrimal solo del lado derecho. De forma llamativa, el ojo izquierdo sin tratar permaneció normalmente húmedo y conservó una barrera superficial saludable, sin embargo, con el tiempo desarrolló una inflamación sutil y signos claros de disfunción nerviosa: adelgazamiento de fibras nerviosas profundas y alteración de la sensibilidad, reflejando pero con retraso lo observado en el lado dañado. Estos cambios contralaterales dependieron de TRPV1: los ratones genéticamente carentes de este sensor estuvieron protegidos en ambos ojos, el seco y el intacto. El secuenciado de ARN del ganglio trigémino confirmó que la sequedad unilateral desencadenó también una firma inmune e inflamatoria en el lado opuesto, lo que apunta a un circuito córnea–trigémino–córnea capaz de propagar problemas de un ojo al otro.
Demostrando que TRPV1 basta para causar daño
La sequedad es compleja y activa muchas vías, por lo que los autores preguntaron a continuación si TRPV1 por sí solo podría poner en marcha este circuito. Aplicaron capsaicina tópicamente en la córnea de un ojo, estimulando TRPV1 sin resecar la superficie. El ojo tratado mostró una marcada degeneración de los nervios corneales y sensibilidad reducida, aunque la barrera epitelial permaneció intacta. De manera notable, el ojo no tratado volvió a presentar pérdida más leve pero mensurable de terminaciones nerviosas y cambios en la sensibilidad, lo que confirma que una activación intensa de TRPV1 en una córnea basta para provocar lesión nerviosa y alteraciones funcionales en el ojo compañero a través de la red trigémina compartida. Los ratones carentes de linfocitos T y B solo desarrollaron cambios en el ojo tratado, lo que sugiere que la propagación bilateral completa requiere una respuesta inmune adaptativa además de la activación nerviosa.
Un mensajero que potencia el dolor y una posible vía terapéutica
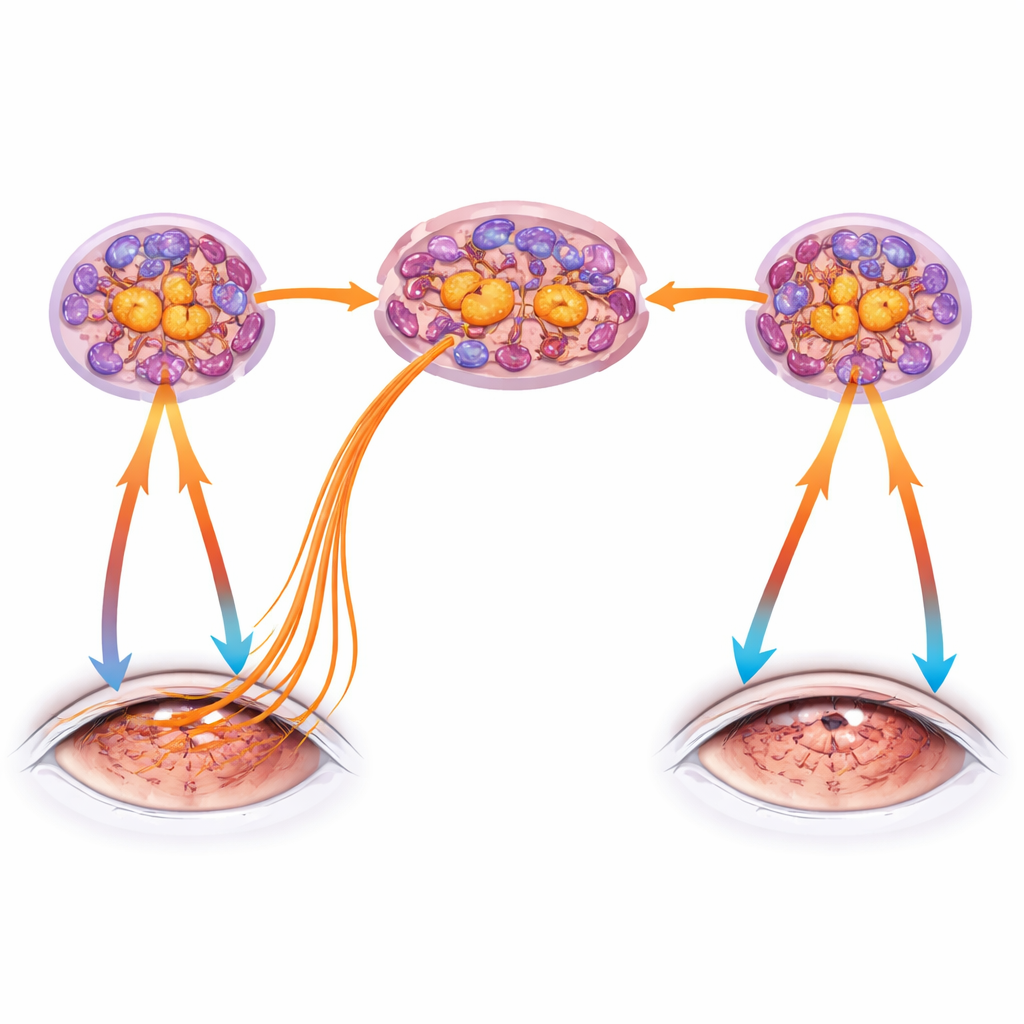
El estudio también examinó la sustancia P, un neuropéptido liberado por las fibras de dolor estimuladas que puede inflam ar aún más los tejidos y potenciar la actividad de TRPV1. Bloquear los receptores de la sustancia P con colirios en el ojo no seco de ratones con ojo seco unilateral no dañó la superficie corneal, pero mitigó significativamente la pérdida de sensibilidad al tacto y la respuesta aumentada a la estimulación de TRPV1. Sin embargo, no impidió por completo la pérdida estructural de terminaciones nerviosas, lo que subraya que varios factores colaboran para dañar los nervios corneales. En conjunto, los hallazgos describen un círculo vicioso: la sequedad y la lesión activan TRPV1 en los nervios corneales, que envían señales de peligro al ganglio trigémino, reclutan y reprograman células inmunitarias allí, y luego retroalimentan señales nerviosas proinflamatorias y liberación de neuropéptidos a la superficie ocular, agravando la degeneración nerviosa y propagando la disfunción entre los ojos.
Qué significa esto para las personas con ojos secos y dolorosos
Para los no especialistas, el mensaje clave es que la enfermedad del ojo seco no es solo un problema local de falta de lágrimas. Implica un bucle nervio–inmunidad autorreforzante que conecta la superficie ocular con centros sensoriales en la cabeza y de vuelta. TRPV1 se sitúa en el punto de entrada de este bucle, actuando como una alarma hipersensible que, una vez desencadenada, ayuda a mantener la inflamación y el daño nervioso incluso si la sequedad original es leve o unilateral. Por tanto, las terapias que reduzcan la actividad de TRPV1 en los nervios corneales, o que interrumpan mensajeros posteriores como la sustancia P, podrían hacer más que calmar una superficie seca: podrían romper un circuito profundo del dolor y proteger la compleja red nerviosa que mantiene nuestros ojos confortables y sensibles.
Cita: Pizzano, M., Vereertbrugghen, A., Martinez Gomez, M.J. et al. A transient receptor potential vanilloid 1-dependent corneal–trigeminal neuroinflammatory circuit promotes corneal neuropathy. Exp Mol Med 58, 605–621 (2026). https://doi.org/10.1038/s12276-026-01653-y
Palabras clave: enfermedad del ojo seco, nervios corneales, TRPV1, neuroinflamación, sustancia P