Clear Sky Science · es
Intercambio metabólico entre fibroblastos asociados al cáncer, adipocitos y células inmunitarias como motor de un microambiente tumoral inmunosupresor
Por qué importa el vecindario del tumor
El cáncer no crece en aislamiento. Vive en un vecindario concurrido de células de soporte, células grasas y células inmunitarias que intercambian constantemente nutrientes y señales químicas. Este artículo explica cómo el “metabolismo” de ese vecindario —la forma en que las células usan y comparten combustible— inclina silenciosamente la balanza a favor del tumor y en perjuicio del sistema inmunitario. Comprender esta economía oculta de azúcares, grasas y aminoácidos está abriendo nuevas vías para mejorar las inmunoterapias y cortar el sistema de apoyo del tumor.
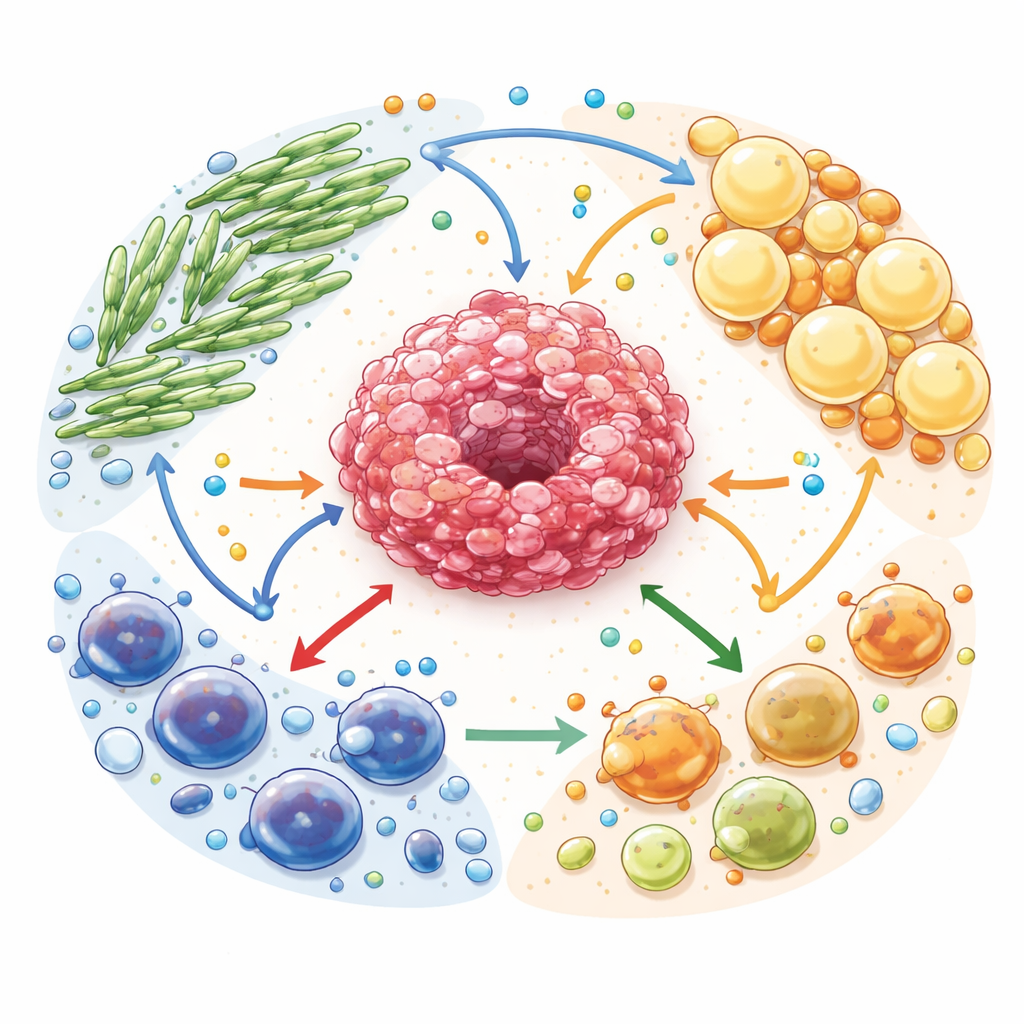
Compartir combustible en un ecosistema tumoral
Los autores describen el microambiente tumoral como un ecosistema complejo. Las células cancerosas están rodeadas por fibroblastos asociados al cáncer (células de soporte similares a cicatrices), adipocitos asociados al cáncer (células grasas reprogramadas) y muchos tipos de células inmunitarias. Todas estas células compiten y se intercambian combustibles como glucosa, ácidos grasos y aminoácidos. Pero este intercambio no es neutral: las células de soporte se reconfiguran para descomponer sus propias reservas y exportar moléculas ricas en energía que alimentan a las células tumorales. Al mismo tiempo, subproductos tipo desecho, incluidos el lactato y la adenosina, se acumulan y actúan como potentes señales que debilitan a las células inmunitarias protectoras mientras favorecen a las que atenúan el ataque inmunitario.
Cómo las células grasas ayudan a los tumores y dificultan las defensas
Las reservas de grasa cercanas hacen mucho más que almacenar calorías. Bajo la influencia de señales tumorales y de la baja disponibilidad de oxígeno, los adipocitos ordinarios se transforman en adipocitos asociados al cáncer. Reducen sus gotas de grasa, aumentan la lipólisis y vierten ácidos grasos libres, moléculas inflamatorias y pequeñas vesículas cargadas de contenido. Las células cancerosas importan vorazmente estos lípidos y los queman en sus mitocondrias, obteniendo una fuente de energía flexible y duradera que les ayuda a sobrevivir al estrés, diseminarse y resistir tratamientos. Las células inmunitarias en regiones ricas en grasa no salen bien paradas: las células T citotóxicas y las células NK se sobrecargan de lípidos, sufren estrés oxidativo y entran en un estado de “agotamiento” con una capacidad reducida para destruir células tumorales. En contraste, las células T reguladoras y ciertos tipos de células mieloides prosperan con estos lípidos, volviéndose más supresoras y ahogando aún más las respuestas inmunitarias.
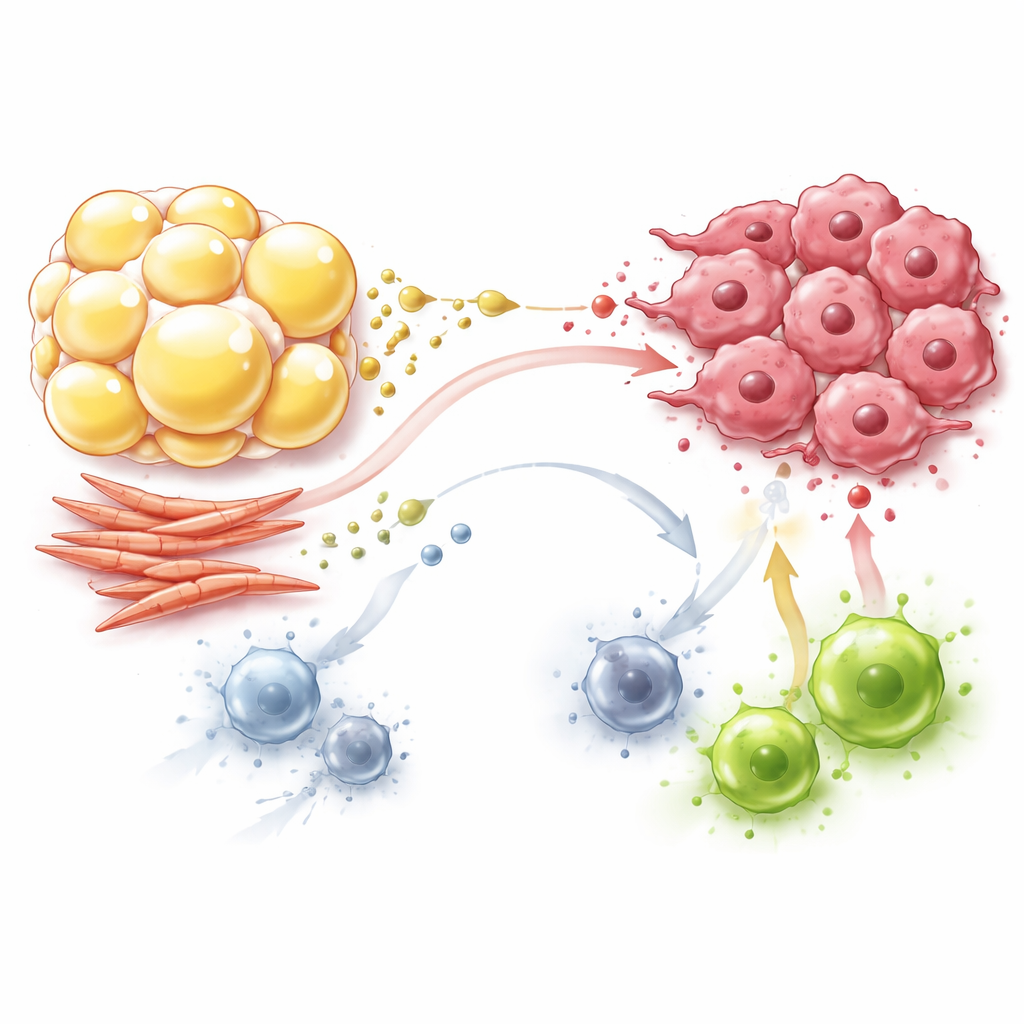
Fibroblastos: constructores que también reprograman el metabolismo
Los fibroblastos, conocidos desde hace tiempo como los constructores del tejido similar a cicatriz alrededor de los tumores, también son actores activos en este drama metabólico. Los fibroblastos asociados al cáncer se orientan hacia un comportamiento que consume azúcar, convirtiendo grandes cantidades de glucosa en lactato y piruvato incluso cuando hay oxígeno disponible. Exportan estos productos al espacio circundante, donde las células tumorales los reutilizan como combustible para sus propias centrales energéticas, reservando glucosa para el crecimiento. Los fibroblastos también fabrican e intercambian aminoácidos como glutamina, prolina y asparagina, que sostienen tanto la estructura del tumor como su crecimiento bajo estrés nutricional. Al mismo tiempo, los fibroblastos consumen nutrientes clave y liberan lactato, desplazando a las células T efectoras que dependen de la glucosa y empujando a macrófagos y células T hacia estados más tolerantes y menos agresivos.
Células inmunitarias atrapadas en una trampa metabólica
El sistema inmunitario dentro de los tumores está determinado tanto por la disponibilidad de combustible como por los antígenos. Las células T citotóxicas y las células NK, que necesitan una quema rápida de azúcares para impulsar su ataque, se encuentran en un entorno despojado de glucosa y anegado de lactato, lípidos y otros metabolitos supresores. Sus motores se paralizan, sus mitocondrias se dañan y aumentan los “frenos” inhibitorios en su superficie. Mientras tanto, las células T reguladoras y los macrófagos asociados al tumor están bien adaptados a este entorno hostil. Prefieren la oxidación de grasas y el metabolismo oxidativo, lo que les permite prosperar donde otros fracasan. Apoyadas por fibroblastos y adipocitos, estas células refuerzan un estado tolerante similar a la curación de heridas que protege al tumor y reduce el impacto de los inhibidores de puntos de control y otras inmunoterapias.
Convertir el metabolismo en un objetivo terapéutico
La revisión destaca una caja de herramientas experimental en expansión diseñada para interrumpir esta red de apoyo sin limitarse a envenenar células en división. Algunos enfoques buscan bloquear la liberación de grasas de los adipocitos o la captación y oxidación de lípidos en las células tumorales. Otros apuntan a vías impulsadas por fibroblastos que generan lactato, remodelan la matriz o atraen células mieloides supresoras. Al reducir los niveles de lactato, bloquear transportadores específicos de combustible o reprogramar los sensores lipídicos dentro de las células, estas estrategias intentan restaurar el acceso a la glucosa y la salud mitocondrial en las células T y NK agotadas. El objetivo final no es solo privar de alimento al tumor, sino “reeducar” su vecindario para que las células inmunitarias vuelvan a ver, alcanzar y atacar eficazmente a las células cancerosas.
Cita: Kim, T.H., Lim, S.H., Lee, H. et al. Metabolic crosstalk among cancer-associated fibroblasts, adipocytes and immune cells as an immunosuppressive tumor microenvironment driver. Exp Mol Med 58, 366–381 (2026). https://doi.org/10.1038/s12276-026-01650-1
Palabras clave: microambiente tumoral, metabolismo del cáncer, fibroblastos asociados al cáncer, adipocitos asociados al cáncer, inmunosupresión tumoral