Clear Sky Science · es
La deficiencia del componente del complejo exocisto Exoc5 agrava la progresión de la fibrosis renal
Por qué importa la cicatrización renal
La enfermedad renal crónica afecta a cientos de millones de personas en todo el mundo, y una de las razones principales por las que progresa es la fibrosis: tejido cicatricial que reemplaza de forma paulatina al tejido renal funcional. Este estudio explora una maquinaria celular menos conocida, el exocisto, y una de sus piezas llamada Exoc5, para plantear una pregunta práctica: ¿ayuda esta proteína a que los riñones sanen adecuadamente tras una lesión, o los empuja hacia la cicatrización y el fallo?
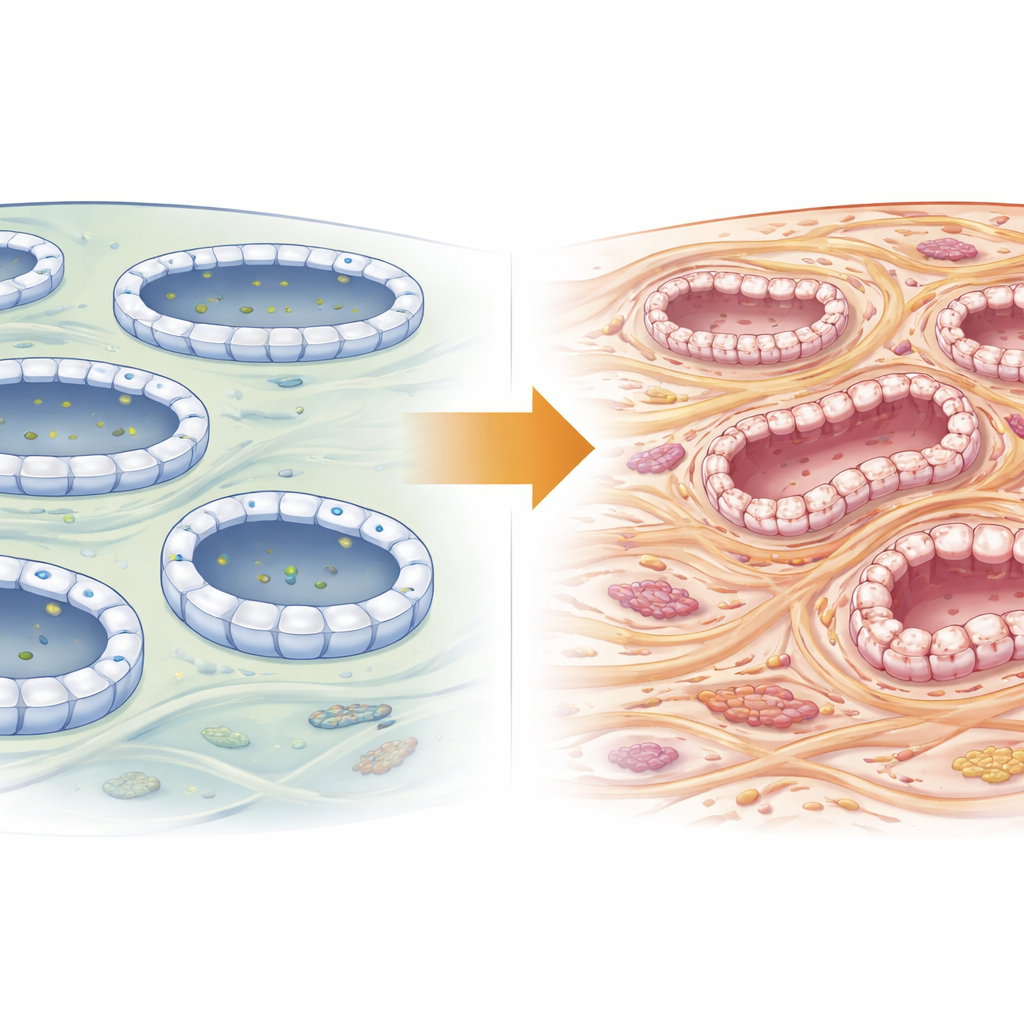
Un centro de envíos celular en las células tubulares
Cada célula de los túbulos renales es un centro logístico muy activo, moviendo constantemente pequeñas burbujas cargadas de material a puntos concretos de su superficie. Este tráfico lo organiza el exocisto, un complejo de anclaje formado por ocho subunidades. Exoc5 se sitúa en el centro de esta maquinaria, conectando la carga que llega desde el interior de la célula con el sitio de acoplamiento en la membrana externa. Trabajos anteriores mostraron que alterar Exoc5 daña varios órganos y que contribuye a que las células de los túbulos renales mantengan su estructura apretada y ordenada. Dado que la pérdida de esa estructura es una característica de la fibrosis, los autores sospecharon que Exoc5 podría determinar silenciosamente si los riñones dañados se recuperan o se cicatrizan.
Evaluando el papel de Exoc5 en riñones de ratón
Los investigadores diseñaron ratones cuyo Exoc5 se eliminó únicamente en las células del túbulo proximal —los segmentos que realizan la mayor parte de la filtración y la reabsorción renal. Sorprendentemente, estos ratones crecieron con normalidad y presentaron una estructura renal, localización de transportadores y función normales en condiciones cotidianas. Para simular una lesión intensa y localizada que con frecuencia conduce a cicatrización, el equipo ligó un uréter, un procedimiento estándar que provoca acumulación de presión, inflamación y fibrosis en el riñón afectado durante una semana. En ratones normales y en los deficientes en Exoc5, esta obstrucción redujo los niveles de Exoc5, pero los animales knockout desarrollaron una atrofia tubular mucho más severa, acumulación de colágeno e invasión por células relacionadas con la inflamación.
De túbulos ordenados a células errantes
Las células tubulares sanas están fuertemente conectadas, con superficies bien definidas en su cara apical y basal. Durante la fibrosis a menudo sufren una “transición epitelio-mesenquimal” (TEM), un cambio de un estado anclado y en lámina a otro más móvil y fibroso. Los autores hallaron que tras la obstrucción, los riñones sin Exoc5 mostraron una activación más intensa de impulsores clave de la TEM y niveles más altos de proteínas típicas de células migratorias y productoras de fibra, junto con una mayor pérdida de proteínas de unión que normalmente mantienen la polaridad de las células tubulares. También observaron la reaparición de Pax2, un regulador del desarrollo que normalmente se apaga cuando los túbulos renales maduran. Pax2 reapareció con mayor intensidad en los túbulos deficientes en Exoc5, particularmente en células estresadas que no se estaban dividiendo con éxito, lo que sugiere que la pérdida de Exoc5 empuja a las células hacia un estado medio reparado y desdiferenciado propenso a la fibrosis.
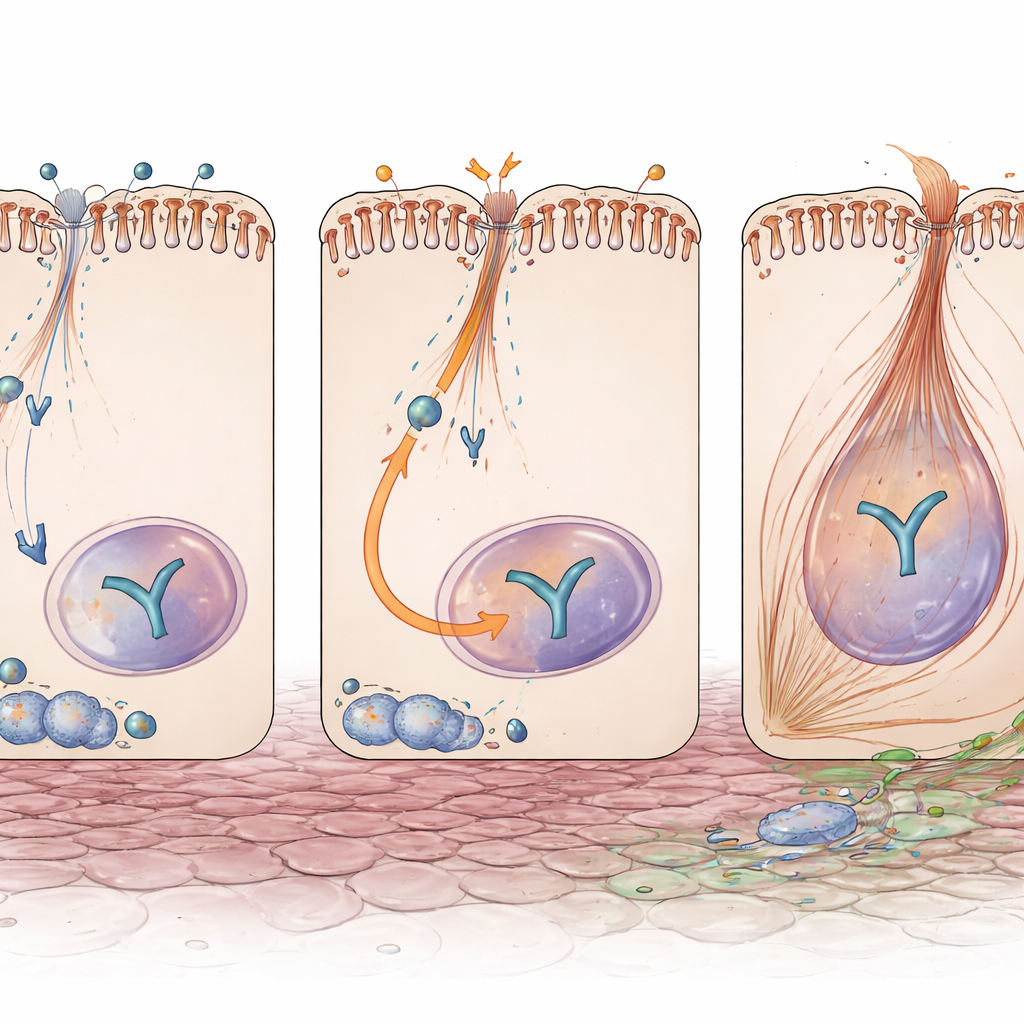
Un interruptor que vincula la lesión con las señales de cicatrización
Otro actor central en la fibrosis es YAP, una proteína sensible a señales que se desplaza al núcleo para activar genes implicados en el crecimiento y la producción de matriz. Incluso sin lesión, los túbulos carentes de Exoc5 presentaban niveles proteicos de YAP más altos. Tras la obstrucción, YAP se activó con mayor intensidad y se concentró en los núcleos celulares de estos riñones, y sus productos aguas abajo—moléculas conocidas por impulsar el remodelado fibrótico—aumentaron. Es importante destacar que esto no se debía a un incremento de la actividad génica de YAP, lo que implica que Exoc5 normalmente restringe a YAP a nivel de la proteína o del tráfico intracelular. En células tubulares renales humanas en cultivo, reducir EXOC5 mediante interferencia de ARN aumentó YAP y Pax2, y potenció la respuesta celular a la señal fibrosis TGF-β, con cambios más marcados tipo TEM y más células adquiriendo fibras contráctiles típicas de miofibroblastos.
Qué implica esto para futuros tratamientos
En conjunto, los hallazgos presentan a Exoc5 como un guardián silencioso: bajo estrés, ayuda a que las células tubulares mantengan su identidad organizada y mantiene bajo control señales pro-cicatrización como YAP y Pax2. Cuando los niveles de Exoc5 caen —ya sea por pérdida genética o por lesión— las células tubulares pierden con mayor facilidad su polaridad, entran en un estado parecido al del desarrollo y alimentan el proceso fibrótico. Dado que eliminar Exoc5 en los túbulos proximales no dañó los riñones sanos pero sí empeoró claramente la cicatrización tras la lesión, este trabajo señala a Exoc5 y sus asociados de señalización como objetivos prometedores para terapias destinadas a frenar o revertir la fibrosis renal antes de que progrese hasta la insuficiencia renal.
Cita: Lim, H.J., Han, Y.K., Noh, M.R. et al. Deficiency of exocyst complex component Exoc5 exacerbates the progression of kidney fibrosis. Exp Mol Med 58, 681–695 (2026). https://doi.org/10.1038/s12276-026-01649-8
Palabras clave: fibrosis renal, Exoc5, transición epitelio-mesenquimal, señalización YAP, enfermedad renal crónica