Clear Sky Science · es
La suplementación con L‑aspártico corrige MASLD y MASH en ratones al inhibir la fragmentación mitocondrial mediada por la interacción plaqueta‑hepatocito a través del eje ATP–P2X7–NEK7–DRP1
Por qué importa este estudio sobre el hígado
Muchísimas personas acumulan grasa extra en el hígado sin saberlo. Este problema silencioso, hoy denominado enfermedad hepática esteatósica asociada a disfunción metabólica (MASLD), puede progresar hacia una inflamación grave, formación de cicatriz y hasta cáncer de hígado. El artículo resumido aquí explora si un aminoácido natural sencillo, el L‑aspártico, puede proteger el hígado en ratones y revela a un culpable inesperado del daño hepático: plaquetas sanguíneas hiperactivas que lesionan las “centrales energéticas” de las células hepáticas, las mitocondrias.
Un problema hepático común en la vida moderna
La MASLD está estrechamente ligada a la obesidad y a la diabetes tipo 2 y pronto podría afectar a más de un tercio de la población mundial. En la MASLD, las células hepáticas se llenan de grasa, se estresan y empiezan a morir, lo que desencadena inflamación y formación de cicatriz. Las mitocondrias sanas normalmente queman grasas y azúcares para obtener energía, pero en esta enfermedad se dañan y fragmentan, de modo que el hígado quema menos grasa y acumula más. A pesar de la magnitud del problema, hasta ahora solo se ha aprobado un fármaco y ayuda solo a una fracción de los pacientes, por lo que los investigadores buscan tratamientos seguros y asequibles que restauren la maquinaria energética hepática.
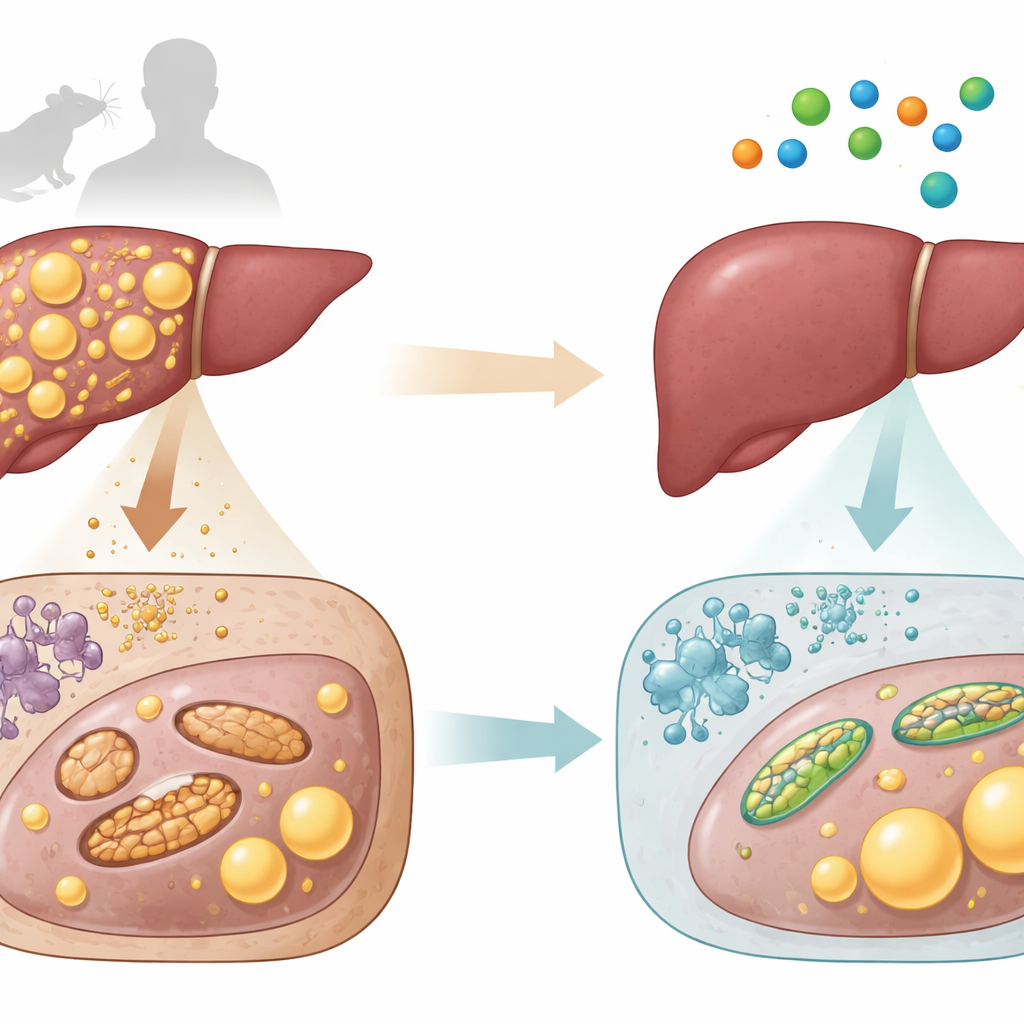
Un aminoácido sencillo como posible aliado
El L‑aspártico es un pequeño bloque formador de proteínas que también participa en los ciclos energéticos del organismo y ya se emplea clínicamente como compuesto de soporte hepático. Los investigadores midieron primero L‑aspártico en muestras de sangre e hígado de ratones y de personas. Encontraron que los animales y los pacientes humanos con hígados más grasos y dañados tenían niveles consistentemente más bajos de L‑aspártico en el tejido hepático. En ambas especies, cuanto menos L‑aspártico había, mayor era el contenido graso y más intensas las señales de lesión hepática. Este patrón sugiere que la caída de L‑aspártico podría ir de la mano con el empeoramiento de la salud hepática.
Revirtiendo la esteatosis y la inflamación en ratones
El equipo se preguntó entonces si volver a suministrar L‑aspártico podría reparar la enfermedad. Alimentaron a ratones con una dieta alta en grasas y colesterol o con una dieta especial que provoca inflamación y cicatrización hepática severas, reproduciendo la MASLD humana y su forma avanzada, MASH. Cuando estos ratones recibieron inyecciones de L‑aspártico a dosis comparables a las usadas en clínica, sus hígados se volvieron más claros y menos grasos, las enzimas hepáticas en sangre disminuyeron y los exámenes microscópicos mostraron menos gotas de grasa, menos inflamación y menor fibrosis. Estos beneficios aparecieron tanto en la esteatosis temprana como en la enfermedad inflamatoria avanzada y fueron comparables a los de fármacos de referencia establecidos en los mismos modelos.
Protegiendo las centrales energéticas de la célula
Al mirar en el interior del hígado, los científicos observaron que los ratones enfermos tenían menos mitocondrias, muchas de ellas agrandadas y dañadas o fragmentadas en trozos diminutos. El tratamiento con L‑aspártico restauró una red mitocondrial más saludable y alargada. Aumentó la actividad de complejos enzimáticos clave productores de energía, elevó el uso de oxígeno mitocondrial y la producción de ATP, e incrementó marcadores de “limpieza” y renovación mitocondrial. Mediciones a nivel del animal entero mostraron mayor consumo de oxígeno y gasto energético, lo que indica que los ratones estaban quemando más combustible en general y no simplemente comiendo menos.
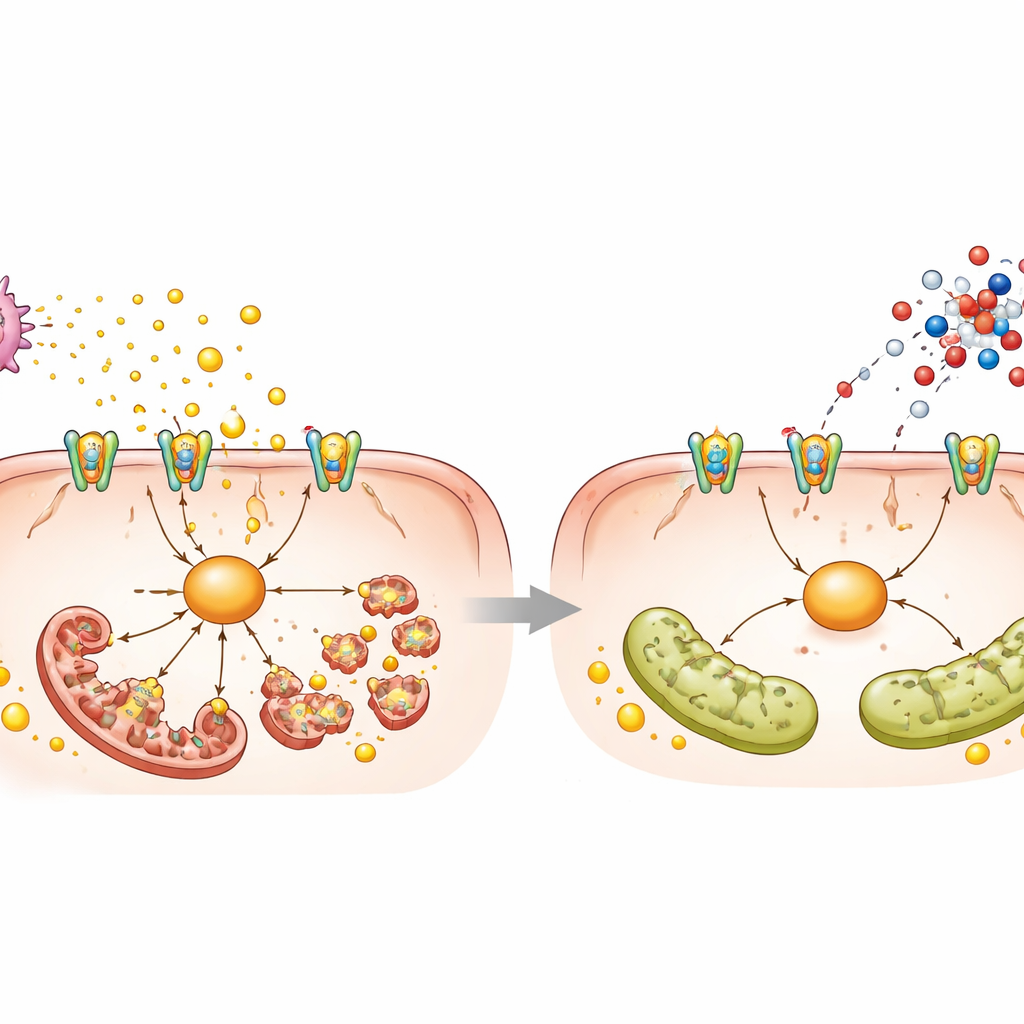
Plaquetas, una señal tóxica y una cadena molecular
Para entender cómo ejerce sus efectos el L‑aspártico, los investigadores combinaron perfiles de actividad génica y metabolitos tras una única dosis. Surgió una señal inesperada: vías relacionadas con la activación plaquetaria y una molécula mensajera llamada GMPc. En la esteatosis, las plaquetas en sangre y en el hígado eran más numerosas y activadas, y liberaban ATP adicional, una molécula energética normal que se vuelve dañina cuando se vierte fuera de las células. Este ATP activó un receptor llamado P2X7 en las células hepáticas, que a su vez activó una proteína llamada NEK7 y la proteína de fisión DRP1, impulsando la fragmentación mitocondrial y promoviendo la acumulación de grasa y la muerte celular. El L‑aspártico elevó los niveles de GMPc dentro de las plaquetas, atenuó su activación y agregación, redujo la liberación de ATP y calmó esta cadena P2X7–NEK7–DRP1 dentro de las células hepáticas. Bloquear directamente las plaquetas con aspirina, inhibir P2X7 o reducir NEK7 reprodujo muchos de los efectos protectores del L‑aspártico, lo que respalda la idea de que el diálogo plaqueta–hígado es central en el daño.
Qué podría significar esto para los pacientes
En conjunto, estos hallazgos sugieren que en la enfermedad hepática grasa, las plaquetas hiperactivas bombardean el hígado con ATP, lo que desencadena una cascada molecular que destruye las mitocondrias y empeora la acumulación de grasa y el daño. En ratones, suplementar con L‑aspártico rompe este bucle: mantiene las plaquetas más calmadas, limita la liberación de ATP, preserva la forma y la función mitocondrial y revierte tanto la esteatosis simple como la enfermedad inflamatoria y fibrótica. Dado que el L‑aspártico es barato y ya se usa como agente de apoyo hepático, el trabajo lo destaca como un candidato prometedor para probar en MASLD y MASH humanos, y apunta además a la lesión mitocondrial impulsada por plaquetas como un nuevo objetivo para futuras terapias.
Cita: Cao, WJ., Su, R., Fu, HL. et al. Supplementation of L-aspartate corrects MASLD and MASH in mice by inhibiting platelet–hepatocyte interaction-mediated mitochondrial fragmentation via the ATP–P2X7–NEK7–DRP1 axis. Exp Mol Med 58, 533–547 (2026). https://doi.org/10.1038/s12276-026-01648-9
Palabras clave: enfermedad hepática grasa, plaquetas, mitocondrias, L‑aspártico, enfermedad hepática metabólica