Clear Sky Science · es
Progresión de la esclerosis múltiple asociada a la microglía: identificación de dianas y compromiso terapéutico en modelos humanos in vitro
Por qué importan las células inmunitarias del cerebro en la esclerosis múltiple
La esclerosis múltiple (EM) suele describirse como una enfermedad en la que el sistema inmunitario del cuerpo ataca el cerebro y la médula espinal. Muchos fármacos actuales reducen con éxito los ataques súbitos, o brotes, pero no detienen el empeoramiento lento y silencioso que muchos pacientes experimentan a lo largo de los años. Esta revisión explica cómo unas diminutas células inmunitarias que viven de forma permanente en el cerebro, llamadas microglías, pueden impulsar ese declive a largo plazo —y cómo nuevos modelos cerebrales humanos cultivados en el laboratorio están ayudando a los científicos a encontrar tratamientos que finalmente puedan ralentizar o frenar la progresión.
El motor oculto del daño continuo
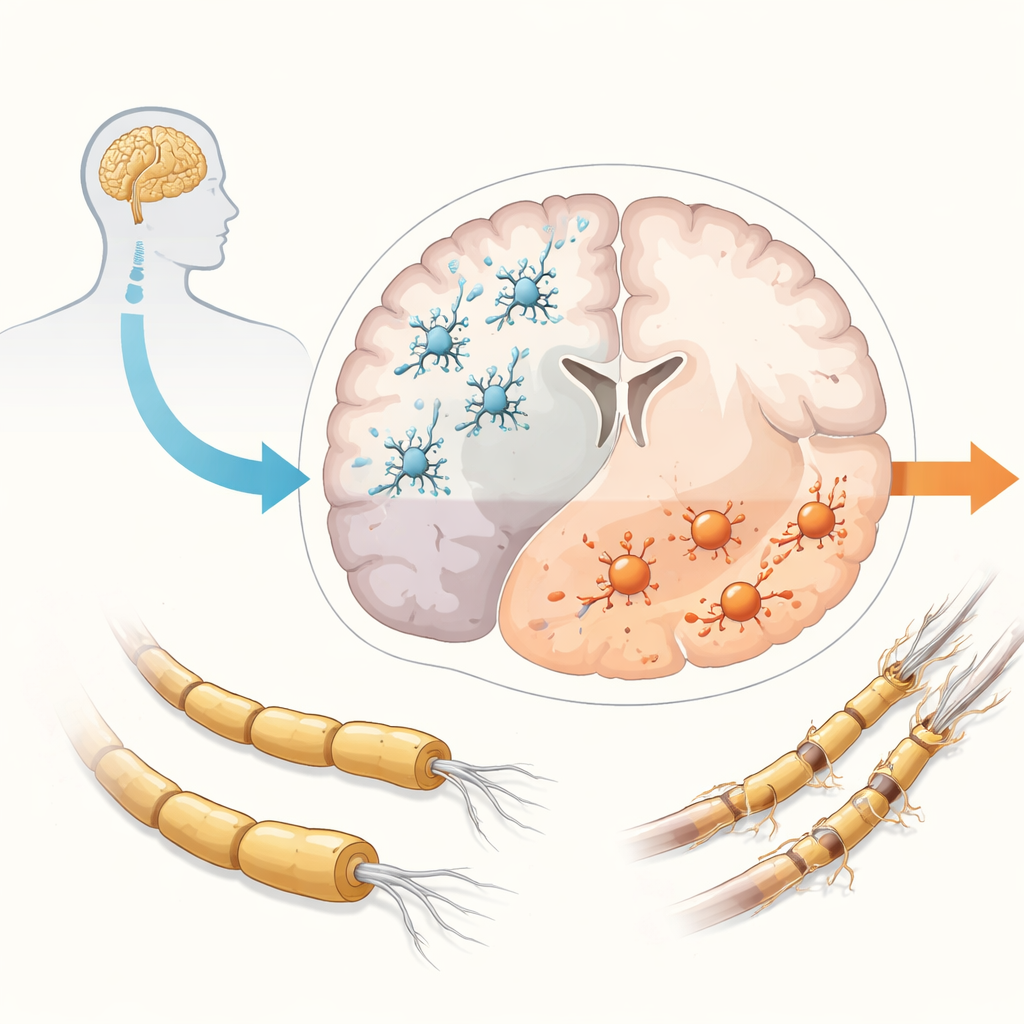
La EM se ha dividido tradicionalmente en formas remitente y progresiva, pero ahora hay evidencia de que la progresión comienza muy pronto en casi todas las personas con la enfermedad, incluso cuando aún parecen tener solo brotes. Mientras que los brotes son impulsados por células inmunitarias que entran desde la sangre, la progresión parece estar alimentada por inflamación atrapada dentro del cerebro y la médula espinal. En este entorno aislado, las microglías participan en muchos procesos dañinos: inflamación continua, pérdida de la vaina aislante de mielina en fibras nerviosas tanto de materia blanca como gris, acumulación de compuestos oxidativos perjudiciales y fallo de la reparación. El resultado final es la pérdida gradual de neuronas y de sus conexiones. Las microglías normalmente ayudan a mantener el cerebro sano al eliminar desechos y apoyar a las neuronas, pero en la EM a menudo pasan a estados más agresivos y pierden parte de sus funciones protectoras, lo que las convierte en sospechosas principales en la conducción de la progresión.
Por qué los modelos animales tradicionales se quedan cortos
Durante décadas, los estudios en ratones y otros animales han sido cruciales para desarrollar fármacos que limitan los brotes, pero en gran medida no han producido terapias que detengan la progresión. Una razón es que los modelos animales solo reproducen parcialmente la EM humana y no reflejan por completo la inflamación compleja y duradera observada en los cerebros de los pacientes. Las microglías de los roedores también difieren de las humanas en genes y respuestas importantes. Como resultado, tratamientos que parecen prometedores en animales a menudo no funcionan en personas. La escasez de modelos animales que capturen verdaderamente la EM progresiva ha impulsado a los investigadores a construir nuevos sistemas humanos en el laboratorio, donde pueden estudiar más directamente las microglías y otras células cerebrales.
Construir modelos humanos del cerebro en una placa
Los científicos utilizan ahora varias capas de modelos de laboratorio para estudiar las microglías humanas. Las células primarias tomadas directamente de tejido cerebral de roedor o humano preservan muchas características naturales pero son difíciles de obtener, cambian rápidamente fuera de su entorno nativo y no se pueden escalar fácilmente. Para superar estos obstáculos, los investigadores recurren a células madre pluripotentes inducidas (iPS): células adultas reprogramadas a un estado flexible similar al de las células madre. Estas iPS pueden guiarse para convertirse en microglías, neuronas u otras células cerebrales. En cultivos simples en dos dimensiones, las microglías derivadas de iPS capturan muchos rasgos clave y pueden producirse en gran número, lo que permite experimentos detallados y cribados de fármacos. Incluso pueden generarse a partir de pacientes individuales con EM, revelando diferencias intrínsecas como actividad génica alterada y cambios en cómo estas células responden al estrés y eliminan desechos.
Añadir vecindarios cerebrales realistas
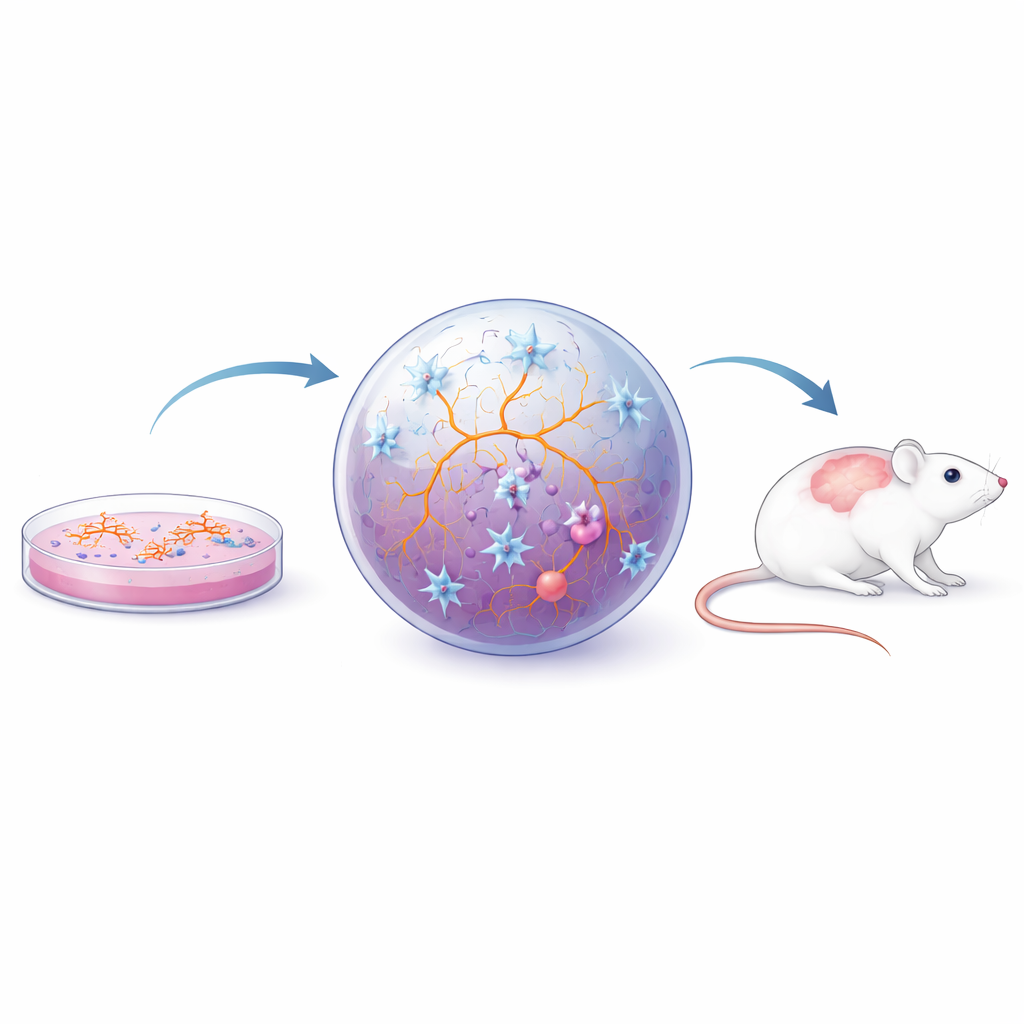
Dado que el comportamiento microglial está fuertemente moldeado por su entorno, los investigadores han avanzado más allá de las monocapas hacia montajes más realistas. En cocultivos bidimensionales, las microglías crecen junto con neuronas y células de soporte, lo que les ayuda a adoptar formas y comportamientos más naturales y permite a los científicos explorar cómo los tipos celulares se influyen mutuamente. Los esferoides y organoides tridimensionales —pequeñas piezas autoorganizadas de tejido similar al cerebral— van más allá, proporcionando un entorno blando y denso que se parece más al tejido cerebral real. Cuando las microglías se integran en estas estructuras, muestran formas ramificadas complejas, reaccionan a lesiones, interactúan con una capa similar a la barrera hematoencefálica y responden a señales inflamatorias presentes en el líquido cefalorraquídeo de personas con EM. Tales modelos se han utilizado para estudiar cómo la inflamación crónica desencadena un estado «cansado pero inflamado» llamado senescencia celular en microglías y astrocitos, y cómo los cambios en el manejo lipídico microglial pueden perjudicar la reparación de la mielina. Paralelamente, trasplantar microglías humanas derivadas de iPS u organoides al cerebro de ratones permite que estas células maduren más dentro de una red viva y ser probadas en modelos de enfermedad similares a la EM ya establecidos.
De los modelos de laboratorio a tratamientos futuros
En conjunto, estos modelos humanos in vitro y quiméricos forman un conjunto de herramientas para diseccionar cómo las microglías contribuyen a la progresión de la EM y para probar nuevas terapias que buscan calmar la actividad microglial dañina a la vez que restauran sus funciones protectoras. Aunque ninguno de los modelos reproduce completamente el cerebro humano, cada uno captura distintas piezas del rompecabezas y, juntos, salvan la brecha entre cultivos celulares simples y modelos animales imperfectos. Al combinar los conocimientos de estos sistemas, los investigadores esperan identificar dianas farmacológicas precisas —como vías que controlan la inflamación, cambios similares al envejecimiento y el metabolismo de lípidos en microglías— que finalmente puedan traducirse en tratamientos que ralenticen o detengan la discapacidad gradual que caracteriza a la EM progresiva.
Cita: Blenkle, A., Geladaris, A. & Weber, M.S. Microglia-associated progression of multiple sclerosis: target identification and therapeutic engagement in human in vitro models. Exp Mol Med 58, 357–365 (2026). https://doi.org/10.1038/s12276-026-01647-w
Palabras clave: progresión de la esclerosis múltiple, microglía, células madre pluripotentes inducidas, organoides cerebrales, neuroinflamación