Clear Sky Science · es
PAK4 en enfermedades metabólicas: regulación por señales nutricionales e implicaciones terapéuticas
Por qué importa un interruptor celular para la salud cotidiana
La obesidad, la diabetes tipo 2 y la enfermedad del hígado graso suelen atribuirse solo a las calorías, pero en el interior de nuestras células, interruptores moleculares deciden si quemamos o almacenamos combustible. Esta revisión se centra en uno de esos interruptores, una proteína llamada PAK4, y explica cómo responde a las señales cambiantes de nutrientes y hormonas, remodelando el metabolismo en tejido adiposo, hígado y músculo. Comprender este sistema de control oculto puede abrir la puerta a nuevos tratamientos que aborden varias enfermedades metabólicas a la vez en lugar de tratar un síntoma tras otro. 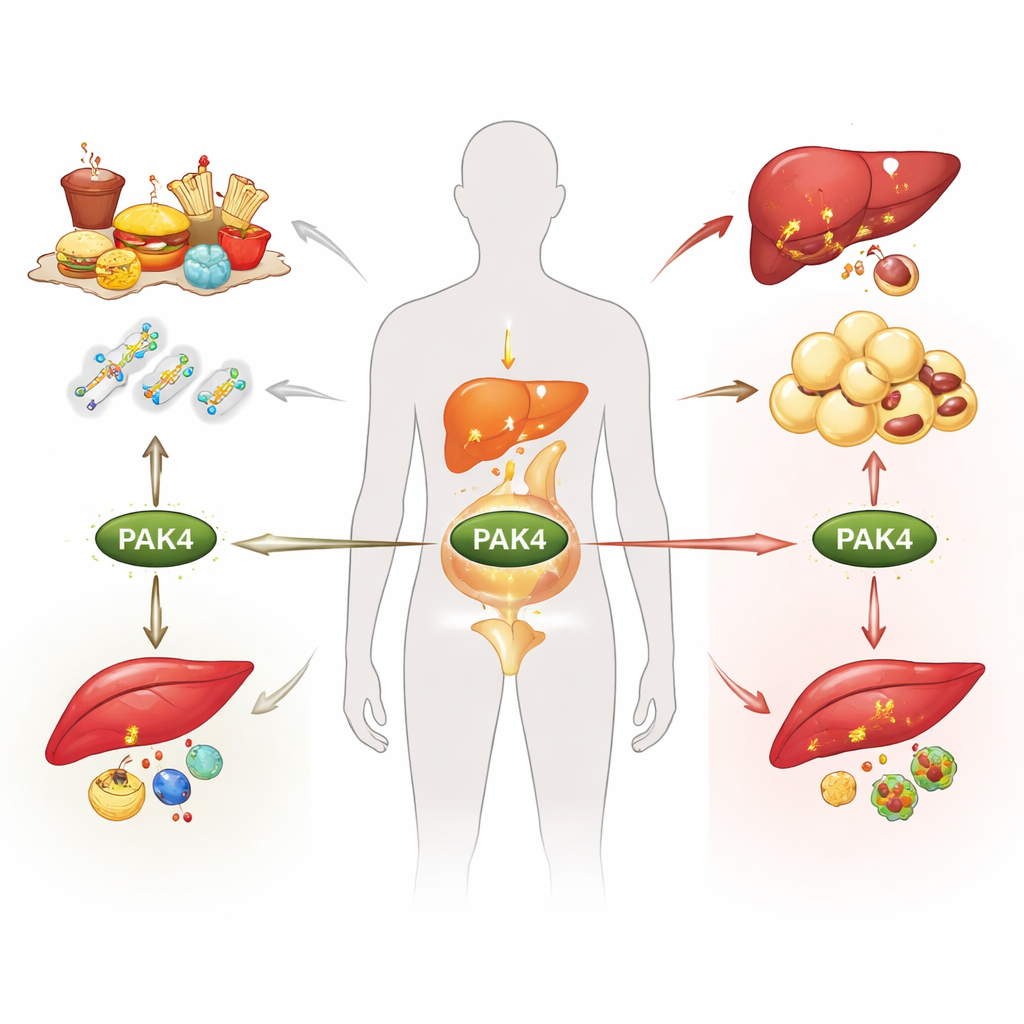
Un interruptor maestro escondido en nuestras células
PAK4 pertenece a una familia de enzimas que transmiten señales de pequeños “mensajeros” moleculares dentro de las células. En condiciones saludables, PAK4 está presente en niveles bajos en los principales órganos metabólicos. Cuando se altera el equilibrio energético, como en la obesidad o la diabetes tipo 2, sus niveles aumentan en el tejido adiposo, el hígado y el músculo esquelético. La actividad de PAK4 se controla de varias maneras: por mensajeros upstream que cambian su conformación y por etiquetas químicas añadidas o eliminadas tras la síntesis de la proteína. Estas incluyen etiquetas fosfato que pueden activar PAK4 o marcarlo para su destrucción, así como otras modificaciones que afectan su estabilidad o actividad. El ayuno, la alimentación, las hormonas y el estrés influyen en estas marcas, de modo que PAK4 “percibe” efectivamente el estado nutricional del organismo y transmite esa información a vías metabólicas clave.
Cómo PAK4 inclina a las células grasas hacia el almacenamiento
En las células grasas, PAK4 actúa como un freno a la quema de grasa. Normalmente, cuando ayunamos o aumentan las hormonas de estrés, otra enzima llamada PKA desencadena la degradación controlada de la grasa almacenada dentro de pequeñas gotas. La revisión describe cómo PAK4 contrarresta este proceso al colocar etiquetas fosfato inhibitorias directamente sobre la lipasa sensible a hormonas y sobre una proteína de unión a ácidos grasos que ayuda a transportar las moléculas de grasa. Estos cambios debilitan la maquinaria que libera grasa del depósito. PAK4 también favorece la formación de nuevas células adiposas en etapas tempranas de la vida al ayudar a proteínas del ciclo celular a impulsar a las células precursoras a convertirse en adipocitos maduros. Cuando PAK4 se elimina o bloquea en modelos animales, las células grasas queman más combustible, muestran rasgos de “marroneamiento” que aumentan el gasto energético, y los animales quedan protegidos frente al aumento de peso inducido por la dieta. 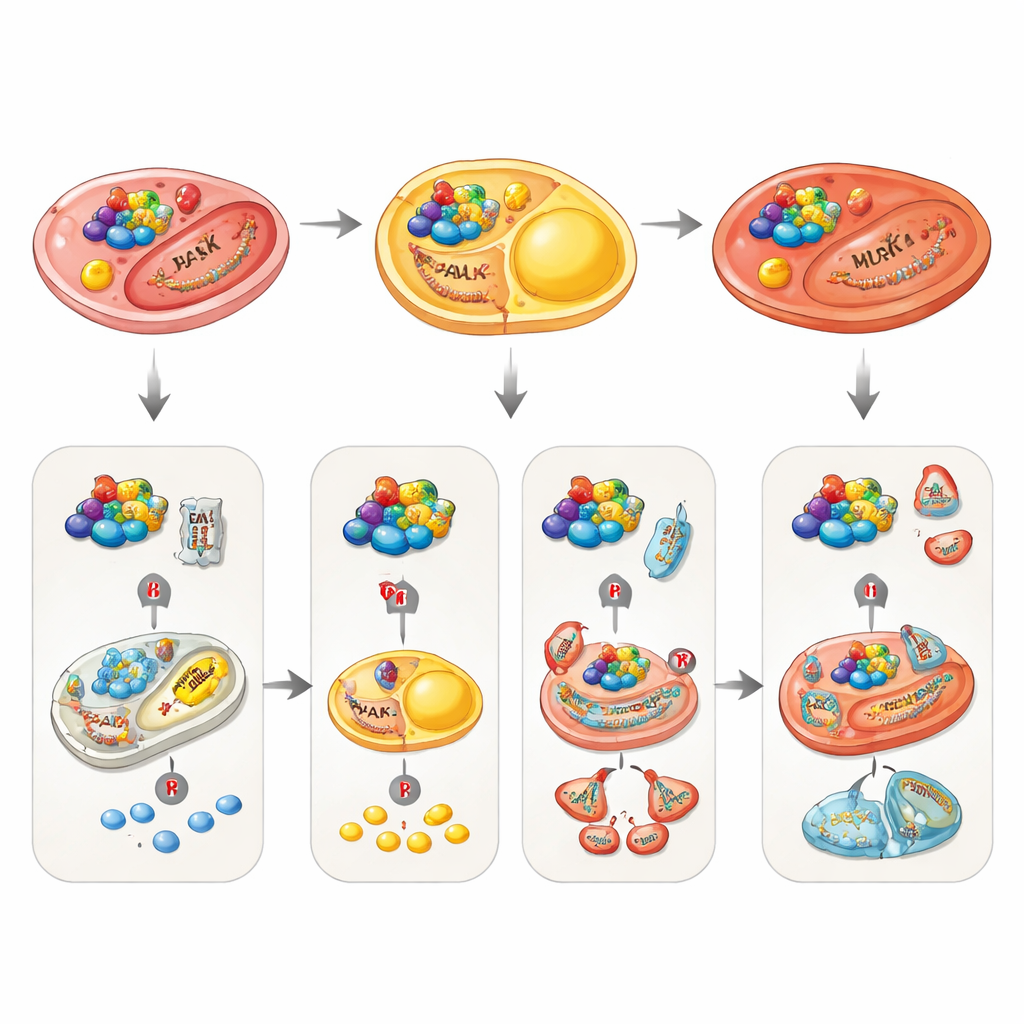
El papel de PAK4 en el hígado graso y el manejo del azúcar en el músculo
En el hígado, PAK4 vuelve a favorecer el almacenamiento sobre la quema. Durante el ayuno o con una dieta cetogénica, los niveles de PAK4 disminuyen, permitiendo que las células hepáticas aumenten la degradación de grasas y la producción de cetonas, que suministran energía a otros tejidos e incluso pueden ralentizar el crecimiento tumoral. Cuando PAK4 es abundante, añade etiquetas fosfato a un correpresor nuclear que luego reprime a PPARα, un regulador maestro de la oxidación de grasas y la formación de cetonas. El resultado es más grasa atrapada en el hígado y menos cetonas protectoras en la sangre. En el músculo esquelético, PAK4 interfiere con AMPK, un sensor energético central que promueve tanto la captación de glucosa como la actividad mitocondrial. Al modificar AMPK de una manera que bloquea su activación, PAK4 reduce la cantidad de transportador de glucosa en la superficie de la célula muscular y contribuye a la resistencia a la insulina. La pérdida específica de PAK4 en el músculo de ratones revierte estos efectos, mejorando el control de la glucemia incluso en condiciones de obesidad.
Estrés, protección y conexiones con otros interruptores celulares
La revisión también destaca el impacto de PAK4 más allá del metabolismo cotidiano. Durante episodios de flujo sanguíneo reducido y reperfusión súbita en órganos como el hígado, PAK4 debilita las defensas antioxidantes al marcar y desestabilizar Nrf2, un protector clave frente al estrés oxidativo. Al mismo tiempo, otro miembro de la familia, PAK1, suele desempeñar papeles más favorables en el músculo cardíaco, el músculo esquelético y las células secretoras de insulina del páncreas, ayudando a mantener un manejo normal de la glucosa. Este contraste entre la señalización perjudicial de PAK4 en la enfermedad metabólica y las acciones generalmente beneficiosas de PAK1 subraya la necesidad de fármacos altamente selectivos que inhiban PAK4 sin alterar proteínas relacionadas que son esenciales para la salud cardíaca y endocrina.
Convertir un hallazgo en tratamiento
Dado que PAK4 está sobreactivado en el cáncer y en trastornos metabólicos, los diseñadores de fármacos han buscado pequeñas moléculas que bloqueen su actividad, así como nuevos medicamentos “degradadores” que etiqueten al propio PAK4 para su eliminación. Los primeros compuestos bloqueadores de PAK4 mostraron potencial antitumoral pero enfrentaron desafíos de especificidad y farmacocinética. Moléculas más recientes que apuntan con mayor precisión a PAK4 han producido resultados llamativos en ratones obesos: menor peso corporal sin menor ingesta, hígados más sanos, músculos más activos y mejor control de la glucemia. Los fármacos degradadores van un paso más allá al eliminar físicamente PAK4, y estudios animales iniciales sugieren que podrían proteger frente a la pérdida muscular y ciertos tipos de cáncer. En conjunto, estos hallazgos respaldan la idea de que reducir la actividad de PAK4 podría aliviar simultáneamente la obesidad, la diabetes y el hígado graso, convirtiendo un interruptor celular otrora oscuro en un prometedor objetivo para futuras terapias metabólicas.
Cita: Bang, I.H., Park, BH. & Bae, E.J. PAK4 in metabolic diseases: regulation by nutrient signals and therapeutic implications. Exp Mol Med 58, 416–424 (2026). https://doi.org/10.1038/s12276-026-01645-y
Palabras clave: PAK4, enfermedad metabólica, obesidad, hígado graso, resistencia a la insulina