Clear Sky Science · es
La proteína sensible al redox HMGB1: roles intracelulares y extracelulares
Por qué importa una proteína que cambia de forma para la salud
En el interior de casi cada célula de tu cuerpo reside una pequeña proteína llamada HMGB1 que se comporta un poco como una navaja suiza. En condiciones de calma ayuda discretamente a organizar el ADN. Pero cuando las células están estresadas o dañadas, HMGB1 puede salir del núcleo, deslizarse hacia el tejido circundante y actuar como una señal de alarma para el sistema inmune. Este artículo de revisión explica cómo pequeños cambios químicos impulsados por la oxidación convierten a HMGB1 en personalidades biológicas muy distintas —unas que pueden proteger los tejidos, impulsar la inflamación o incluso contribuir a enfermedades crónicas. Comprender este «anillo del humor» molecular podría abrir nuevas vías para calmar la inflamación excesiva sin apagar por completo el sistema inmunitario.
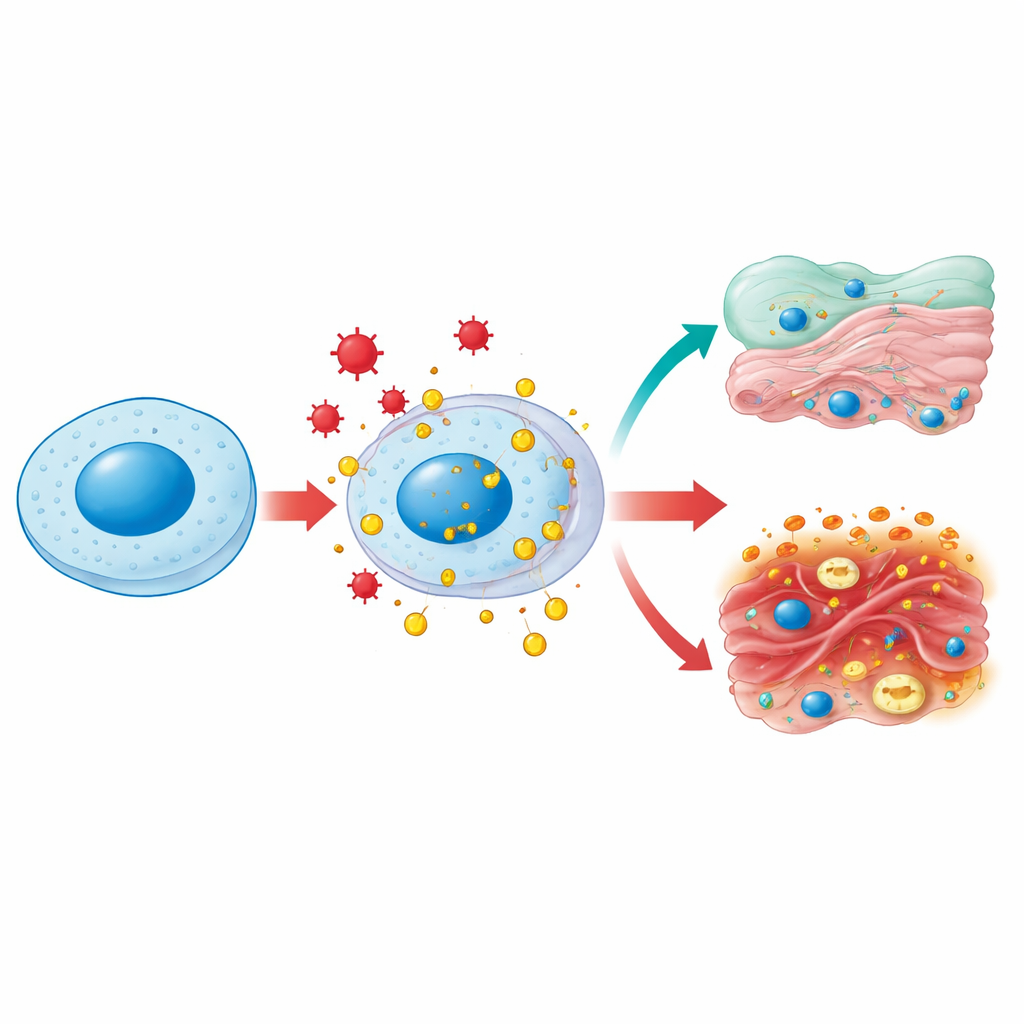
Una proteína, muchos vecindarios
HMGB1 normalmente vive en el núcleo celular, donde dobla y afloja el ADN para que los genes puedan copiarse y repararse. Bajo estrés —como infección, hiperglucemia o lesión tóxica— puede sufrir modificaciones químicas y ser escoltada hacia el interior acuoso de la célula y luego hacia el exterior. En el citoplasma, HMGB1 ayuda a mantener las mitocondrias, las centrales energéticas de la célula, saludables fomentando un proceso de limpieza llamado autofagia y evitando la fragmentación excesiva de estos orgánulos. Cuando se libera fuera de la célula, HMGB1 se convierte en una clásica “señal de peligro”: las células inmunitarias la reconocen como un indicio de daño tisular y acuden al lugar. Así, la misma molécula desempeña funciones de mantenimiento dentro de las células y roles de alarma fuera de ellas, según dónde se encuentre y cómo haya sido químicamente modulada.
Cómo la oxidación reescribe su comportamiento
El núcleo de esta revisión es cómo la oxidación —reacciones impulsadas por especies reactivas de oxígeno (ROS)— remodela a HMGB1. La proteína contiene tres residuos que portan azufre que actúan como pequeños interruptores. En su estado totalmente reducido, HMGB1 tiende a apoyar la supervivencia celular y el reclutamiento de células reparadoras. Una oxidación leve puede enlazar dos de estos sitios dentro de la misma proteína, creando una forma “disulfuro” que es especialmente buena para engancharse a receptores inmunitarios como los receptores tipo Toll y RAGE en la superficie celular. Esta versión estimula fuertemente la producción de mensajeros inflamatorios. Un estrés oxidativo más intenso puede empujar la molécula hacia una forma sobreoxidada que ya no puede unirse eficazmente al ADN ni a los receptores; esta versión “quemada” queda inmunológicamente silente y se asocia con la fase de resolución de la inflamación y con programas de muerte celular que no provocan un ataque inmune.
De señales de muerte celular a motores de enfermedad
HMGB1 está profundamente entrelazado con las múltiples formas en que las células mueren. Durante formas violentas de muerte como necrosis, necroptosis, ferroptosis y piroptosis, HMGB1 se filtra o es transportada activamente fuera de las células, llevando una firma redox que refleja las condiciones oxidativas circundantes. Al inicio de la necrosis, tiende a encontrarse en una forma reducida, mientras que el estrés prolongado la empuja hacia estados más oxidados. Una vez fuera, HMGB1 reducido puede fomentar la autofagia protectora en algunas células cancerosas, ayudándolas a sobrevivir a la quimioterapia, mientras que las formas ricas en disulfuros y dimerizadas amplifican las cascadas inflamatorias y la activación del complemento que pueden agravar el daño tisular. HMGB1 también puede retroalimentar y promover ciertas vías de muerte —por ejemplo, asociándose con lípidos bacterianos para desencadenar necroptosis o impulsando la muerte celular dependiente de hierro en las células de soporte cerebral tras un ictus. De este modo, HMGB1 tanto marca como modula el equilibrio vida–muerte en los tejidos.
Vínculos con la inflamación, la autoinmunidad y el cáncer
Debido a que su comportamiento es muy sensible a la oxidación, las distintas variantes de HMGB1 aparecen en patrones característicos según la enfermedad. HMGB1 rico en disulfuros se asocia fuertemente con la inflamación crónica: aparece en las articulaciones inflamadas de la artritis reumatoide, en el hígado fibrótico, en la lesión pulmonar, en el daño por isquemia–reperfusión tras cirugía y en la sepsis, donde sus niveles sanguíneos correlacionan con la gravedad y el riesgo de muerte. HMGB1 reducido, por el contrario, suele correlacionar con migración celular y remodelado tisular, como el movimiento de fibroblastos cardíacos o de monocitos guiados por la quimiocina CXCL12. HMGB1 sobreoxidado e inmunológicamente silencioso se encuentra enriquecido en contextos como la apoptosis en fases tardías, donde el organismo quiere eliminar las células moribundas sin provocar una respuesta. En los tumores, la forma disulfuro favorece un entorno inmune supresor y permisivo al crecimiento, mientras que bloquear HMGB1 puede reducir tumores y aumentar la eficacia de las inmunoterapias basadas en puntos de control.
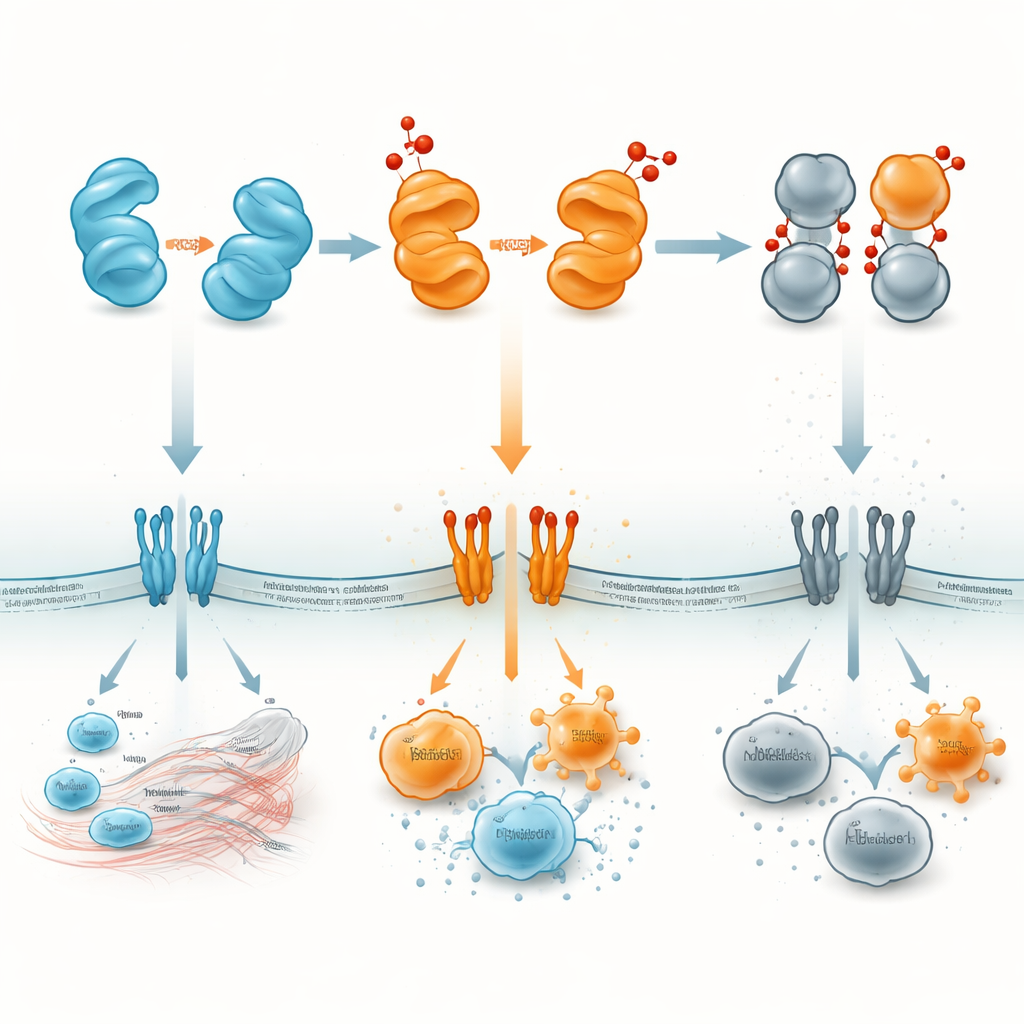
Convertir una alarma molecular en un objetivo terapéutico
Para un observador no especializado, HMGB1 puede pensarse como una pequeña alarma proteica cuya intensidad y mensaje cambian con su estado químico. HMGB1 reducido tiende a reclutar equipos de reparación; las formas disulfuro y dimerizadas pueden emitir una alarma estridente que alimenta una inflamación dañina; y la forma totalmente oxidada cae efectivamente en silencio, ayudando a que la inflamación remita. Al mapear dónde y cuándo aparece cada versión —en núcleos, en el citoplasma, en sangre o en órganos concretos— los investigadores esperan diseñar fármacos que bloqueen las formas perjudiciales o estabilicen las beneficiosas. Tales estrategias podrían permitir a los médicos tratar la sepsis, la autoinmunidad, el ictus, la lesión pulmonar o el cáncer apuntando no solo a HMGB1 en sí, sino al “atenuador” oxidativo que controla cómo esta proteína se comunica con el sistema inmune.
Cita: Kwak, M.S., Jung, S.F., Park, I.H. et al. The redox-sensitive protein HMGB1: intracellular and extracellular roles. Exp Mol Med 58, 345–356 (2026). https://doi.org/10.1038/s12276-026-01640-3
Palabras clave: HMGB1, inflamación, estrés oxidativo, muerte celular, enfermedad autoinmune