Clear Sky Science · es
Transducción mecánica a través de los receptores de células T: consensos, controversias y perspectivas futuras
Cómo las células inmunitarias perciben su entorno
Nuestro sistema inmunitario no se limita a captar señales químicas; también percibe fuerzas físicas. Este artículo de revisión explora cómo las células T —glóbulos blancos que buscan virus y cáncer— pueden usar pequeños empujes y tirones sobre sus receptores de superficie para decidir si atacan. Comprender este “sentido del tacto” a escala molecular podría reconfigurar la forma en que pensamos sobre las vacunas, la inmunoterapia contra el cáncer y las enfermedades autoinmunes.
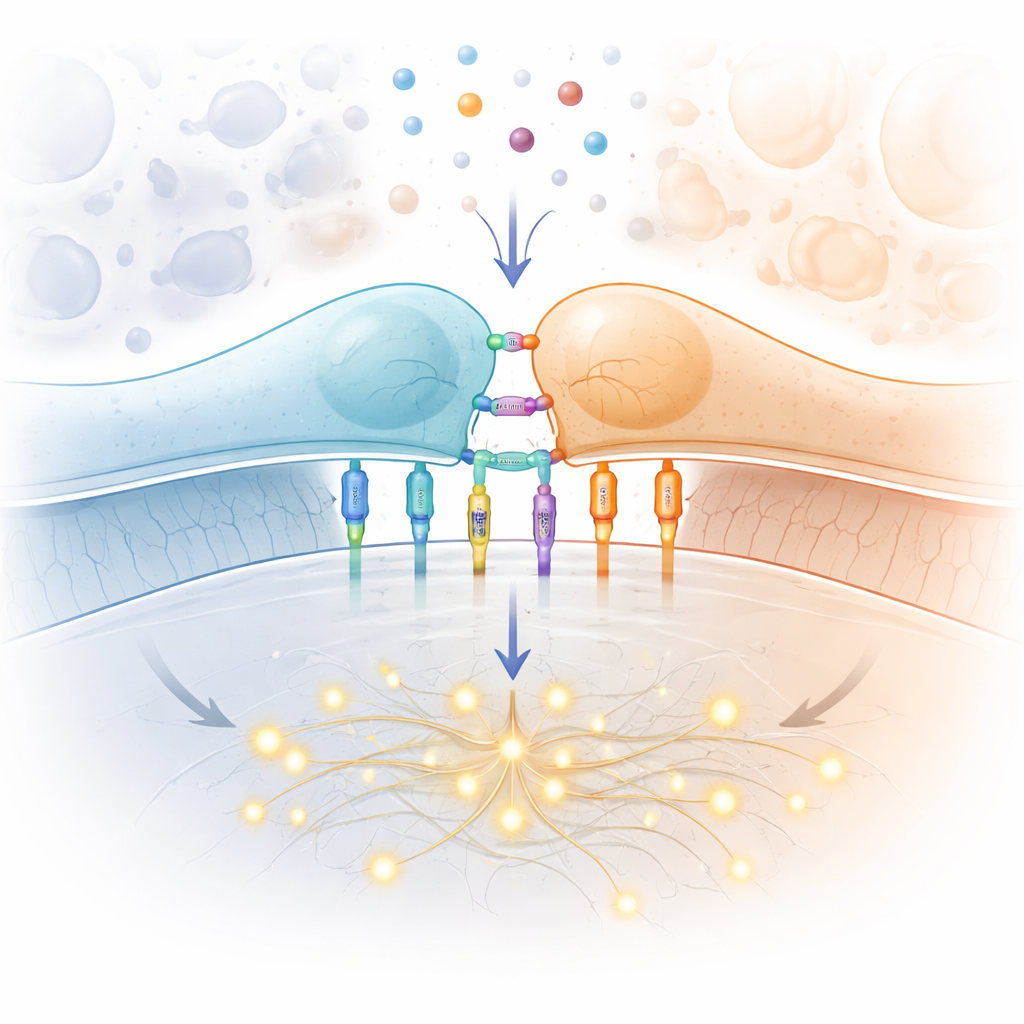
La función especial del receptor de la célula T
En el centro de la historia está el receptor de la célula T, una máquina molecular en la superficie de la célula T que inspecciona fragmentos de proteínas presentados por otras células. Cuando se encuentra el fragmento correcto, la célula T puede activarse, multiplicarse y eliminar objetivos infectados o cancerosos. Este receptor debe cumplir un conjunto exigente de demandas: reaccionar ante cantidades extremadamente pequeñas de fragmentos extraños, ignorar un mar de fragmentos propios inofensivos, actuar con rapidez mientras las células T patrullan el organismo y hacerlo para millones de variantes de receptor en cada persona. El cableado clásico de la vía de señalización dentro de la célula —que incluye quinasas, andamiajes y factores de transcripción— está bien cartografiado. Lo que sigue siendo misterioso es el primer paso: cómo el simple acto de unirse a un fragmento en la superficie celular convierte al receptor de silencioso a activo.
Ideas enfrentadas sobre la chispa inicial
Los investigadores han propuesto varios modelos sobre cómo el receptor de la célula T se enciende inicialmente. En una visión, la señalización comienza cuando los receptores se agrupan en pequeños cúmulos, aumentando la concentración local y permitiendo que las reacciones de señalización avancen con mayor eficacia. Otra idea enfatiza los cambios de forma: la unión podría torcer o relajar partes del complejo receptor, liberando segmentos ocultos en el interior de la célula para que las enzimas los modifiquen. Un tercer modelo destaca el hacinamiento en el contacto célula–célula. Aquí, parejas receptor–ligando cortas se empaquetan en zonas estrechas que excluyen físicamente a enzimas voluminosas que normalmente apagan las señales, inclinando el equilibrio hacia la activación. Cada modelo cuenta con respaldo experimental y explica parte del rompecabezas, pero ninguno por sí solo explica completamente la extrema sensibilidad del receptor ni su capacidad para distinguir entre fragmentos proteicos muy similares.
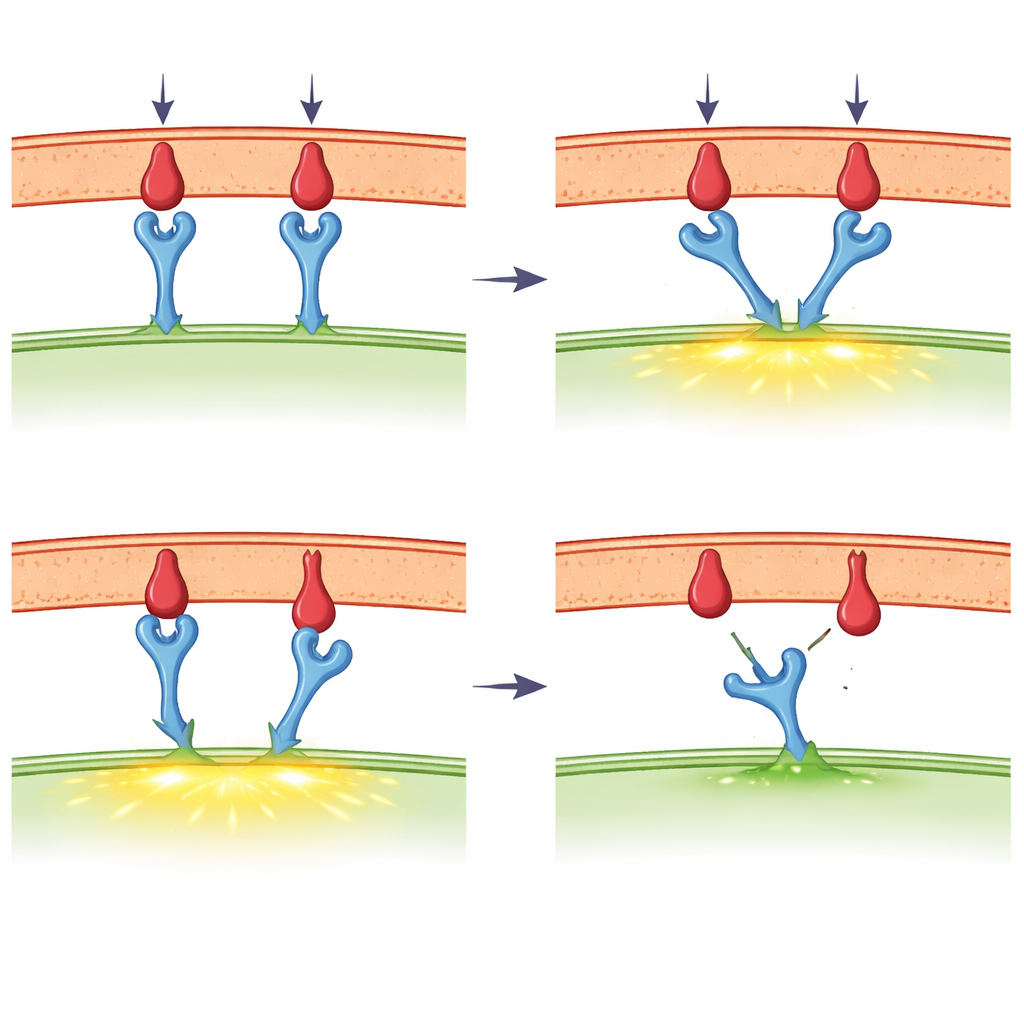
Cuando el tacto y la fuerza entran en juego
Un foco principal de la revisión es la idea emergente de que el receptor de la célula T actúa como un mecanosensor —un elemento que responde a la fuerza. Con instrumentos ultrasensibles, los científicos han tirado de enlaces individuales receptor–ligando con fuerzas billones de veces menores que el peso de una manzana. Observan que, para fragmentos extraños potentes, un ligero tirón puede prolongar la vida del enlace, un comportamiento conocido como respuesta de “catch”. Los fragmentos débiles o propios muestran en cambio un comportamiento de “slip”: se separan más rápidamente cuando se les aplica fuerza. Las propias células T generan tales fuerzas a través de su esqueleto interno de filamentos de actina y proteínas motoras, especialmente en la zona de contacto estrecho llamada sinapsis inmune. Nuevos sondas moleculares de tensión muestran que las fuerzas en el rango donde aparece el comportamiento catch están presentes durante la activación temprana de las células T, aunque distintos métodos experimentales a veces informan valores diferentes y han provocado un vivo debate.
Decodificar lo propio de lo ajeno a lo largo del tiempo
El artículo también revisa cómo las células T podrían convertir eventos de contacto ruidosos y fugaces en decisiones fiables. Una idea antigua, la depuración cinética, sugiere que la señalización progresa a través de una secuencia de pasos que requiere tiempo; solo los fragmentos que mantienen el receptor comprometido el tiempo suficiente permiten que la cadena alcance un punto sin retorno. Los autores discuten cómo los efectos mecánicos pueden afinar este filtro temporal: las fuerzas de tracción extienden la vida de los enlaces productivos y acortan la de los no productivos, ampliando la brecha entre estímulos fuertes y débiles. También consideran cómo las células T pueden integrar muchos contactos cortos en lugar de depender de uno solo largo, y cómo la retroalimentación dentro de la red de señalización puede almacenar una especie de “memoria” molecular de encuentros recientes. Estas mejoras ayudan a explicar cómo las células T logran a la vez rapidez y precisión en entornos tisulares complejos.
Principios compartidos entre receptores inmunitarios
Aunque el receptor de la célula T tiene exigencias excepcionales, muchos de sus principios de diseño aparecen en otros receptores inmunitarios. Los receptores de células B y los receptores de anticuerpos en células inmunitarias innatas comparten motivos de señalización similares y a menudo operan en zonas de contacto estrecho donde el hacinamiento, la agregación y las fuerzas citosqueléticas importan. Se han descrito respuestas similares a la fuerza tipo catch para varios pares receptor–ligando. Esto sugiere que percibir señales mecánicas puede ser una estrategia general que el sistema inmunitario utiliza para comprobar si un objetivo está firmemente anclado, correctamente presentado y merece una respuesta.
Por qué esto importa para la salud y la terapia
Para el lector no especializado, la conclusión es que las células T no solo detectan la presencia de moléculas extrañas: también prueban cómo se sienten esas moléculas cuando se tiran de ellas. Combinando química, física y biología celular, esta revisión sostiene que los receptores inmunitarios convierten diferencias sutiles tanto en afinidad como en fuerza en decisiones de vida o muerte para las células. Un entendimiento más profundo de estas reglas mecanobiológicas podría orientar el diseño de mejores terapias basadas en células T, vacunas más precisas y nuevos tratamientos que modulen las respuestas inmunitarias al alterar no solo a qué se unen los receptores, sino cómo se comprometen mecánicamente.
Cita: Travaglino, S., Jeon, Y., Kim, Y. et al. Mechanotransduction through T cell receptors: consensus, controversies and future outlooks. Exp Mol Med 58, 319–335 (2026). https://doi.org/10.1038/s12276-026-01639-w
Palabras clave: receptor de célula T, transducción mecánica, enlaces catch, sinapsis inmune, depuración cinética