Clear Sky Science · es
UBE2M como puente entre la neddilación y la regulación del ciclo celular en el adenocarcinoma colorrectal
Por qué esta investigación importa para el cáncer intestinal
El cáncer colorrectal es uno de los tumores más frecuentes y letales en todo el mundo, en gran parte porque las células tumorales aprenden a dividirse de forma incontrolada. Este estudio revela un interruptor de control hasta ahora oculto que ayuda a las células del cáncer colorrectal a atravesar con rapidez un punto de control crítico de la división celular. Al explicar cómo funciona este interruptor a nivel molecular —y al mostrar que un fármaco antifúngico ya existente puede interferir en él—, el trabajo apunta a una posible vía nueva para ralentizar o detener el crecimiento tumoral.
Una capa oculta de control dentro de las células tumorales
Las células no se dividen al azar; avanzan mediante un ciclo ordenado con puntos de control que verifican si es seguro copiar el ADN y dividirse en dos. Las células cancerosas a menudo alteran estos puntos de control. Los autores se centraron en un proceso de etiquetado químico llamado neddilación, que modifica sutilmente las proteínas después de su síntesis. Estudios previos sugerían que la neddilación está más activa en muchos cánceres, pero no quedaba claro cómo se relacionaba con el ciclo de división de las células colorrectales. Utilizando grandes conjuntos de datos de células individuales de tumores humanos, junto con datos de expresión génica en bloque de más de 1.800 pacientes, el equipo encontró que la actividad de la neddilación es especialmente alta en células malignas intestinales que se encuentran en la fase G2/M—la puerta final antes de que una célula se divida.
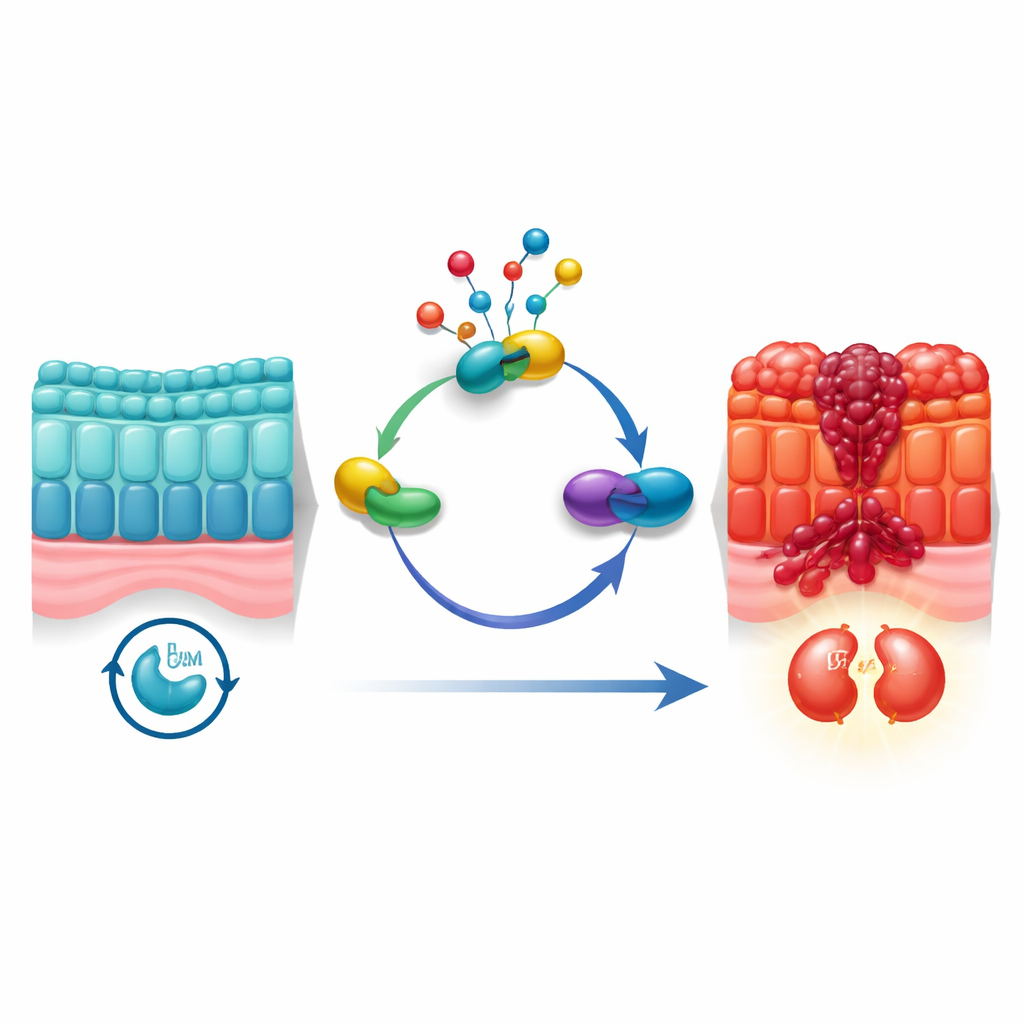
Foco en una proteína molecular “puente”
Para identificar qué moléculas conectan la neddilación con la división celular, los investigadores emplearon análisis computacionales en forma de redes para cribar miles de genes. Una proteína destacó: UBE2M, una enzima que ayuda a unir la pequeña etiqueta NEDD8 a otras proteínas. UBE2M no solo se asoció de forma destacada con las vías de neddilación y del ciclo celular en los datos; también se encontró en niveles mucho más altos en tumores colorrectales que en tejido sano adyacente. Los pacientes cuyos tumores presentaban más UBE2M tendían a tener una supervivencia peor, lo que la señala como posible impulsora más que como mero espectador. Cuando el equipo redujo UBE2M en líneas celulares cancerosas y en modelos tumorales en ratón, el crecimiento tumoral se ralentizó, las células se dividieron menos y aumentó la muerte celular programada. A la inversa, forzar la sobreproducción de UBE2M aceleró el crecimiento y la progresión del ciclo celular.
Un relevo que protege una proteína clave promotora del crecimiento
Yendo más a fondo, los científicos preguntaron cómo UBE2M ayuda a las células a dividirse. Descubrieron que UBE2M no actúa sola, sino que desencadena un relevo que involucra a otras dos proteínas, USP39 y PABPC1. Normalmente, PABPC1 es marcada para su destrucción mediante una cadena de etiquetas de ubiquitina, que la envían a la maquinaria de reciclaje proteico de la célula. El equipo mostró que UBE2M modifica químicamente a USP39 con la etiqueta NEDD8. Esta modificación aumenta la capacidad de USP39 para cortar cadenas de ubiquitina de PABPC1, rescatándola de la degradación y estabilizándola. Con más PABPC1 disponible, la célula es más eficaz traduciendo ciertos ARNm a proteína, incluido el ARNm de CCNB1, una ciclina que actúa como acelerador en el punto de control G2/M. En esencia, UBE2M ayuda a estabilizar PABPC1, que a su vez potencia la producción de CCNB1, impulsando con mayor facilidad la entrada de las células en división.
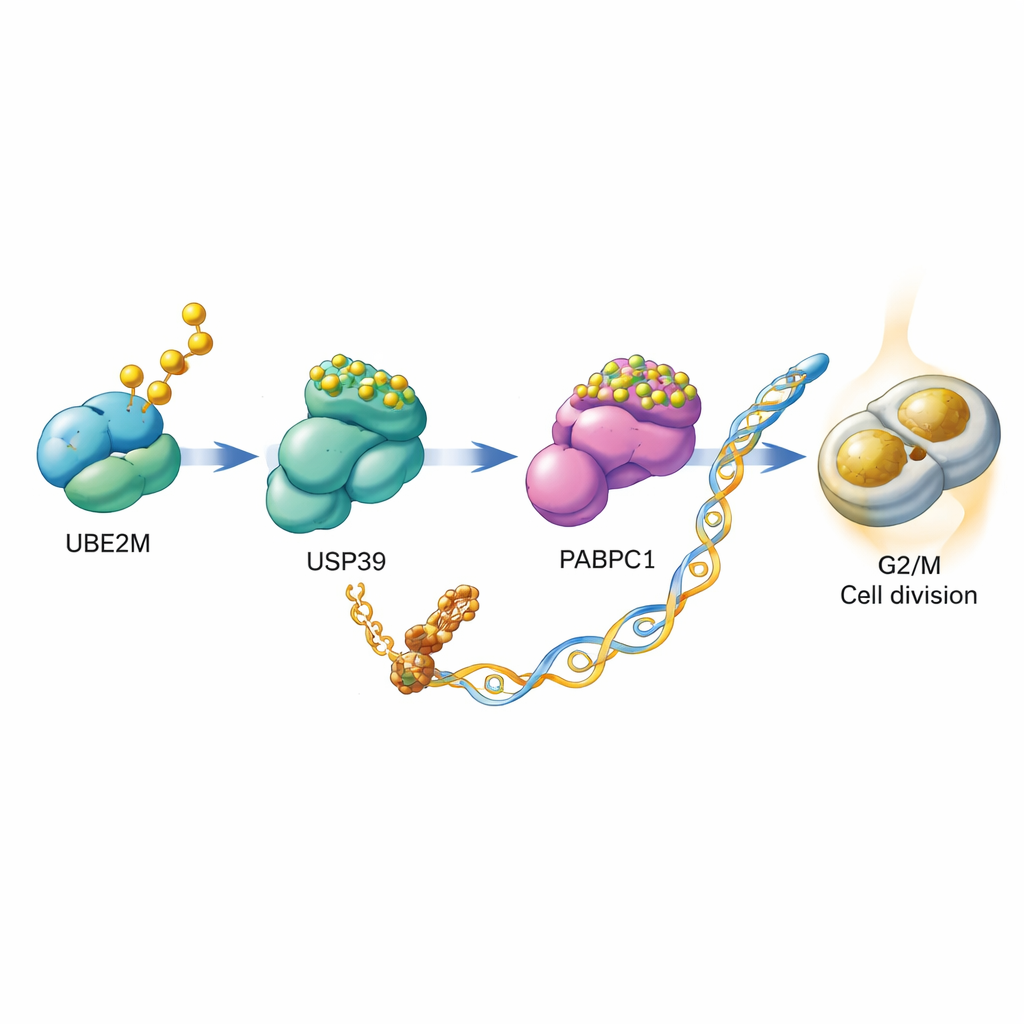
Del mecanismo molecular a una oportunidad farmacológica
El descubrimiento de esta cadena UBE2M–USP39–PABPC1–CCNB1 sugiere una nueva vulnerabilidad en las células del cáncer colorrectal. Los autores recurrieron a la micafungina, un fármaco ya usado para tratar infecciones fúngicas y recientemente identificado como inhibidor de la actividad de neddilación de UBE2M. En células de cáncer intestinal cultivadas en el laboratorio, la micafungina debilitó la neddilación de USP39, aumentó la degradación de PABPC1 y redujo los niveles de la proteína CCNB1. Como resultado, la división celular se ralentizó, más células quedaron atrapadas en el punto de control G2/M y aumentó la apoptosis. En ratones implantados con células de cáncer colorrectal, el tratamiento diario con micafungina redujo significativamente el tamaño de los tumores en comparación con animales no tratados, sin necesidad de eliminar UBE2M por completo.
Qué significa esto para los pacientes a largo plazo
Este trabajo ofrece una imagen clara de cómo una sola enzima, UBE2M, puede enlazar un sistema sutil de etiquetado proteico con la decisión de una célula de cáncer intestinal de dividirse. Al estabilizar un factor de traducción (PABPC1) a través de USP39, UBE2M eleva indirectamente los niveles de un potente impulsor del ciclo celular, CCNB1, permitiendo que los tumores crezcan más rápido. Aunque hacen falta más investigaciones y ensayos clínicos, los hallazgos sugieren que bloquear este relevo—potencialmente con fármacos reposicionados como la micafungina—podría ofrecer una nueva estrategia dirigida para frenar la progresión del cáncer colorrectal y mejorar los resultados en los pacientes.
Cita: Wang, Z., Wang, Y., Chen, Y. et al. UBE2M as a bridge spanning neddylation and cell cycle regulation in colorectal adenocarcinoma. Exp Mol Med 58, 501–518 (2026). https://doi.org/10.1038/s12276-026-01636-z
Palabras clave: cáncer colorrectal, ciclo celular, neddilación, UBE2M, terapia dirigida