Clear Sky Science · es
CDK13 impulsa el carcinoma de células renales claras mediante la modificación m6A del ARNm de ACLY mediada por METTL16
Por qué importan los tumores renales llenos de grasa
El cáncer renal de células claras suele verse pálido y aceitoso al microscopio porque sus células están repletas de lípidos. Esa apariencia inusual no es solo cosmética; refleja una reorganización profunda de cómo estas células cancerosas manejan el combustible. Este estudio plantea una pregunta sencilla pero importante: ¿qué interruptor molecular indica a las células tumorales renales que acumulen grasa, y puede apagarse ese interruptor para frenar la enfermedad?
Un director oculto del crecimiento tumoral
Los investigadores se centraron en una proteína llamada CDK13, parte de una familia de enzimas que normalmente ayudan a las células a dividirse. Al analizar grandes conjuntos de datos de pacientes y muestras tumorales, encontraron que los niveles de CDK13 son consistentemente más altos en los cánceres renales de células claras que en el tejido renal normal. Los pacientes cuyos tumores mostraban más CDK13 tendían a presentar cánceres más grandes, más avanzados y con peores resultados. Cuando el equipo redujo CDK13 en líneas celulares de cáncer renal, las células crecieron más despacio y tuvieron dificultades para avanzar en el ciclo celular, lo que sugiere que CDK13 actúa como un director oculto que coordina tanto el crecimiento como la supervivencia.
De azúcar a grasa: reprogramando la fábrica de combustible celular
Dado que los tumores renales de células claras están llenos de lípidos, el equipo examinó si CDK13 también controla cómo estas células sintetizan grasa. Mediante una combinación de perfilado de expresión génica y tinciones microscópicas de lípidos, mostraron que aumentar CDK13 incrementa la acumulación de gotas lipídicas dentro de las células cancerosas, mientras que reducir CDK13 produce el efecto contrario. CDK13 influyó de forma notable en una enzima llamada ACLY, que convierte un intermediario metabólico común en acetil-CoA, el material de partida para la síntesis de ácidos grasos y colesterol. Altos niveles de CDK13 iban de la mano con altos niveles de ACLY en los tumores de pacientes, y ambas proteínas se concentraban en las mismas regiones del tejido tumoral. Cuando ACLY se aumentó de forma artificial, rescató muchas de las deficiencias de crecimiento y almacenamiento de grasa causadas por la pérdida de CDK13, situando a ACLY como un efector clave aguas abajo de esta vía. 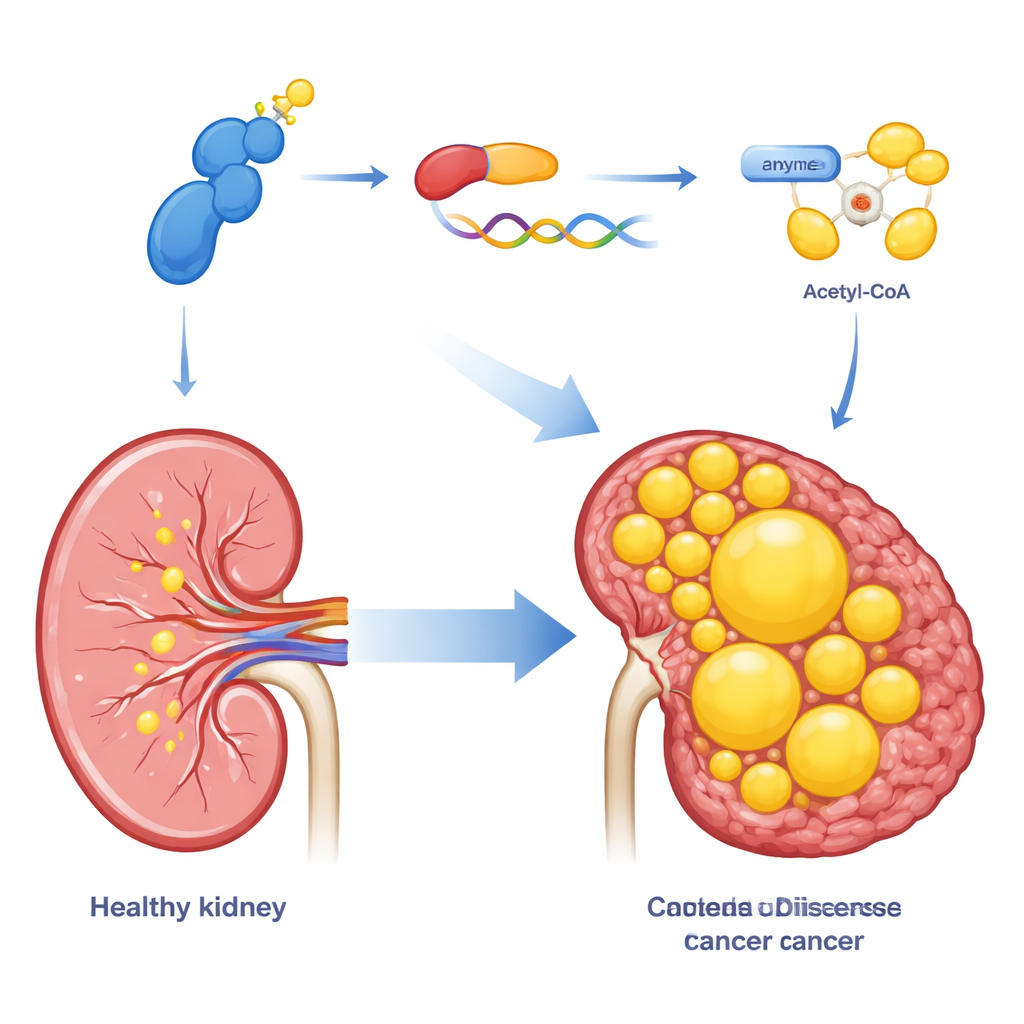
Un sistema de mensajes en capas dentro de las células cancerosas
En lugar de actuar directamente sobre ACLY como un simple interruptor, CDK13 ejerce su influencia a través de un sistema de mensajes en capas basado en el ARN, la molécula que transporta las instrucciones genéticas del ADN a las fábricas de proteínas. Los autores descubrieron que CDK13 se une físicamente y modifica químicamente a otra enzima, METTL16, que marca con pequeños grupos metilo mensajes de ARN específicos. CDK13 añade una etiqueta de fosfato a METTL16 en un punto preciso, haciendo a METTL16 más activa. A su vez, METTL16 coloca marcas metilo adicionales en el ARN que codifica ACLY. Estas marcas no cambian el código genético en sí, pero alteran cómo la célula maneja ese mensaje. Una tercera proteína, YTHDC2, reconoce el ARN de ACLY marcado y lo protege de la degradación, permitiendo que se produzca más proteína ACLY con el tiempo. Esta cascada—CDK13 activando METTL16, METTL16 marcando el ARN de ACLY y YTHDC2 protegiendo ese mensaje marcado—crea un impulso potente para impulsar la síntesis de grasa. 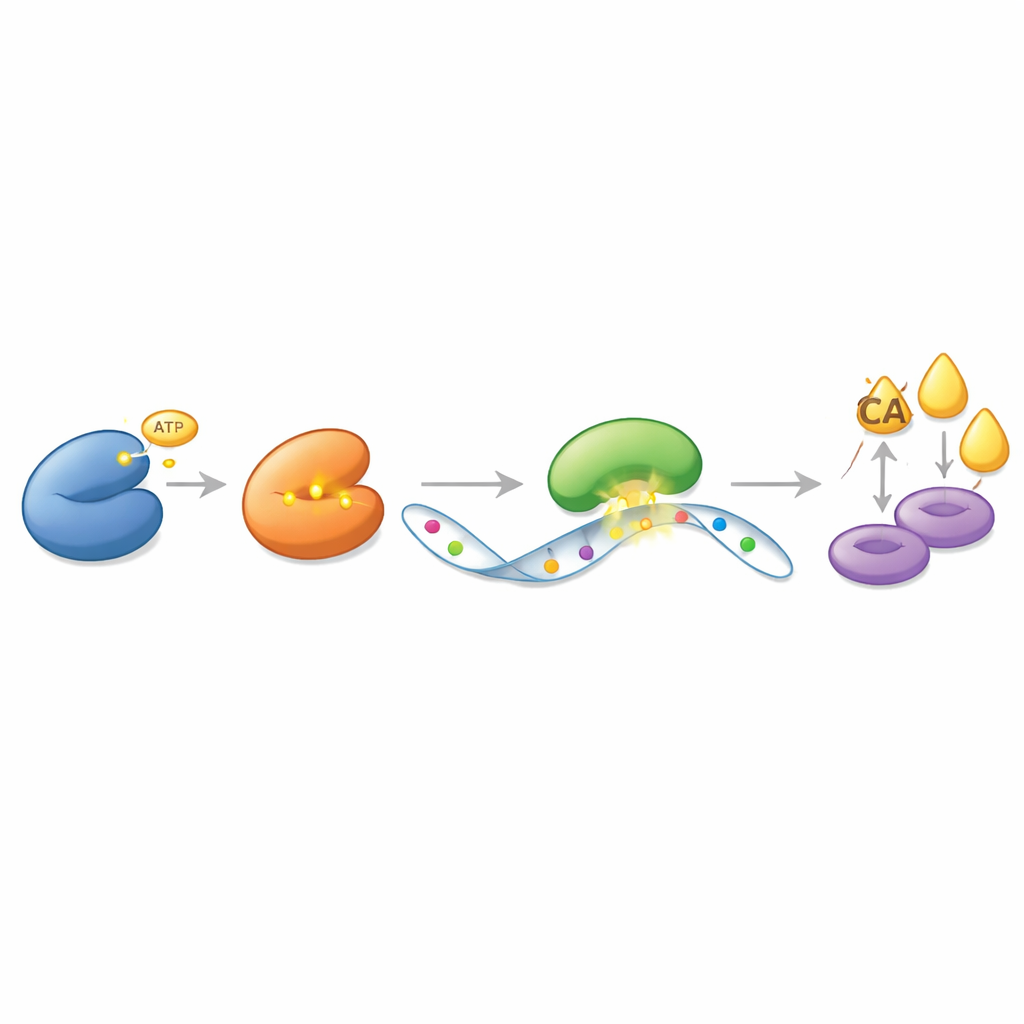
Poniendo a prueba la cadena en células, ratones y muestras de pacientes
La solidez del trabajo radica en lo exhaustivo de las pruebas de esta cadena de acontecimientos. En células de cáncer renal cultivadas, interrumpir cualquier parte de la vía CDK13–METTL16–ACLY redujo las gotas lipídicas y frenó la proliferación. En ratones implantados con células humanas de cáncer renal, bloquear CDK13 o ACLY por separado hizo que los tumores se redujeran y disminuyeron las reservas de grasa en su interior, mientras que bloquear ambos juntos tuvo un efecto aún más potente. El equipo también usó un compuesto de pequeña molécula, 1NM-PP1, que inhibe la actividad de CDK13. Este agente tipo fármaco redujo la etiqueta activadora en METTL16, bajó los niveles de ACLY y suprimió el crecimiento tumoral, especialmente cuando se combinó con la depleción de METTL16. En los conjuntos de datos de pacientes, CDK13, METTL16 y ACLY tendieron a aumentar y disminuir juntos, reforzando la idea de que este eje está activo en cánceres reales, no solo en modelos de laboratorio.
Qué podría significar esto para tratamientos futuros
Para no especialistas, el mensaje clave es que este estudio expone un nuevo control para la «fábrica de grasa» dentro de los tumores renales de células claras. En lugar de dirigirse únicamente a las enzimas que producen lípidos, los investigadores revelan una cadena de mando de nivel superior que estabiliza las instrucciones para esas enzimas. Al interrumpir el eje CDK13–METTL16–ACLY, podría ser posible privar a los tumores de las grasas que necesitan para crecer y diseminarse, al tiempo que las células normales resultan menos afectadas. Aunque el trabajo sigue siendo preclínico y 1NM-PP1 aún no es un fármaco para el cáncer renal, los hallazgos apuntan a nuevas estrategias que combinan inhibidores de quinasas con fármacos dirigidos a enzimas modificadoras de ARN, ofreciendo una manera más precisa de tratar esta forma de cáncer renal impulsada por el metabolismo.
Cita: Chen, J., Liu, H., Zhang, Y. et al. CDK13 drives clear cell renal carcinoma through METTL16-mediated m6A modification of ACLY mRNA. Exp Mol Med 58, 472–486 (2026). https://doi.org/10.1038/s12276-025-01634-7
Palabras clave: carcinoma de células renales claras, metabolismo de lípidos, CDK13, metilación de ARN, ACLY