Clear Sky Science · es
El factor regulador de interferón 5 participa en la patogénesis del enfisema a través de NLRP3 y células que expresan Ly6C
Por qué importa este estudio pulmonar
La enfermedad pulmonar obstructiva crónica (EPOC) y el enfisema privan de aliento a millones de personas, a menudo mucho después de dejar de fumar. Los medicamentos actuales pueden ayudar a abrir las vías respiratorias, pero hacen poco para calmar la inflamación latente que sigue devorando los pulmones. Este estudio descubre a un “cabecilla” molecular de ese daño, lo que sugiere una nueva vía para proteger los frágiles sacos alveolares y frenar el deterioro de la función pulmonar.
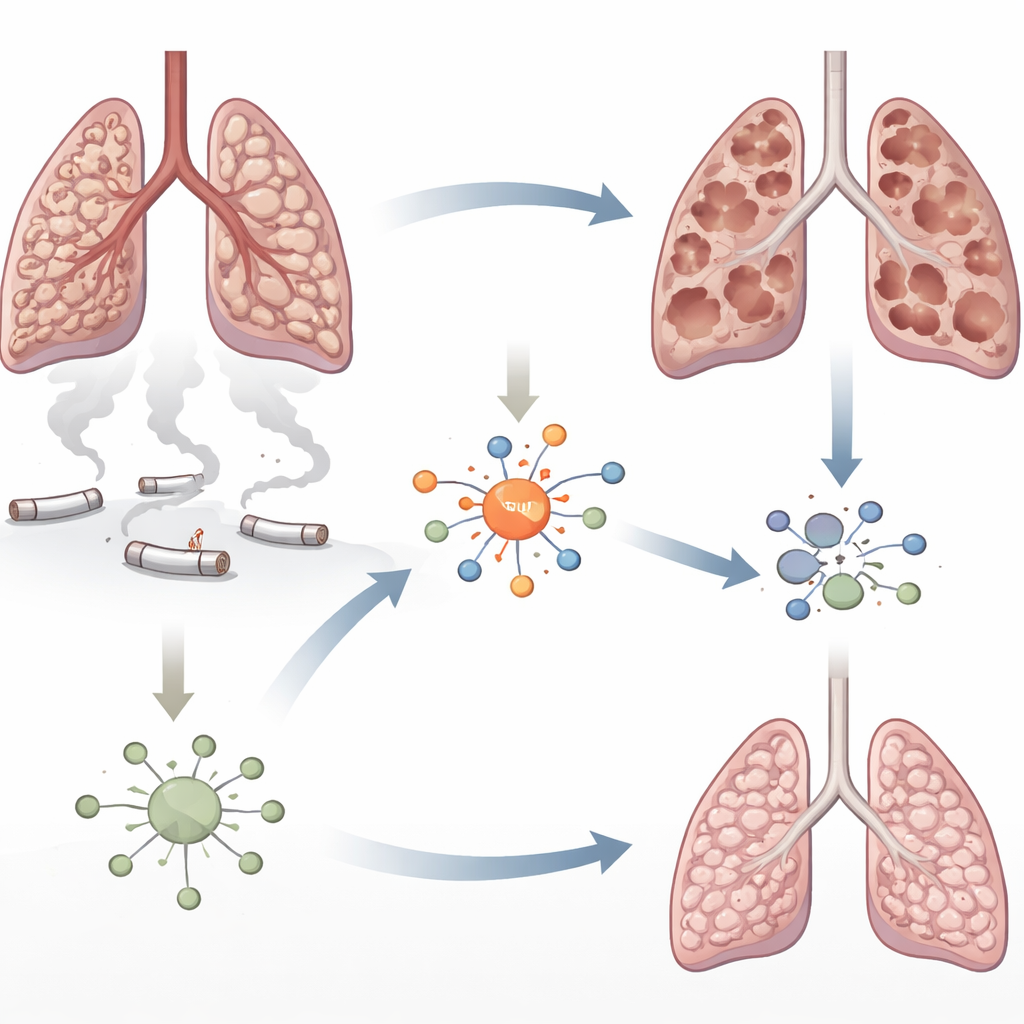
Una mirada más cercana a los pulmones dañados por el humo
El enfisema se caracteriza por la destrucción gradual de los diminutos sacos de aire que intercambian oxígeno y dióxido de carbono. El humo de cigarrillo baña los pulmones con partículas tóxicas que lesionan las células y atraen oleadas de células inmunitarias. Los autores se centraron en una proteína llamada factor regulador de interferón 5 (IRF5), conocida por impulsar la inflamación en enfermedades autoinmunes pero poco estudiada en la EPOC. Trabajos anteriores sugerían que los niveles de IRF5 aumentan en pulmones expuestos al humo. Aquí, los investigadores buscaron determinar si IRF5 simplemente acompaña a la inflamación o si realmente contribuye a la destrucción del tejido pulmonar.
Apagar un interruptor clave en ratones
Para sondear el papel de IRF5, el equipo diseñó ratones que carecen por completo del gen de esta proteína. Luego expusieron animales normales y deficientes en IRF5 al humo de cigarrillo durante varias semanas y compararon el estado de sus pulmones. En los ratones normales, el humo provocó signos claros de enfisema: se perdieron las paredes entre sacos de aire vecinos, dejando espacios grandes y sobredistendidos. En contraste, los ratones sin IRF5 estuvieron en gran medida protegidos de este daño estructural, aunque el humo siguió atrayendo células inmunitarias a los espacios aéreos y elevó muchas moléculas inflamatorias. Esto apuntó a IRF5 como un vínculo crucial entre la exposición al humo y la destrucción efectiva de la arquitectura pulmonar.
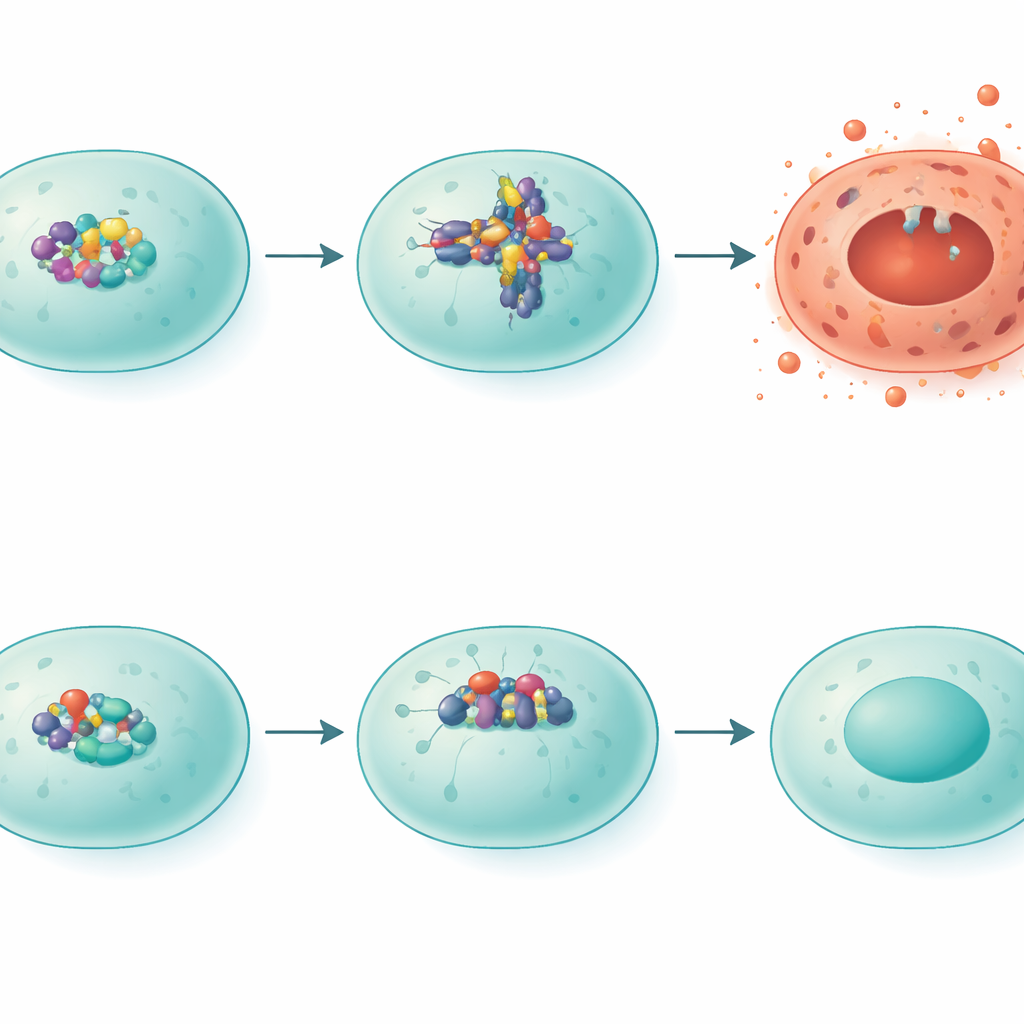
Cómo IRF5 empuja a las células hacia una muerte ardiente
Los investigadores profundizaron en una forma particular de muerte celular violenta llamada piroptosis, que perfora las membranas celulares y derrama contenidos inflamatorios en el tejido circundante. Un complejo proteico conocido como NLRP3 está en el centro de este proceso. En ratones normales expuestos al humo, los niveles de NLRP3 aumentaron, y los patrones de otra proteína, gasdermina D, coincidieron con un estado similar a la piroptosis. En los ratones deficientes en IRF5, los niveles de NLRP3 fueron mucho más bajos y la gasdermina D se fragmentó en formas alternativas asociadas con resultados menos destructivos. Cuando el equipo aumentó artificialmente IRF5 en células relacionadas con el pulmón en el laboratorio, los niveles de NLRP3 subieron, confirmando que IRF5 actúa como un interruptor transcripcional que enciende esta vía dañina.
Células inmunitarias protectoras entran en escena
IRF5 también remodeló la composición de las células inmunitarias en el pulmón. En ratones sin IRF5, hubo un aumento notable en un subconjunto de células procedentes de la sangre, marcadas fuertemente por una molécula de superficie llamada Ly6C. Estas células Ly6C‑altas incluían tanto monocitos como células T y aparecieron en mayor número tras la exposición al humo. Cuando los científicos purificaron células Ly6C‑altas de ratones deficientes en IRF5 y las infundieron en animales normales expuestos al humo, los recipientes desarrollaron menos destrucción de los sacos de aire y mostraron niveles reducidos de NLRP3 en el pulmón. Experimentos adicionales revelaron que IRF5 reprime directamente la actividad del gen Ly6C, lo que sugiere que cuando IRF5 está presente, se producen o mantienen menos de estas células potencialmente protectoras.
Los pulmones humanos confirman la señal
Para comprobar si estos hallazgos podrían ser relevantes en humanos, los autores examinaron tejido pulmonar de pacientes sometidos a cirugía por cáncer de pulmón. Compararon muestras de individuos con buena capacidad de intercambio gaseoso con aquellas de personas con enfisema significativo. Los niveles de proteína IRF5 fueron sustancialmente más altos en los pulmones del grupo con enfisema. Aunque este estudio no fue lo suficientemente grande como para vincular IRF5 con precisión a la gravedad de los síntomas o a las exacerbaciones, el patrón coincidió con los hallazgos en ratones: más IRF5 en pulmones enfermos, menos en los más sanos.
Qué podría significar esto para tratamientos futuros
En conjunto, el trabajo pinta a IRF5 como un coordinador central del daño pulmonar inducido por el humo. Potencia un motor de muerte celular centrado en NLRP3 y orienta a las células inmunitarias fuera de las poblaciones Ly6C‑altas que parecen ayudar a preservar la estructura de los sacos de aire. Para los pacientes, la implicación es directa: un fármaco que rebaje la actividad de IRF5 podría, en teoría, reducir las formas más destructivas de inflamación sin apagar por completo el sistema inmunitario. Aunque tales terapias aún no existen para la EPOC, este estudio proporciona un objetivo molecular claro y una vía biológica plausible hacia tratamientos que hagan más que abrir vías respiratorias estrechadas: podrían proteger realmente el delicado armazón del pulmón.
Cita: Heo, SH., Park, S.Y., Kim, N.H. et al. Interferon regulatory factor 5 involves the pathogenesis of emphysema through NLRP3 and Ly6C expressing cells. Exp Mol Med 58, 425–435 (2026). https://doi.org/10.1038/s12276-025-01632-9
Palabras clave: enfisema, EPOC, inflamación, inmunidad pulmonar, muerte celular