Clear Sky Science · de
Ganzfeldige, hochauflösende Fourier-Ptychographie mit neuraler Pupillen-Optimierung
Scharfere Ansichten über das gesamte Präparat
Moderne Mikroskope können erstaunliche zelluläre Details sichtbar machen — meist jedoch nur in einem kleinen, optimalen Bereich nahe der Bildmitte. An den Rändern eines großen Gewebeschnitts verwischen feine Strukturen häufig und treten zurück, sodass Ärzte und Forscher den Beobachtungen weniger vertrauen können. Diese Arbeit stellt eine neue Methode vor, um ein leistungsfähiges Bildgebungsverfahren, die Fourier-ptychographische Mikroskopie, näher an seine theoretischen Grenzen zu bringen und über ein weites Sichtfeld hinweg scharfe Details zu liefern, ohne das Mikroskop neu aufbauen zu müssen.
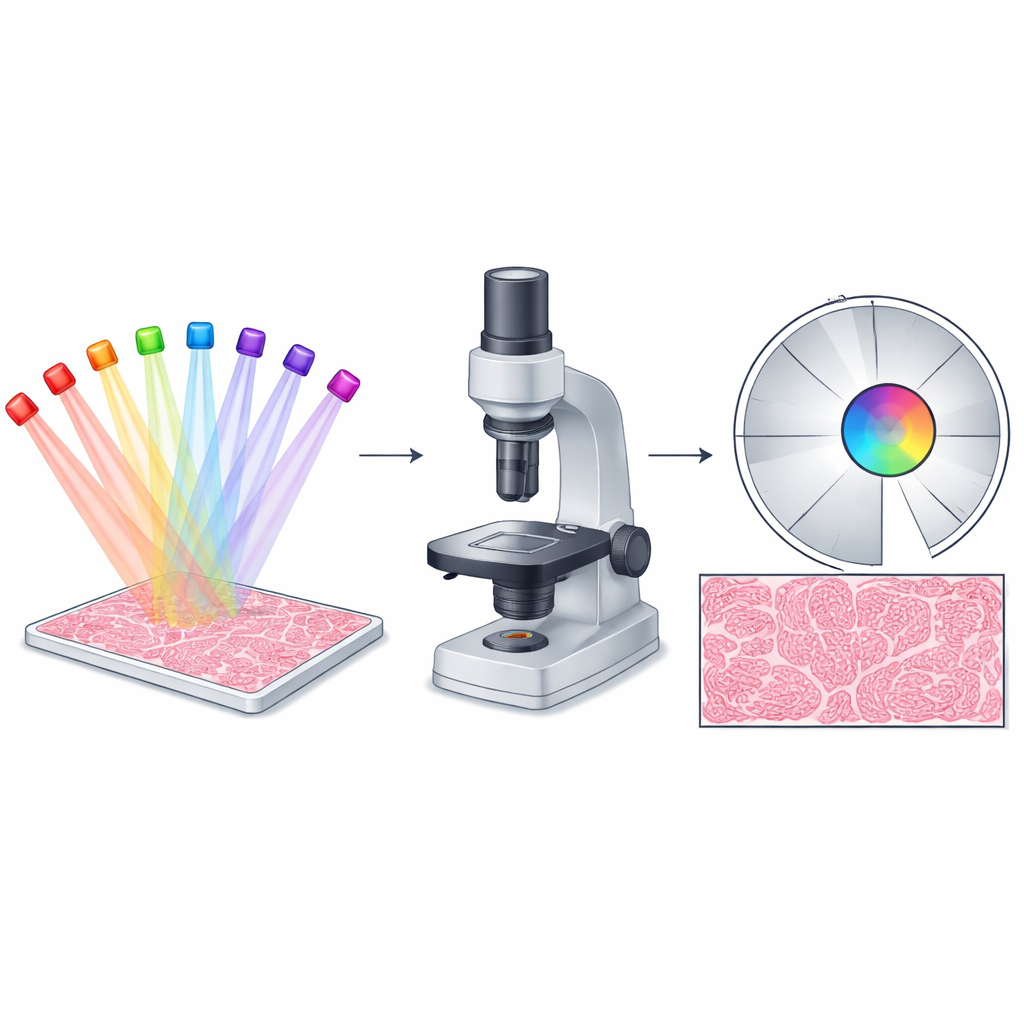
Warum Mikroskope an den Rändern Probleme haben
Die Fourier-ptychographische Mikroskopie (FPM) arbeitet, indem sie ein Objekt aus vielen verschiedenen Winkeln beleuchtet und die entstehenden niedrigauflösenden Aufnahmen rechnerisch zu einem einzigen hochauflösenden Bild kombiniert. Prinzipiell sollte diese Strategie Bilder erzeugen, die sowohl sehr scharf als auch sehr großflächig sind — ideal für Ganzpräparate-Pathologie, Live-Zellstudien und industrielle Inspektion. In der Praxis liefert FPM jedoch meist nur in der optischen Mitte optimale Ergebnisse. Weiter außen brechen Linsenunvollkommenheiten und die gekrümmten Wellenfronten der LED-Beleuchtung eine vereinfachende Annahme, dass das Abbildungssystem überall gleich funktioniert. Dadurch zeigen die Randbereiche Artefakte, Kontrastverluste und fehlende feine Details, obwohl die Bildmitte ausgezeichnet aussieht.
Eine intelligente, formwandelnde Blende
Der Kern des Problems liegt darin, wie FPM typischerweise mit der Pupillenfunktion des Mikroskops umgeht — einem optischen „Fenster“, das festlegt, welche Teile der räumlichen Frequenzen durchgelassen werden. Standard-FPM behandelt dieses Fenster als festen, zentrierten Kreis in einem mathematischen Raum der räumlichen Frequenzen. Die Autoren beobachteten, dass im realen Experiment insbesondere in Bereichen abseits der Mitte das effektive Fenster leicht verschoben ist. Anstatt ein komplizierteres physikalisches Modell von Hand zu entwickeln, ließen sie ein neuronales Netzwerk lernen, wie sich dieses Fenster verschieben sollte. Ihr Ansatz, genannt neural pupil engineering FPM (NePE-FPM), stellt die Pupille als kontinuierliche Funktion dar, codiert durch ein kleines neuronales Netzwerk und eine mehrstufige Hash-Tabelle. Diese Struktur erlaubt es der Pupille, während der Rekonstruktion glatt im Frequenzraum zu rutschen, sodass der Algorithmus sich an off-axis Verhalten anpassen kann, ohne zusätzliche, schwer messbare Systemparameter einzuführen.
Klarere Zellen und schärfere Muster
Um ihre Methode zu testen, bildeten die Forscher Pflanzenwurzelgewebe und standardisierte Auflösungsziele ab. Im Vergleich zur konventionellen FPM mit fester Pupille erzeugte NePE-FPM an den Feldrändern deutlich schärfere Zellgrenzen und höheren Bildkontrast. Quantitative Tests zeigten in manchen Bereichen Verbesserungen des Kontrasts von bis zu etwa 55 %, wobei einzelne gefärbte Zellen dort deutlich unterscheidbar wurden, wo sie zuvor verschwommen waren. Auf einem öffentlich verfügbaren Auflösungsziel, das FPM besonders herausfordert, hatten konkurrierende Algorithmen Schwierigkeiten, sowohl Amplitude als auch Phase genau wiederherzustellen, wenn die Krümmung der Beleuchtung wichtig war. NePE-FPM dagegen bewahrte feine Streifenmuster und lieferte genauere Phasenabbildungen — eine Schlüsselanforderung für quantitative, kennzeichnungsfreie Bildgebung.
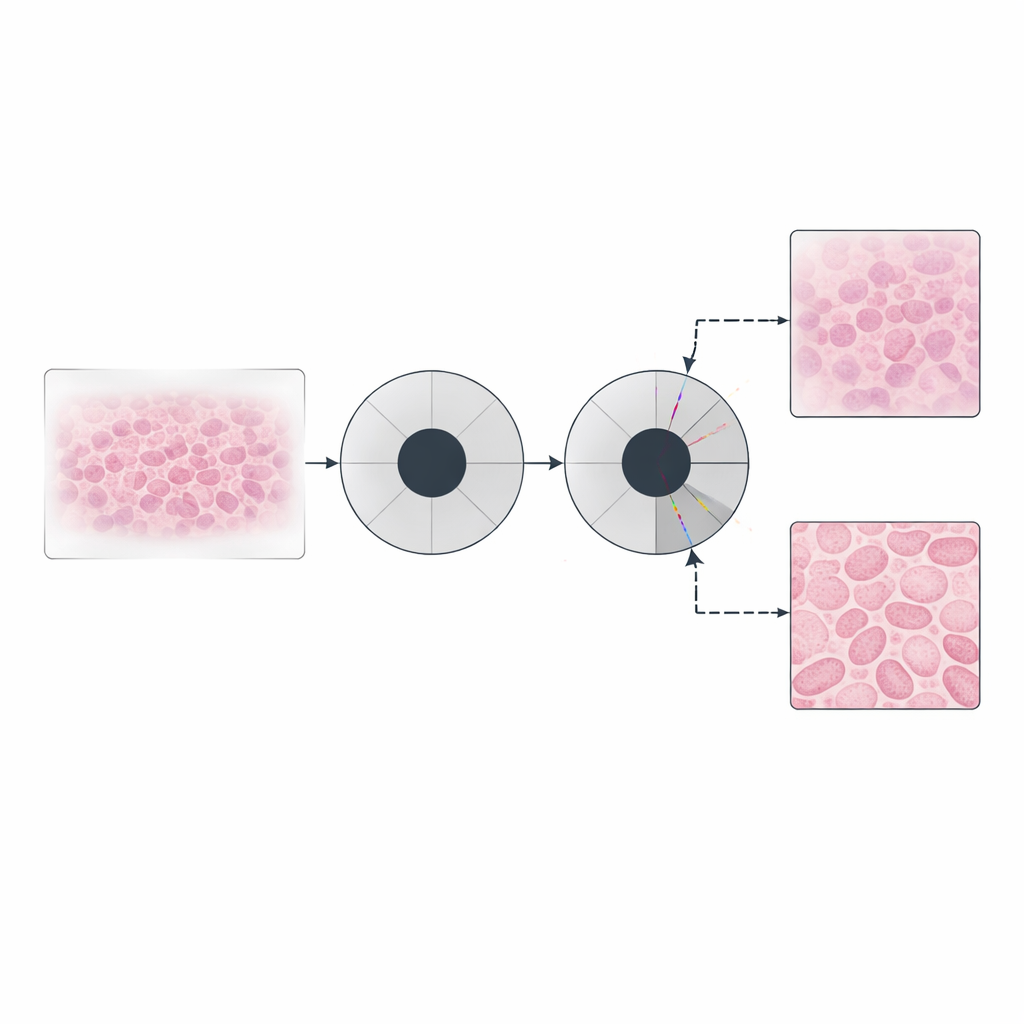
Gleichzeitig Probe und Optik lernen
Die Autoren gingen noch weiter und ließen neuronale Netze nicht nur die verschiebbare Pupille, sondern auch die Probe selbst repräsentieren. In diesem „doppelt impliziten“ Schema kodiert ein Netzwerk, wie die Probe das Licht modifiziert, während ein anderes Netzwerk beschreibt, wie sich das optische Fenster über die Frequenzen verhält. Sorgfältig gewählte Aktivierungsfunktionen sorgen dafür, dass Amplitude und Phase physikalisch realistisch bleiben. Diese kontinuierliche, koordinatenbasierte Beschreibung wirkt wie ein intelligenter Filter: Sie glättet Rauschen natürlich, während echte Übergänge erhalten bleiben, und vermeidet die blockartigen Artefakte, die auftreten können, wenn traditionelle Methoden stark auf bestimmte Regularisierungen angewiesen sind. Tests an Gewebeschnitten zeigten glattere, sauberere Phasenbilder mit verbessertem Kontrast, bei gleichzeitiger Übereinstimmung mit den zugrundeliegenden quantitativen Werten.
Beschleunigung für den praktischen Einsatz
Da Ganzpräparate-Bildgebung große Datensätze erfordert, ist Geschwindigkeit wichtig. NePE-FPM wurde mit Blick auf Effizienz entwickelt. Die mehrstufige Hash-Codierung erlaubt es, die neuronale Repräsentation in konstanter Zeit abzufragen, und die Autoren implementierten eigene CUDA-Routinen, um die rechnerisch intensiven Schritte auf einer Grafikkarte auszuführen. Für typische Datensätze mit Millionen von Pixeln und Dutzenden Beleuchtungswinkeln sanken die Rekonstruktionszeiten auf einige Dutzend Sekunden — etwa fünfzehnmal schneller als vergleichbare CPU-basierte Implementierungen — und erzielten zugleich große Auflösungsgewinne über das gesamte Feld.
Theorie und Praxis näher zusammenbringen
Einfach ausgedrückt lehrt diese Arbeit das „Fenster“ des Mikroskops, sich dorthin zu bewegen, wo es gebraucht wird, anstatt es in einem zu starren Modell festzuhalten. Indem ein kompakter neuronaler Netzwerk-Ausdruck kontinuierlich anpasst, wie Licht im Frequenzraum gefiltert wird, stellt NePE-FPM feine zelluläre Details gleichmäßig über große Flächen wieder her, verringert die Lücke zwischen dem, was FPM theoretisch verspricht, und dem, was es im Labor liefert, und das bei praktischen Geschwindigkeiten. Für Anwendungen wie digitale Pathologie oder Hochdurchsatz-Inspektion bietet es einen Weg zu Gigapixel-Bildern, bei denen die Ränder endlich so vertrauenswürdig sind wie die Mitte.
Zitation: Shuhe Zhang and Liangcai Cao, "Whole-field, high-resolution Fourier ptychography with neural pupil engineering," Optica 12, 1615-1624 (2025). https://doi.org/10.1364/OPTICA.575065
Schlüsselwörter: Fourier-ptychographische Mikroskopie, computationales Imaging, neuronale Pupillen-Optimierung, quantitative Phasenbildgebung, Ganzpräparate-Mikroskopie