Clear Sky Science · de
Ultrasensible Nachweis von Alzheimer-Biomarkern mit nanopillaren Photonic-Crystal-Biosensoren
Warum ein einfacher Bluttest bei Gedächtnisstörungen wichtig ist
Da neue Medikamente verfügbar werden, die das Fortschreiten der Alzheimer‑Krankheit verlangsamen können, benötigen Ärztinnen und Ärzte dringend einfache Tests, die anzeigen, wer lange vor dem Auftreten klarer Symptome gefährdet ist. Heute bedeutet die Bestätigung von Alzheimer meist teure Hirnscans oder Lumbalpunktionen, die in der Routineversorgung nur selten durchgeführt werden. Diese Studie beschreibt einen winzigen, lichtbasierten Sensor, der Alzheimer-assoziierte Moleküle in einem Tropfen Blut in klinisch relevanten Konzentrationen nachweisen kann und damit den Weg für schnelle, kostengünstige Tests ebnen könnte, die in der Praxis oder sogar am Krankenbett eingesetzt werden können.
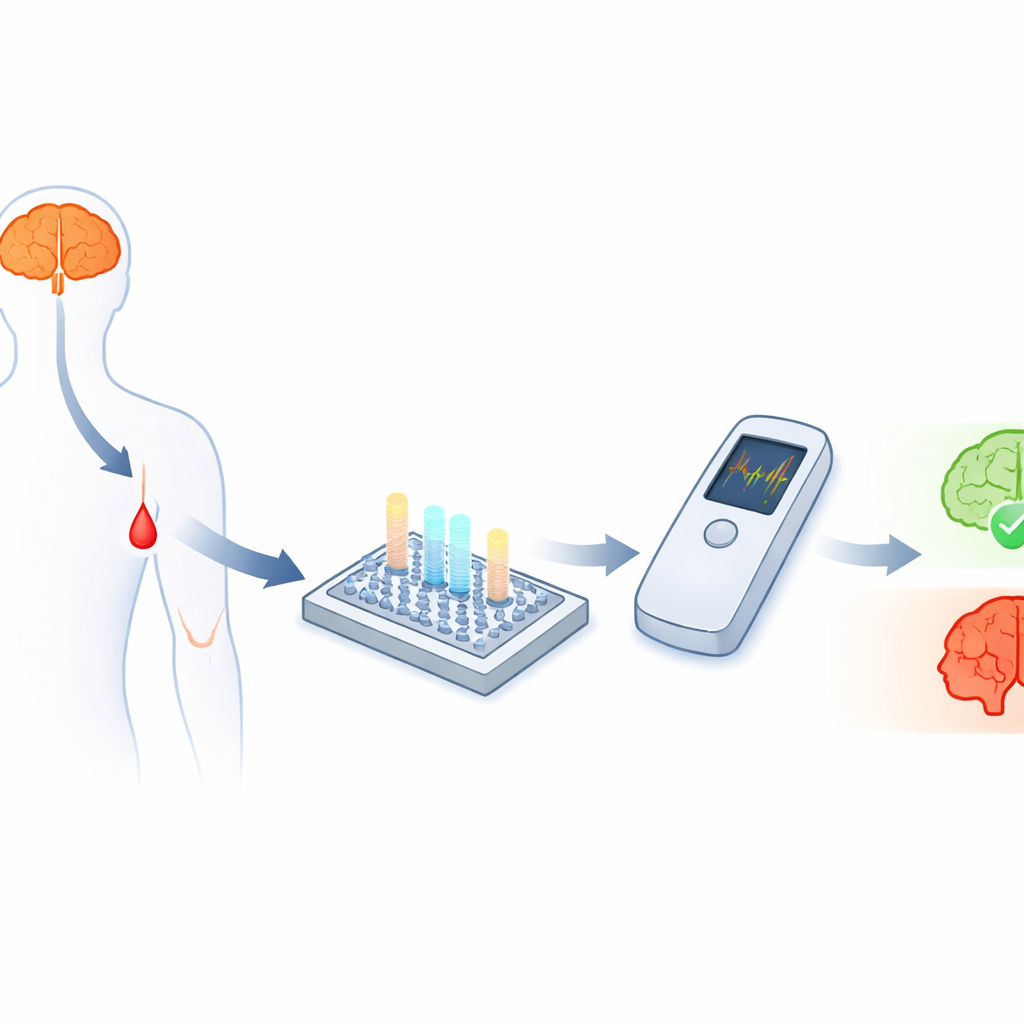
Auf der Suche nach Hinweisen im Blut
Die Alzheimer‑Krankheit hängt eng mit kleinen Proteinfragmenten zusammen, den Amyloid‑beta‑Peptiden, insbesondere den beiden Formen Aβ40 und Aβ42. Ihre Mengen und vor allem ihr Verhältnis liefern wichtige Hinweise darauf, ob die Krankheit vorliegt und wie sie sich entwickelt. Das Problem ist, dass diese Fragmente sehr klein sind und im Blut in extrem niedrigen Konzentrationen zirkulieren — Billionstel Gramm pro Milliliter —, wodurch sie außerhalb spezialisierter Labors nur schwer genau zu messen sind. Zwar können elektrochemische Sensoren solche niedrigen Konzentrationen prinzipiell erfassen, aber sie in robuste, kostengünstige Point‑of‑Care‑Tests zu verwandeln, die mehrere Biomarker gleichzeitig verfolgen, hat sich als schwierig erwiesen.
Lichtführung durch winzige Säulen
Das Team ging die Herausforderung mit Nanophotonik an — Strukturen, die Licht auf einer Skala steuern, die kleiner ist als die Wellenlänge des Lichts. Sie bauten einen Chip, der mit einem regelmäßigen Gitter aus gepaarten, haarfeinen Siliziumsäulen auf Glas bedeckt ist. Wenn Licht auf diese strukturierte Oberfläche trifft, wird es in einem speziellen Resonanzmodus gefangen, der extrem empfindlich auf Veränderungen in der Nähe der Säulenspitzen reagiert, ähnlich wie sich der Ton einer Stimmgabel verschiebt, wenn Material hinzugefügt wird. Durch die sorgfältige Anpassung des Abstands zwischen den Säulen in jedem Paar konnten die Forschenden drei wichtige Eigenschaften gleichzeitig ausbalancieren: wie scharf die optische Resonanz ist, wie stark sie auf ihre Umgebung reagiert und wie groß das erzeugte Signal ist. Dieses Design des „sweet spot“ macht den Chip besonders geeignet zum Nachweis sehr kleiner Materialmengen.
Unsichtbare Moleküle sichtbar machen
Selbst mit diesem optimierten Design würden die Alzheimer‑Marker allein das Licht kaum stören. Um den Effekt zu verstärken, verwendeten die Forschenden eine Sandwich‑Strategie mit Goldnanopartikeln. Zunächst beschichteten sie die Sensoroberfläche mit haftender Chemie, die spezialisierte Antikörper korrekt ausrichtet, sodass ihre Bindungsstellen in die Flüssigkeit zeigen. Diese Antikörper binden entweder Aβ40 oder Aβ42 aus der Probe. Anschließend werden Goldnanopartikel, die jeweils mit einem zweiten Antikörper versehen sind, der ein anderes Ende desselben Amyloidfragments erkennt, über den Chip gespült. Immer wenn ein Amyloidfragment vorhanden ist, überbrückt es die Oberfläche und ein Goldpartikel und „markiert“ so seine Anwesenheit. Da Gold die lokale optische Umgebung stark stört, erzeugt jedes eingefangene Fragment eine viel größere Verschiebung der Resonanz des Sensors als das Peptid allein, was die Empfindlichkeit um etwa ein bis zwei Größenordnungen erhöht und gleichzeitig ein klares optisches Signal erhält.
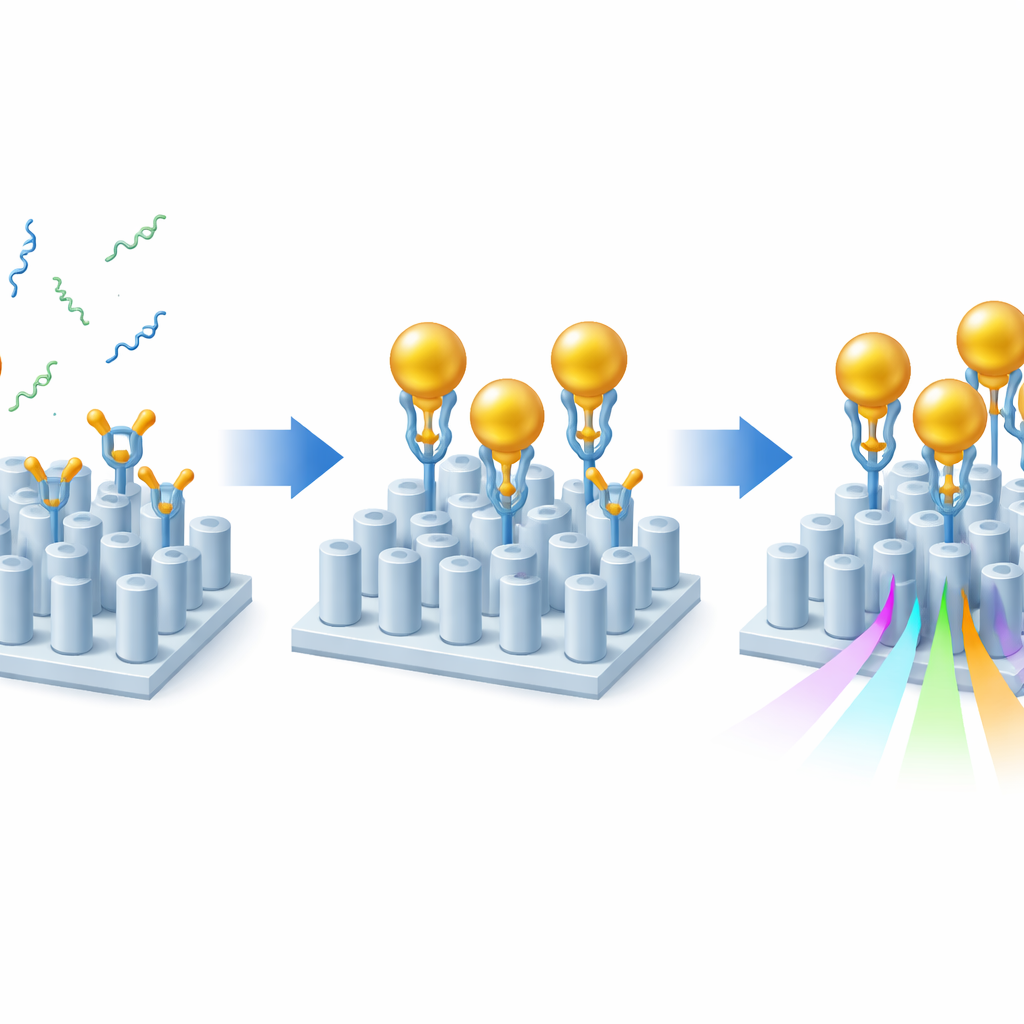
Tests mit realistischen Proben
Um zu zeigen, dass der Ansatz über einfache Laborpuffer hinaus funktioniert, testete das Team ihren Sensor mit menschlichem Blutserum. Sie verdünnten das Serum, um es mit mikrofluidischen Verfahren kompatibel zu machen, hielten jedoch die Amyloidspiegel repräsentativ für die bei Patientinnen und Patienten gefundenen Werte. Wichtig ist, dass sie sowohl Aβ40 als auch Aβ42 in dieser verdünnten Serumprobe bei 0,2 Pikogramm pro Milliliter nachweisen konnten — äquivalent zu dem klinisch relevanten Wert von 20 Pikogramm pro Milliliter im Vollblut. Durch das Aufbringen unterschiedlicher Capture‑Antikörper in separaten Regionen auf demselben Chip maßen sie beide Amyloidformen gleichzeitig in einem einzigen winzigen Kanal, ein entscheidender Schritt, um ihr Verhältnis aus einer einzigen kleinen Probe zu bestimmen. Die Signale unterschieden deutlich Proben, die zusätzliches Amyloid enthielten, von solchen mit nur den natürlich vorkommenden Hintergrundwerten, die selbst bei gesunden Personen zu finden sind.
Was das für die künftige Versorgung bedeuten könnte
Zusammengefasst zeigen diese Fortschritte, dass ein kompakter, lichtbasierter Sensor, verstärkt durch Goldnanopartikel, die für aussagekräftige Alzheimer‑Bluttests erforderlichen Empfindlichkeiten erreichen kann und dabei mehr als einen Biomarker gleichzeitig handhabt. Zwar sind weitere Arbeiten nötig, um daraus ein robustes kommerzielles Gerät zu machen und andere Marker wie verschiedene Formen des Tau‑Proteins hinzuzufügen, doch die zugrundeliegende Technologie besteht aus skalierbaren Materialien und lässt sich mit einfacher, tragbarer Optik kombinieren. Wenn sie vollständig entwickelt ist, könnte sie Klinikern erlauben, die Gehirngesundheit nur mit einer kleinen Blutprobe zu überwachen, was die Früherkennung von Alzheimer und die Verfolgung des Behandlungserfolgs über die Zeit deutlich erleichtern würde.
Zitation: Guilherme S. Arruda, Katie Morris, Augusto Martins, Yue Wang, Sian Sloan-Dennison, Duncan Graham, Steven D. Quinn, Emiliano R. Martins, and Thomas F. Krauss, "Ultrasensitive Alzheimer’s disease biomarker detection with nanopillar photonic crystal biosensors," Optica 12, 1587-1596 (2025). https://doi.org/10.1364/OPTICA.566672
Schlüsselwörter: Alzheimer-Bluttest, nanophotonischer Biosensor, Amyloid‑beta, Goldnanopartikel, Früherkennung