Clear Sky Science · de
Selektive Tumorablation mittels femtosekunden-Laser, der mit Kollagen resoniert
Licht als präzises Krebswerkzeug
Pankreaskrebs gehört zu den tödlichsten Krebserkrankungen, unter anderem weil er sich nur schwer entfernen lässt, ohne das empfindliche umgebende Organ zu schädigen. Diese Studie untersucht einen neuen Ansatz, ultrakurze Pulse unsichtbaren Infrarotlichts zu nutzen, um Bauchspeicheldrüsentumore präziser wegzubrennen, indem sie sich auf einen Strukturbestandteil konzentriert, den Tumore im Überschuss tragen. Die Arbeit deutet auf künftige Therapien hin, die mehr gesundes Gewebe schonen können, während sie den Krebs dennoch gezielt treffen.
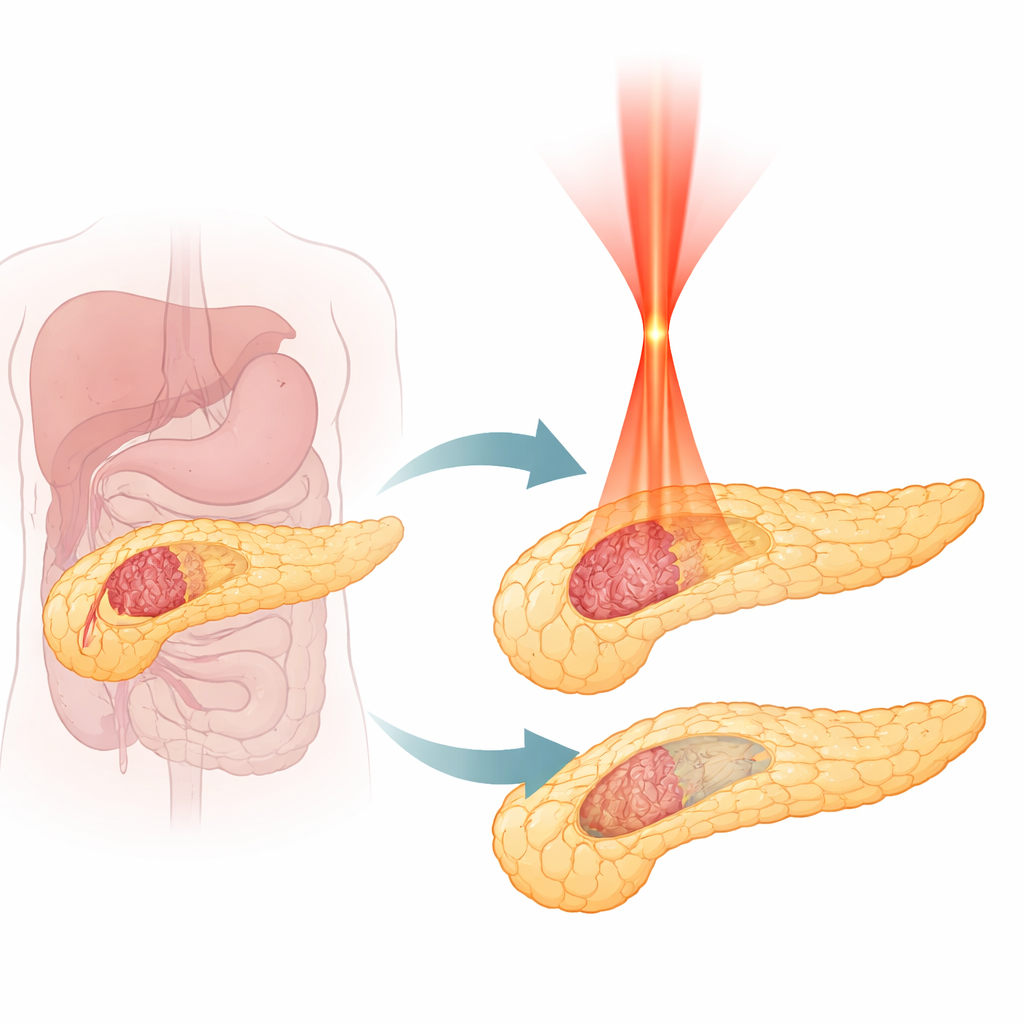
Warum Pankreastumore so schwer zu behandeln sind
Pankreaskarzinom des duktalen Typs, die häufigste Form von Pankreaskrebs, wächst aggressiv und wird oft spät entdeckt. Nur ein kleiner Teil der Patientinnen und Patienten ist operabel, und selbst moderne Chemotherapie und Strahlentherapie bringen nur begrenzten Nutzen. Wärmebasierte Verfahren, die Gewebe zerstören – etwa Radiofrequenz, Mikrowellen oder herkömmliche Laserablation – können Tumore verkleinern, verbrennen aber oft alles auf ihrem Weg. Weil die Bauchspeicheldrüse nahe an lebenswichtigen Blutgefäßen und empfindlichen Verdauungsstrukturen liegt, birgt eine Ausweitung der Behandlungszone ernsthafte Risiken. Ärztinnen und Ärzte brauchen daher eine Methode, die Tumorgewebe während der Zerstörung vom normalen Pankreas unterscheiden kann, statt nur ein breites Gebiet zu verkochen.
Eine verborgene Schwachstelle im Tumorgewebe finden
Die Autorinnen und Autoren konzentrierten sich auf einen grundlegenden physikalischen Unterschied zwischen Pankreastumoren und gesundem Pankreas: Tumoren sind voller steifer, faseriger Substanz mit hohem Kollagenanteil, während normales Gewebe weicher und lockerer ist. Anhand üblicher Gewebefärbungen und Elektronenmikroskopie an Proben aus Operationen zeigten sie, dass Krebsgewebe dichte Bündel von Kollagenfasern enthält, während das angrenzende gesunde Pankreas deutlich weniger aufweist. Mittels Infrarotspektroskopie maßen sie dann, wie stark diese Gewebe verschiedene Wellenlängen des mittleren Infrarots absorbieren. Beide Gewebe absorbieren bei ähnlichen Wellenlängen, doch Tumore zeigen einen deutlich stärkeren Peak nahe 6,1 Mikrometern, der mit Schwingungen von Kollagen korrespondiert. Das legt nahe, dass ein Laser, der genau auf diese Wellenlänge abgestimmt ist, Tumorgewebe effizienter erhitzen und abbauen könnte als normales Pankreas.
Ein Laser, der auf Kollagen abgestimmt ist
Um die Idee zu testen, bauten die Forschenden einen leistungsfähigen Laser im mittleren Infrarot, der ultrakurze Pulse aussendet – von nur wenigen hundert Billiardsteln einer Sekunde dauernd – mit Zentrum bei 6,1 Mikrometern. Diese „Femtosekunden“-Pulse begrenzen unerwünschte Wärmeausbreitung, ähnlich einer Serie winziger, kontrollierter Blitzschläge. Das System wandelt Licht eines hochleistungsfähigen Industrielasers mithilfe spezieller Kristalle in die gewünschte Wellenlänge um und kann mehr als ein Watt mittlere Leistung liefern; das ist ausreichend für praktische Gewebeablation. Die Forschenden entwickelten außerdem eine hohle Glasfaser, die dieses Licht entlang eines flexiblen Pfads leiten kann – ein wichtiger Schritt, um den Laser durch eine dünne Nadel in den Körper für minimalinvasive Eingriffe zu führen.
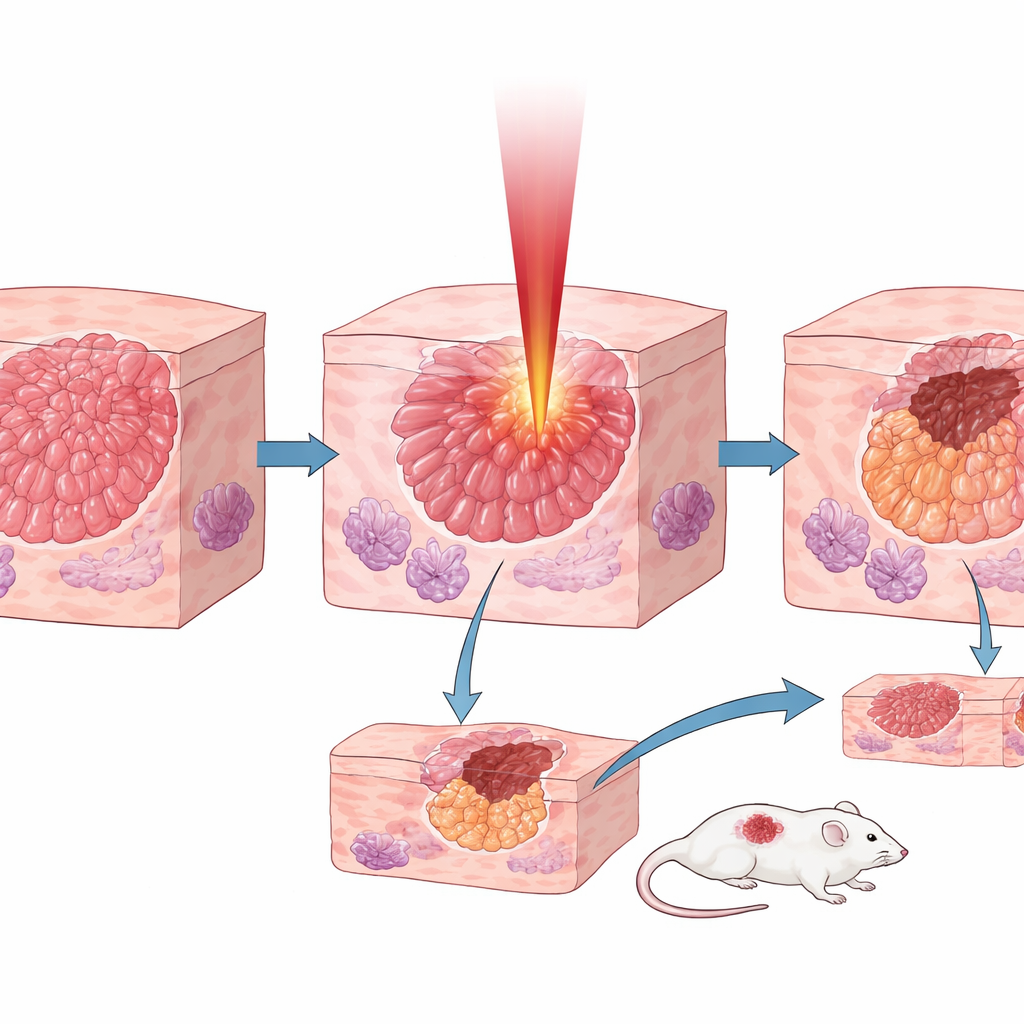
Selektivität in Zellen, Mäusen und menschlichem Gewebe testen
In Zellkulturen zweier Pankreaskrebszelllinien war der 6,1‑Mikrometer‑Laser deutlich tödlicher als Laser bei 1 oder 3 Mikrometern und reduzierte die Zellüberlebensrate innerhalb von Sekunden bis Minuten nach der Bestrahlung stark. In Mäusen mit subkutanen Pankreastumoren verglichen sie drei Wellenlängen. Obwohl der 1‑Mikrometer‑Strahl viel höhere Leistung trug, entfernte er nur flache Tumorschichten. Der kollagenabgestimmte 6,1‑Mikrometer‑Laser erzielte Ablationstiefen, die fünf- bis zehnmal größer waren, und verlangsamte das Tumorwachstum so stark, dass behandelte Tumore am Ende nur etwa ein Achtel der Größe unbehandelter Tumore erreichten. Am wichtigsten: Als das Team den 6,1‑Mikrometer‑Laser an menschlichen Tumorproben und angrenzendem gesundem Pankreas anwendete, waren die Einschnitte im Tumor unter gleichen Bedingungen zwei- bis dreimal tiefer als im gesunden Gewebe und zeigten damit echte Selektivität. Im Gegensatz dazu verschwand der Vorteil weitgehend, als sie eine andere Lebertumorart testeten, die nicht zusätzliches Kollagen anhäuft, was die zentrale Rolle des Kollagens unterstreicht. Schließlich zeigten sie, dass die hohle Faser denselben selektiven Effekt übertragen kann, was nadelbasierte Behandlungen unterstützt.
Was das für die künftige Krebsversorgung bedeuten könnte
Die Studie zeigt, dass sorgfältig abgestimmte Impulse des mittleren Infrarots einen materiellen Unterschied zwischen Tumoren und gesundem Gewebe ausnutzen können, um selektivere Zerstörung zu erreichen. Indem sie kollagenreiche Bereiche anvisieren, schneidet der 6,1‑Mikrometer‑Femtosekunden‑Laser tiefer in Pankreaskrebs und schont mehr vom umliegenden Organ. Obwohl die Arbeit noch experimentell ist und weitere Tests in realistischen Modellen und klinischen Umgebungen nötig sind, weist sie auf eine neue Klasse bildgeführter, fasergeführter Verfahren hin, die nicht nur Pankreastumore, sondern auch andere kollagenreiche Tumoren mit größerer Präzision und weniger Nebenwirkungen behandeln könnten.
Zitation: Dunxiang Zhang, Xing Huang, Xuemei Yang, Ning Xia, Kan Tian, Jinmiao Guo, Maoxing Xiang, Linzhen He, Zhizhuo Fu, Ang Deng, Han Wu, Yuxi Wang, Wonkeun Chang, Bole Tian, Junjie Xiong, Qi Jie Wang, Anderson S. L. Gomes, and Houkun Liang, "Selective tumor ablation via femtosecond laser resonant with collagen," Optica 12, 1578-1586 (2025). https://doi.org/10.1364/OPTICA.561337
Schlüsselwörter: Pankreaskrebs, Laserablation, Kollagen, mittleres Infrarot, minimalinvasive Chirurgie