Clear Sky Science · de
Die quartäre Struktur als Ursache der Fibrillation des Sichel-Hämoglobins: eine Studie mit Molekulardynamik
Warum diese Blutgeschichte wichtig ist
Sichelzellenkrankheit beginnt mit einer winzigen Veränderung eines Blutproteins, kann aber rote Blutkörperchen verformen, Gefäße verstopfen und lebenslange Schmerzen verursachen. Diese Studie blickt physikbasiert und detailliert darauf, wie diese einzelne Veränderung das Hämoglobin dazu bringt, sich innerhalb der Zelle zu starren Fasern zusammenzuschieben. Mithilfe fortgeschrittener Computersimulationen verbinden die Autorinnen und Autoren atomare Details mit Problemen auf Zellebene und liefern neue Hinweise darauf, wie künftige Medikamente verhindern könnten, dass Hämoglobin unsere Blutbahn verstopft.
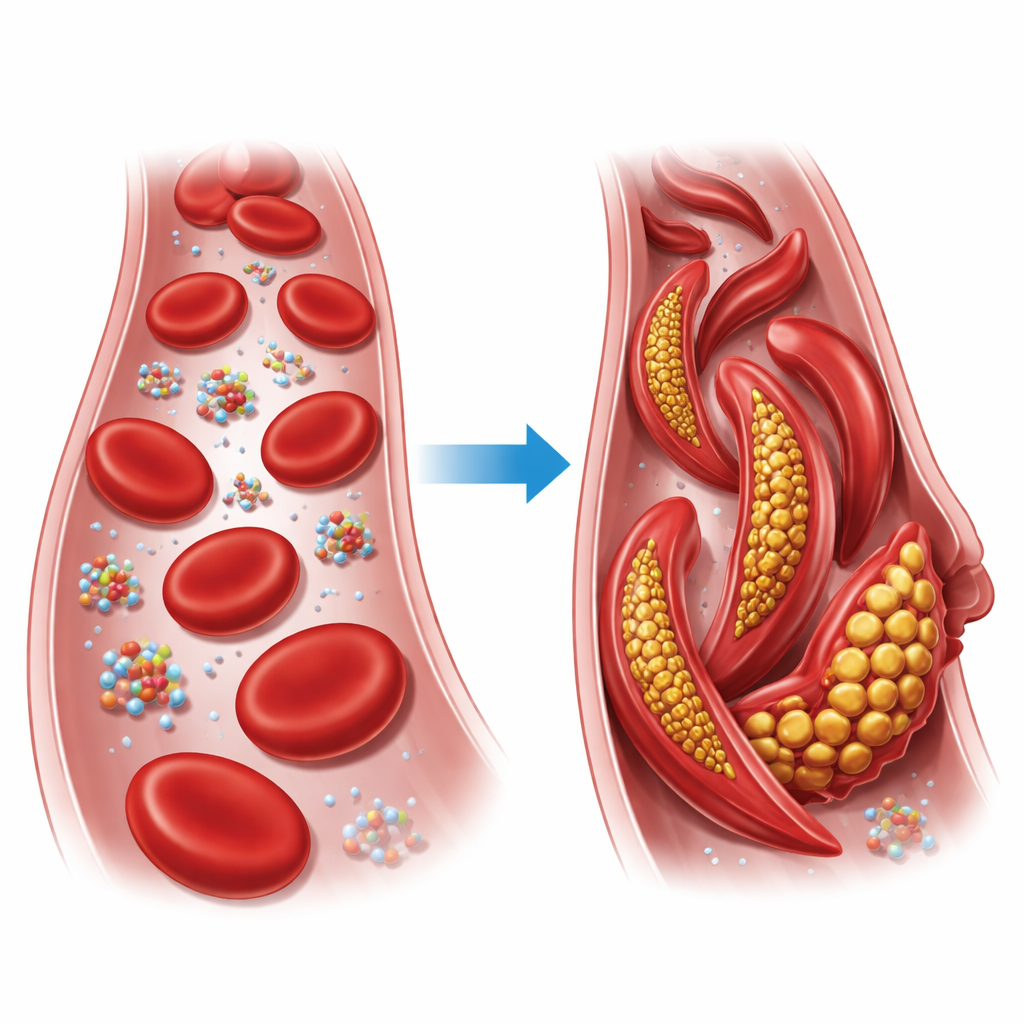
Ein winziger Austausch mit großen Folgen
Hämoglobin ist das sauerstofftragende Protein, das unsere roten Blutkörperchen füllt. Jede Hämoglobineinheit besteht aus vier Ketten, die sich zu zwei Hauptkonformationen anordnen können, die als entspannter (R-)Zustand und angespannter (T-)Zustand bekannt sind. Bei der Sichelzellenkrankheit wird in einer dieser Ketten nur ein Baustein ausgetauscht: eine geladene Glutamatseite wird an Position sechs der Beta-Kette durch das fettige Valin ersetzt. Unter niedrigem Sauerstoffgehalt verbindet sich diese veränderte Form, genannt Sichelhämoglobin, zu langen Fasern, die normalerweise runde rote Blutkörperchen in steife, sichelartige Formen verzerren, kleine Gefäße verstopfen und Gewebe von Sauerstoff abschneiden können.
Die sich ändernde Gestalt des Hämoglobins verfolgen
Die Autorinnen und Autoren konzentrieren sich darauf, wie ganze Hämoglobineinheiten sich drehen und in einer Faser zusammenpacken. Sie verfolgen diese großskalige Formänderung mit einem einzigen Winkel, der misst, wie sich zwei Hälften des Proteins gegeneinander verdrehen. Mithilfe von Molekulardynamik-Simulationen — virtuellen Experimenten, die berechnen, wie Atome sich über die Zeit in Wasser und Salz bewegen — treiben sie diesen Winkel behutsam über einen großen Bereich und berechnen, wie viel Energie jede Konformation kostet. Sie finden, dass sowohl normales als auch Sichelhämoglobin bei Körpertemperatur viele dieser Formen erkunden können. Sichelhämoglobin zeigt einen leicht bevorzugten Winkel, doch diese Formvorlieben allein reichen nicht aus, um zu erklären, warum nur die Sichelvariante stabile Fasern bildet.
Warum Sichel-Fasern kleben und normale zerfallen
Um den Kern der Faserbildung zu erfassen, misst die Studie, wie stark benachbarte Hämoglobineinheiten einander entlang und quer zur Faser anziehen. Das Team berechnet die Kohäsionsenergie — die Nettokraft, die Einheiten zusammenhält — für viele unterschiedliche Gesamtformen. Beim Sichelhämoglobin bleibt diese Kohäsionsenergie über den ganzen getesteten Winkelbereich negativ (also attraktiv), sodass Fasern stabil bleiben und nicht leicht auseinanderfallen. Im Gegensatz dazu weisen einige Konformationen des normalen Hämoglobins positive Kohäsionsenergien auf, was Fasern bei diesen Winkeln instabil macht und zu spontanem Zerfall neigt. Ein entscheidender Unterschied liegt darin, wie sich die mutierten Valin-Seitenketten in benachbarte Proteine schmiegen: Bei Sichelhämoglobin bilden diese fettigen Stellen robuste Kontakte sowohl seitlich als auch entlang der Faserachse und fördern so direkt das Fasernwachstum.
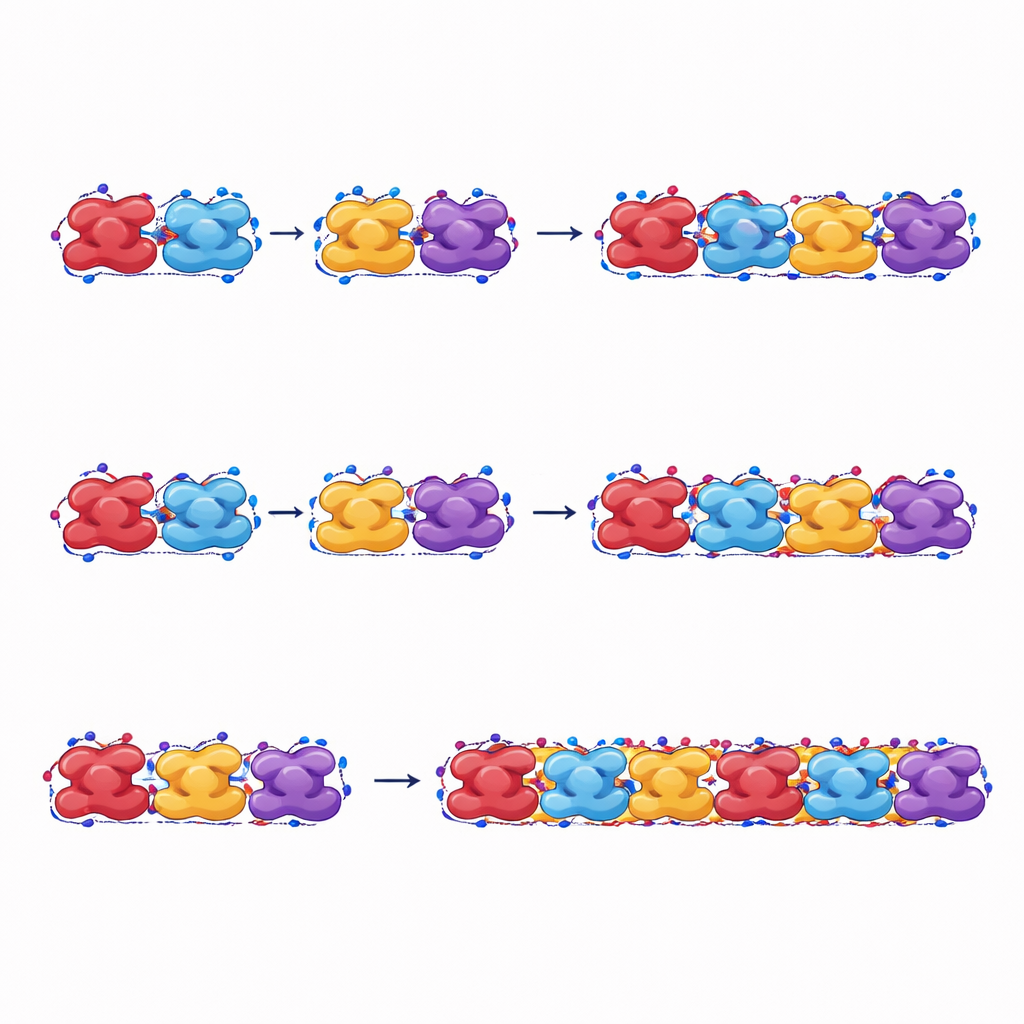
Wie diese Fasern Last tragen und brechen
Die Autorinnen und Autoren dehnen ihre simulierten Fasern außerdem, um mechanischen Stress zu simulieren. Beim Zug entlang ihrer Länge halten Fasern aus Sichelhämoglobin höheren Kräften und Dehnungen stand und dissipieren mehr Energie, bevor sie brechen, als Fasern aus normalem Hämoglobin. Selbst die entspannte Form sichelbedingter Fasern, die nicht diejenige ist, in der Fasern zuerst erscheinen, kann die Kette durch plastische Formänderungen aufrechterhalten und so helfen, die Faser nach ihrer Entstehung intakt zu halten. Fasern aus normalem Hämoglobin trennen sich dagegen leichter zwischen benachbarten Einheiten und nehmen weniger Energie vor dem Versagen auf, was bestätigt, dass sie unter Belastung weniger stabil sind.
Hinweise für zukünftige Therapien und neue Materialien
Insgesamt zeigen die Simulationen, dass eine einzelne Aminosäureänderung die Art verändert, wie Hämoglobineinheiten aufeinandertreffen, und die Gesamtanordnung in Winkel verdreht, die starke Anziehung begünstigen — besonders im angespannten Zustand. Diese Kombination aus Geometrie und Haftung erlaubt es Sichelhämoglobin, lange, steife Fasern zu bilden, die sowohl thermischen Bewegungen als auch mechanischem Zug widerstehen und damit letztlich rote Blutkörperchen verformen und den Blutfluss blockieren. Indem die Arbeit auf spezifische Merkmale der Gesamtprotein-Anordnung hinweist, die die Faserstabilität steuern, legen die Ergebnisse nahe, dass wirksame antisichelnde Medikamente dadurch wirken könnten, dass sie Hämoglobin in Konformationen lenken, in denen Fasern energetisch ungünstig und mechanisch brüchig werden — und so einen tödlichen molekularen Stau wieder in einen freien Blutstrom verwandeln.
Zitation: Jiang, M., Qin, Z. The quaternary structure origin of the fibrillation of sickle hemoglobin: a molecular dynamics study. npj Soft Matter 2, 7 (2026). https://doi.org/10.1038/s44431-026-00019-8
Schlüsselwörter: Sichelzellenkrankheit, Hämoglobinfasern, Proteinaggregation, Molekulardynamik, Bluterkrankungen