Clear Sky Science · de
Dynamin optimiert Protein‑Membran‑Wechselwirkungen für Fission
Wie Zellen ihre Membranen sauber abklemmen
Sekündlich sind Ihre Zellen damit beschäftigt, winzige Membranblasen abzutrennen, um Fracht zu transportieren, innere Kompartimente umzubauen und Viren abzuwehren. Dieser scheinbar einfache Akt, ein schmales Membranrohr in zwei Teile zu schneiden, ist aus physikalischer Sicht überraschend schwierig. Die Studie stellt eine trügerisch einfache Frage: Wie macht ein Protein namens Dynamin das Membrantrennen sowohl möglich als auch zuverlässig, und welche Eigenschaften des Proteins sind dafür wirklich wesentlich?
Die zellulären Kneifer im Einsatz
Dynamin ist eine molekulare Maschine, die sich als Kragen um dünne Membranröhrchen legt und sich wie eine Schlinge zusammenzieht, um deren Bruch zu fördern. Solche Fissionsereignisse liegen Prozessen wie der Endocytose zugrunde, bei der Zellen Material aufnehmen, ebenso wie bei der Teilung innerer Strukturen etwa von Mitochondrien. Ein unbeeinflusstes Membranrohr widersteht dem Aufreißen stark, weil es zunächst auf nahezu die Dicke der Membran selbst zusammengedrückt werden muss und dabei einen instabilen Zwischenzustand durchläuft. Diese energetische Hürde ist weit größer als die zufällige thermische Energie in der Zelle, weshalb spezialisierte Fissionsproteine wie Dynamin unerlässlich sind.
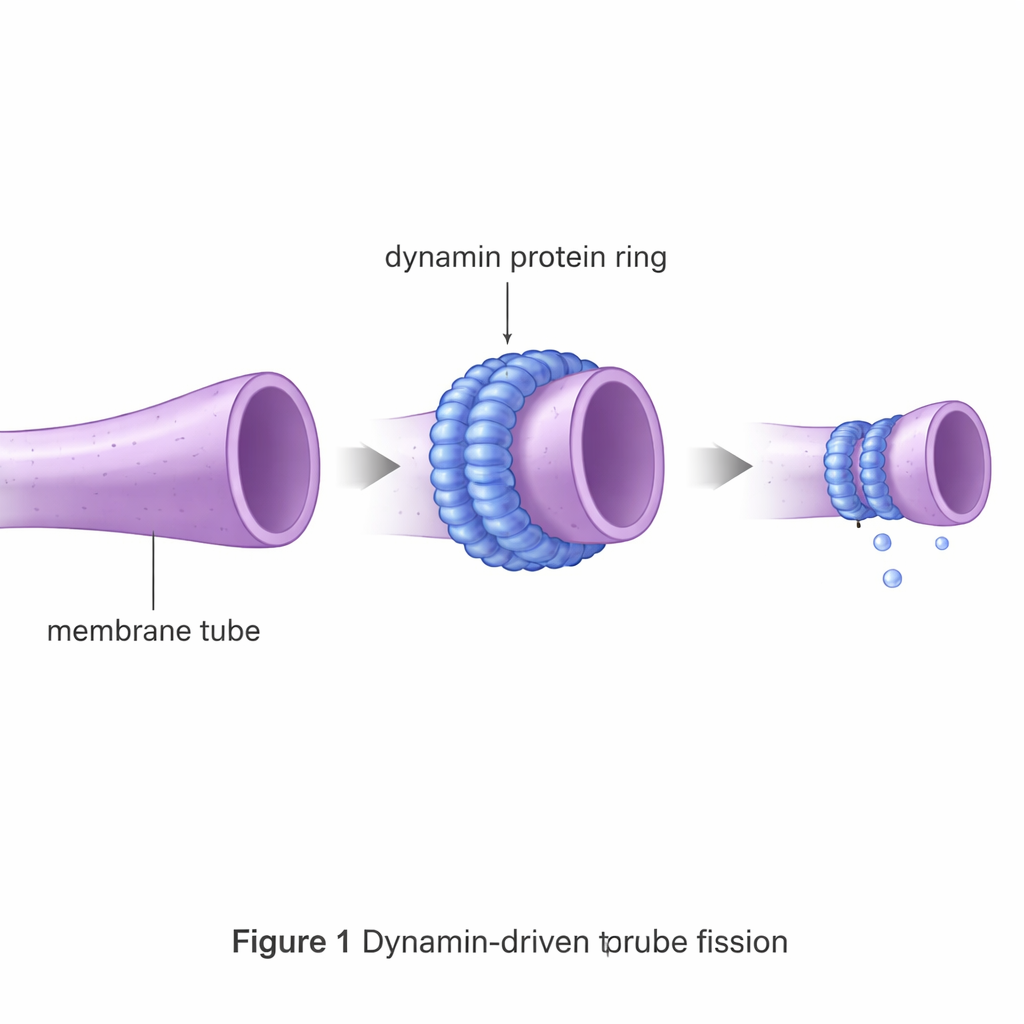
Virtuelle Membranen zum Testen von Proteindesigns
Den kritischen Moment, in dem ein Rohr reißt, direkt in Experimenten zu beobachten, ist extrem schwierig: schnelle Messungen fehlen die molekulare Auflösung, und hochauflösende Methoden frieren das System in der Zeit ein. Um diese Lücke zu schließen, nutzen die Autorinnen und Autoren ein leistungsfähiges theoretisches Werkzeug, die selbstkonsistente Feldtheorie. Anstatt jedes Atom zu verfolgen, beschreiben sie Lipide und Lösungsmittel als flexible Ketten, die glatten Feldern ausgesetzt sind. Proteine werden nicht als vollständige atomare Strukturen dargestellt, sondern als torusförmige externe Potentiale, die entweder einfach Platz ausschließen, an der Membranoberfläche haften oder sich in die äußere Schicht einlagern. Mit diesem Rahmenwerk können sie sowohl die resultierenden Membranformen als auch die gesamte freie Energie berechnen, die für den Übergang von einem intakten Rohr zum Fissionszwischenzustand nötig ist.
Welche Art von Griff hilft einem Rohr zu brechen?
Das Team variiert systematisch, wie ein dynamin‑ähnliches Protein mit der Membran wechselwirkt. Manche Modellproteine drängen nur die Oberfläche zusammen und wirken wie eine starre Manschette; andere haften schwach oder stark an den äußeren Kopfgruppen; wieder andere imitieren die reale PH‑Domäne von Dynamin, indem sie hydrophobe Teile in die äußere Monoschicht einführen und die Kopfgruppen zur Seite „spreizen“. Für jeden Fall untersuchen sie drei verbundene Größen: wie stark das Protein an einem nicht zusammengedrückten Rohr haftet, wie viel Krümmung und Verengung es beim Binden induziert, und wie hoch die verbleibende Energiebarriere ist, damit das Rohr in einen Hemifissionszustand übergehen kann, in dem die inneren Schichten verschmolzen sind. Sie finden heraus, dass einfaches Zusammendrücken die Barriere zwar senkt, aber nicht genug, um effiziente Fission zu erklären, und dass starke Oberflächenadhäsion das Brechen tatsächlich behindern kann, weil die Membran sich zuerst vom Protein lösen muss, um den Kollaps abzuschließen.
Warum flaches Einsetzen besser ist als reines Zusammendrücken
Das effektivste Design ist eines, bei dem das Protein teilweise zwischen die Lipidkopfgruppen eindringt und deren Schwänze nach oben zieht, wodurch eine lokale, chevronförmige Biegung der Membran entsteht. Dieses „Splaying“ verschiebt den engsten Punkt des Rohrs leicht neben den Proteinhalsring statt direkt darunter. Dadurch kann die Membran den kritischen Kollaps in den Hemifissionszwischenzustand abschließen, ohne sich vom Protein zu lösen, und die gesamte Energiebarriere fällt im Vergleich zu einem nackten Rohr um mehr als eine Größenordnung. Wenn die Autorinnen und Autoren die Proteinparameter automatisch anpassen lassen, um diese Barriere zu minimieren, entspricht die optimale Lösung in Größe und Wirkung nahe der PH‑Domäne von Dynamin: ein mäßig breites hydrophobes Feld, das flach eindringt, und nicht eine breite, übermäßig klebrige Oberfläche, die Lipide aus der Lösung reißen würde.
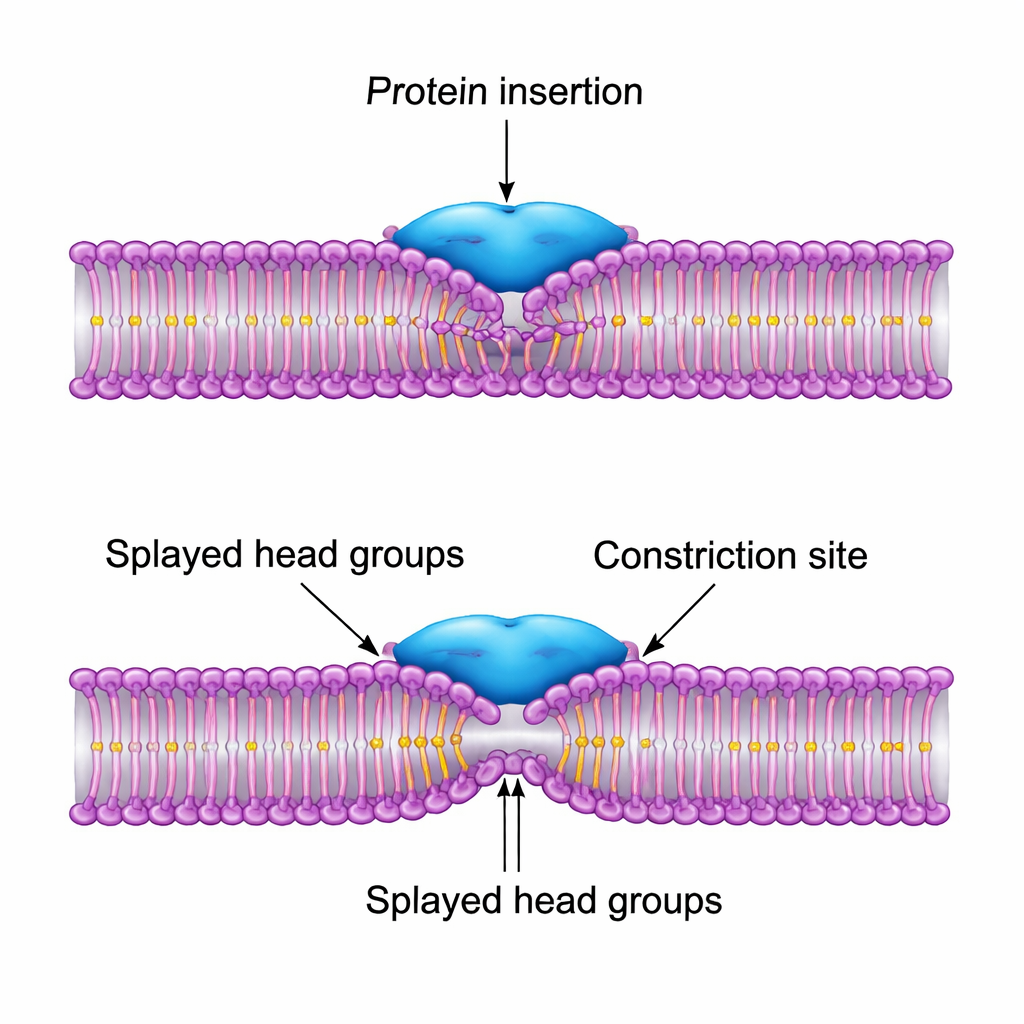
Gestaltungsregeln für Natur und Nanotechnologie
Wesentlich für Nicht‑Spezialisten ist die Botschaft, dass Dynamin nicht nur durch das Zusammenziehen eines Gürtels um die Membran wirkt, sondern dadurch, wie und wo es die äußere Schicht greift, sorgfältig abgestimmt ist. Ein flacher Keil, der die äußeren Lipide spreizt und die Krümmung direkt neben dem Protein konzentriert, erweist sich als weitaus wirkungsvoller als rohe Verengung oder starkes Haften. Diese Ergebnisse helfen zu erklären, warum die Evolution die spezifische Architektur von Dynamin begünstigt hat, und liefern Designprinzipien für synthetische Proteine oder Wirkstoffe, die Membranen in Medizin und Nanotechnologie kontrolliert schneiden oder umgestalten sollen.
Zitation: Spencer, R.K.W., Müller, M. Dynamin optimizes protein-membrane interactions for fission. npj Soft Matter 2, 6 (2026). https://doi.org/10.1038/s44431-026-00018-9
Schlüsselwörter: Membranfission, Dynamin, Protein–Membran‑Wechselwirkungen, Membrankrümmung, selbstkonsistente Feldtheorie