Clear Sky Science · de
APP E590D-Mutation erhöht die Entstehung von Aβ- und Aη-Peptiden und verschärft die Tauopathie
Warum diese seltene Mutation wichtig ist
Die Alzheimer-Krankheit wird meist als langsame Anhäufung von zwei schädlichen Proteinen im Gehirn angesehen: Amyloid und Tau. Die meisten Menschen entwickeln Alzheimer ohne einen einzelnen klaren Auslöser, doch in einigen Familien treten seltene Genveränderungen auf, die das Gleichgewicht stark zugunsten der Erkrankung verschieben können. Diese Studie untersucht eine solche ungewöhnliche Veränderung im Gen für das amyloid-Vorläuferprotein (APP) und zeigt, wie sie die Produktion toxischer Proteinfragmente stark steigern und den hirnverfilzenden Prozess, bekannt als Tauopathie, verschlimmern kann. Das Verständnis dieses seltenen Falls liefert Hinweise, die breiter dafür relevant sein könnten, wie Alzheimer beginnt und sich dann beschleunigt.
Eine kleine genetische Veränderung mit großen Folgen
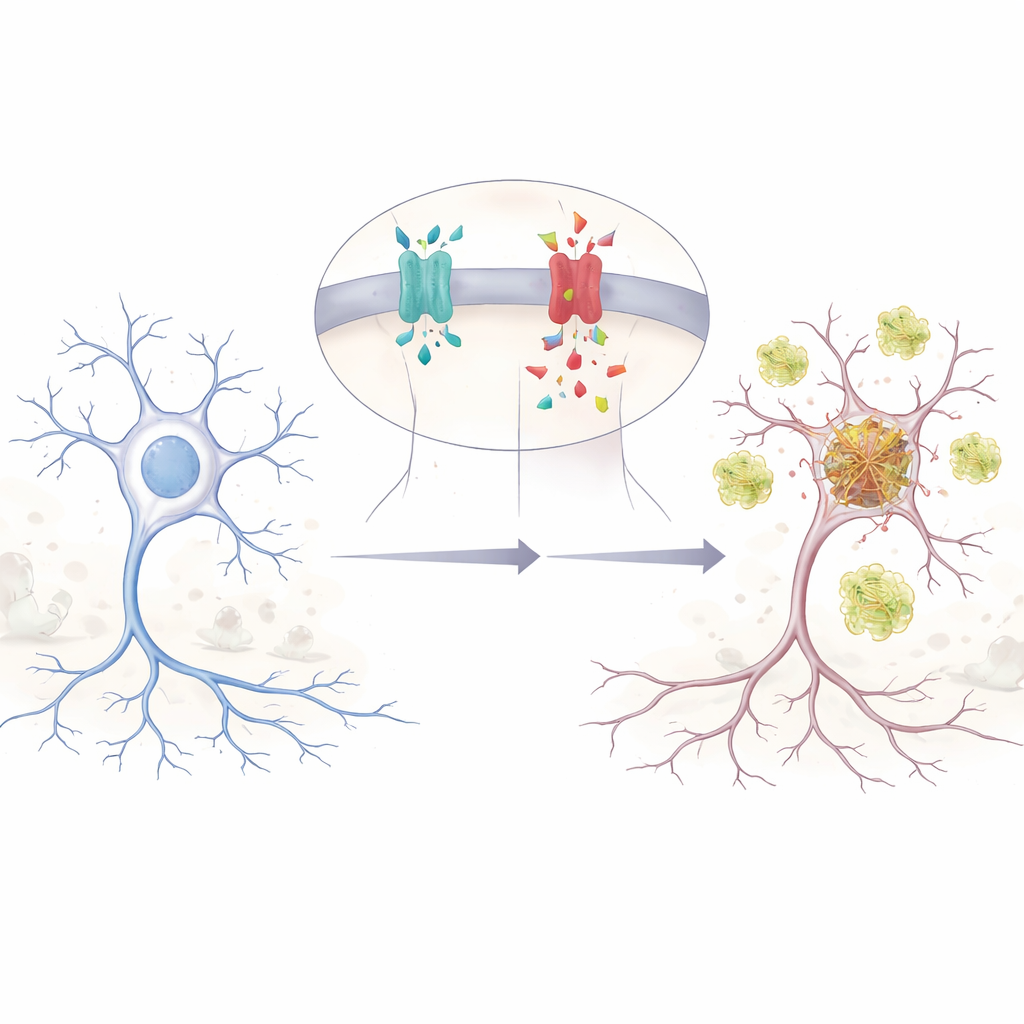
Die Autoren konzentrieren sich auf eine Einzelbuchstabenänderung im APP-Gen, bezeichnet als E590D in der im Gehirn vorherrschenden Form von APP. Diese Mutation wurde bisher nur bei zwei Personen beschrieben, beide mit bestätigter Alzheimer-Erkrankung in vergleichsweise jungem Alter und mit ungewöhnlichen, sehr frühen Störungen von Gedächtnis und Verhalten. Weil sie so selten ist, waren sich Forschende nicht sicher, ob sie tatsächlich die Krankheit verursacht oder nur ein harmloser Begleiter ist. Um das herauszufinden, rekonstruierten die Forscher die Mutation in menschlichen Zellen und in Mausneuronen und verfolgten, wie APP in seine vielen Fragmente zerschnitten wird. Sie entdeckten, dass das mutierte APP bei fairer Vergleichsbasis wesentlich mehr Amyloid‑beta (Aβ) produziert — das klebrige Peptid, das lange mit Alzheimer in Verbindung gebracht wird — als normales APP.
Zwei toxische Peptide statt eines
APP kann an mehreren Stellen geschnitten werden, ähnlich wie ein Baumstamm an verschiedenen Stellen zersägt wird. Der klassische Alzheimer-Weg erzeugt Aβ, aber ein anderer Schnitt produziert ein weniger bekanntes Fragment namens Aη. Frühere Arbeiten zeigten, dass Aη die Verbindungen zwischen Nervenzellen schädigen und die Fähigkeit des Gehirns, Erinnerungen zu stärken, schwächen kann. In ihren Experimenten fanden die Forschenden heraus, dass die E590D-Mutation nicht nur Aβ erhöht; sie verstärkt auch Aη und ein upstream‑Fragment, das in beide Wege einfließt. Das bedeutet, die Mutation verschiebt die APP-Verarbeitung in Richtung eines doppelten Angriffs durch schädliche Peptide und kann Gehirnnetzwerke bereits stören, bevor die klassischen Amyloid-Plaques zu erwarten wären.
Wie die Mutation den zellulären Verkehr beschleunigt
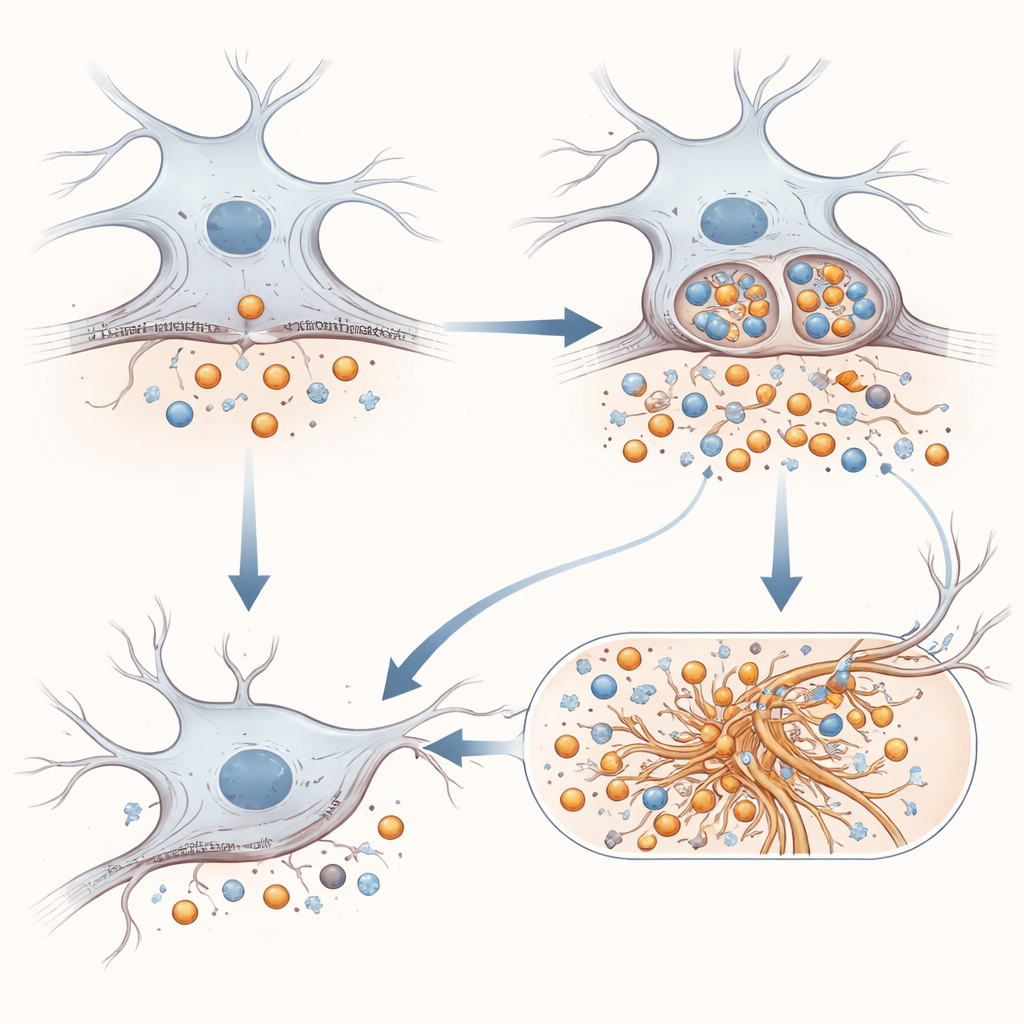
Um zu verstehen, warum mehr toxische Fragmente entstehen, untersuchte das Team, wo APP auf der Zelloberfläche sitzt und wie es sich dort bewegt. Viele der Schnitte, die Aβ erzeugen, erfolgen erst, nachdem APP durch einen Prozess namens Endozytose in die Zelle hinein gezogen wurde. Mit bildgebenden Verfahren und biochemischen Methoden, die Proteine an der Oberfläche markieren und dann deren Internalisierung verfolgen, zeigten die Wissenschaftler, dass mutiertes APP an der Außenseite von Zellen weniger häufig vorkommt und schneller in innere Kompartimente aufgenommen wird als normales APP. Einmal in frühen Endosomen trifft APP auf die Enzyme, die Aβ erzeugen, und die veränderte Trafficking-Dynamik scheint diesen Enzymen mehr Gelegenheit zu geben zu wirken. Gleichzeitig ist auch das Schneiden an der η-Stelle an der Oberfläche erhöht, was den Anstieg von Aη erklärt.
Von Proteinfragmenten zu verfilztem Tau und Gehirnentzündung
Die Geschichte endet nicht bei amyloid‑bezogenen Fragmenten. Die Forschenden prüften, ob mutiertes APP Tau beeinflusst, das Strukturprotein, das in vielen Demenzen gedrehte Fasern bildet. In Zellmodellen, die aufleuchten, wenn Tau‑Samen neue Tau‑Aggregate auslösen, führte das Vorhandensein von E590D‑APP zu stärkerer Aggregation als normales APP oder kein APP. In einem Mausmodell, das ohnehin zu Tau‑Problemen neigt, verschlimmerte die Injektion eines Virus, das das mutierte APP im Hippocampus exprimiert, die Tau‑Verfilzungen und löste stärkere Aktivierung von Astrozyten und Mikroglia aus, den Unterstützungs‑ und Immunzellen des Gehirns. Interessanterweise waren die üblichen löslichen Amyloid‑Fragmente in diesen Mäusegehirnen schwer nachweisbar, doch ein deutliches APP‑abgeleitetes Fragment trat nur bei Vorhandensein der Mutation auf, was auf eine veränderte Verarbeitung im lebenden Gewebe hindeutet.
Was das für das Verständnis von Alzheimer bedeutet
Zusammengefasst zeigen die Ergebnisse, dass diese seltene APP‑Mutation nicht harmlos ist. Sie treibt APP in Richtung der Produktion mehrerer toxischer Peptide, beschleunigt die Internalisierungsschritte, die schädliche Schnitte begünstigen, und verstärkt Tau‑Verfilzung sowie Entzündungsreaktionen im Gehirn. Für Nicht‑Fachleute lautet die Kernbotschaft: Die Biologie von Alzheimer wird nicht von einem einzelnen Übeltäter bestimmt, sondern von einem Netzwerk interagierender Proteinfragmente und zellulärer Reaktionen. Die Untersuchung solcher starken, wenn auch ungewöhnlichen genetischen Varianten bietet eine vergrößerte Sicht auf dieses Netzwerk. In diesem Fall legt sie nahe, dass therapeutische Ansätze sowohl Amyloid als auch alternative APP‑abgeleitete Peptide wie Aη sowie deren gemeinsame Wirkung auf Tau berücksichtigen sollten, anstatt nur einen einzelnen Weg isoliert anzugehen.
Zitation: Liu, T., Wetzel, L., Roy, D. et al. APP E590D mutation increases generation of Aβ and Aη peptides and exacerbates tauopathy. npj Dement. 2, 21 (2026). https://doi.org/10.1038/s44400-026-00069-9
Schlüsselwörter: Alzheimer-Krankheit, amyloid-Vorläuferprotein, Tau-Fibrillen, Neuroinflammation, genetische Mutation