Clear Sky Science · de
Eine Hochdurchsatz‑Quantifizierungsplattform mit 2D-dissoziierten menschlichen zerebralen Organoiden zur Modellierung von Neuroinflammation bei Alzheimer‑Erkrankung
Warum Infektionen fürs Gedächtnis wichtig sein könnten
Alzheimer‑Erkrankung wird meist als langsame Anhäufung klebriger Proteine im Gehirn beschrieben, doch zunehmende Hinweise deuten darauf hin, dass Infektionen diesen Prozess in Gang setzen könnten. Diese Studie untersucht diese Idee mit winzigen, im Labor gezüchteten Modellen des menschlichen Gehirns und stellt eine einfache Frage: Kann ein verbreitetes Lippenherpes‑Virus Alzheimer‑ähnliche Veränderungen in menschlichen Gehirnzellen auslösen, und kann ein antivirales Medikament diese Veränderungen rückgängig machen?
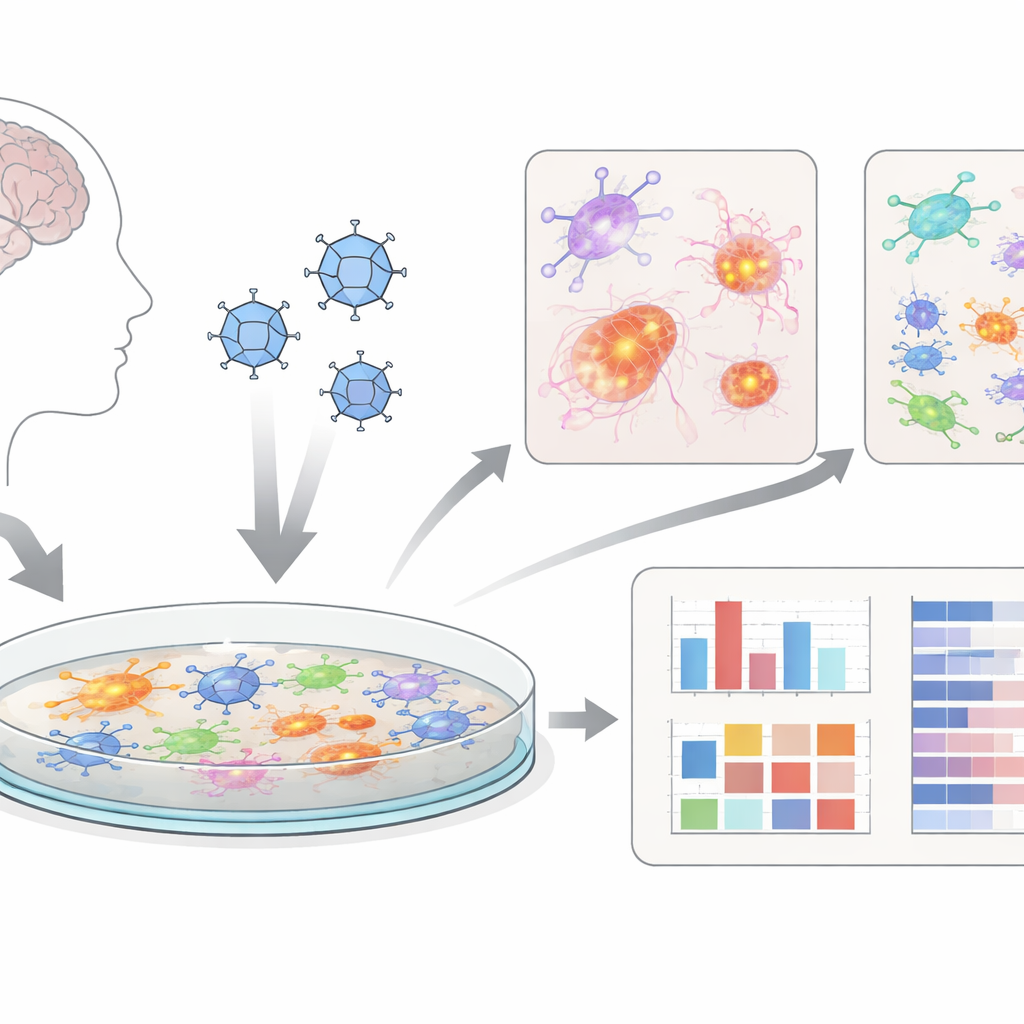
Mini‑Gehirne auf einer Platte
Statt nur mit Tieren zu arbeiten, verwendeten die Forschenden „zerebrale Organoide“ – Zellverbünde mit gehirnähnlichen Eigenschaften, gezüchtet aus humanen Stammzellen. Diese 3D‑Organoide wurden anschließend vorsichtig in flache Schichten gemischter Gehirnzellen aufgelöst, darunter Neuronen, Stützzellen (Astrozyten) und immunähnliche Mikroglia. Diese zweidimensionalen Kulturen, die sie dcOrgs nennen, lassen sich gleichmäßiger infizieren und eignen sich für Hochdurchsatz‑Tests, sodass viele Platten und Wirkstoffbedingungen parallel geprüft werden können. Das macht das System attraktiv als Screeninginstrument für neue Behandlungen.
Ein Lippenherpes‑Virus als Funke
Das Team infizierte dcOrgs mit dem Herpes‑simplex‑Virus 1 (HSV‑1), dem Erreger der meisten Lippenherpes‑Fälle und lange verdächtigt, bei manchen Menschen zur Demenz beizutragen. Sie verglichen infizierte Kulturen mit Schein‑behandelten Kontrollen, mit Kulturen, die ein antivirales Mittel (Acyclovir) erhielten, mit Kulturen, die einem anderen Virus (Influenza A) ausgesetzt waren, und mit Virus, das durch UV‑Licht inaktiviert worden war. Mithilfe automatisierter Zellanalysen und Einzelzellsequenzierung bestätigten sie, dass HSV‑1 viele Zelltypen in der Platte robust infizierte, während das inaktivierte Virus und Influenza sehr unterschiedliche, mildere Veränderungen auslösten.
Alzheimer‑ähnliche Veränderungen in und zwischen Zellen
In HSV‑1‑infizierten dcOrgs häuften viele Zellen hohe Mengen derselben Proteinformen an, die in Alzheimer‑Gehirnen beobachtet werden: intrazelluläre, verklumpte Beta‑Amyloid‑Formen sowie mehrere phosphorylierte Varianten von Tau, einem weiteren Schlüsselprotein der Erkrankung. Diese Anreicherungen waren am stärksten mit Zellen verknüpft, die virale Proteine enthielten, und besonders ausgeprägt in sterbenden Zellen. Gleichzeitig wurde weniger des längeren Beta‑Amyloid‑Fragments (Aβ42) in die umgebende Flüssigkeit freigesetzt im Vergleich zu kürzeren Formen — ein Verschiebung, die Mustern entspricht, die in der Gehirn‑Rückenmarks‑Flüssigkeit von Alzheimer‑Patienten gemessen wurden. Auch die Zellpopulationen veränderten sich: Die Anzahl der Neuronen nahm ab, während Astrozyten und Mikroglia zunahmen, was dem neuronalen Verlust und der reaktiven Entzündung in Patientenhirngewebe ähnelt.
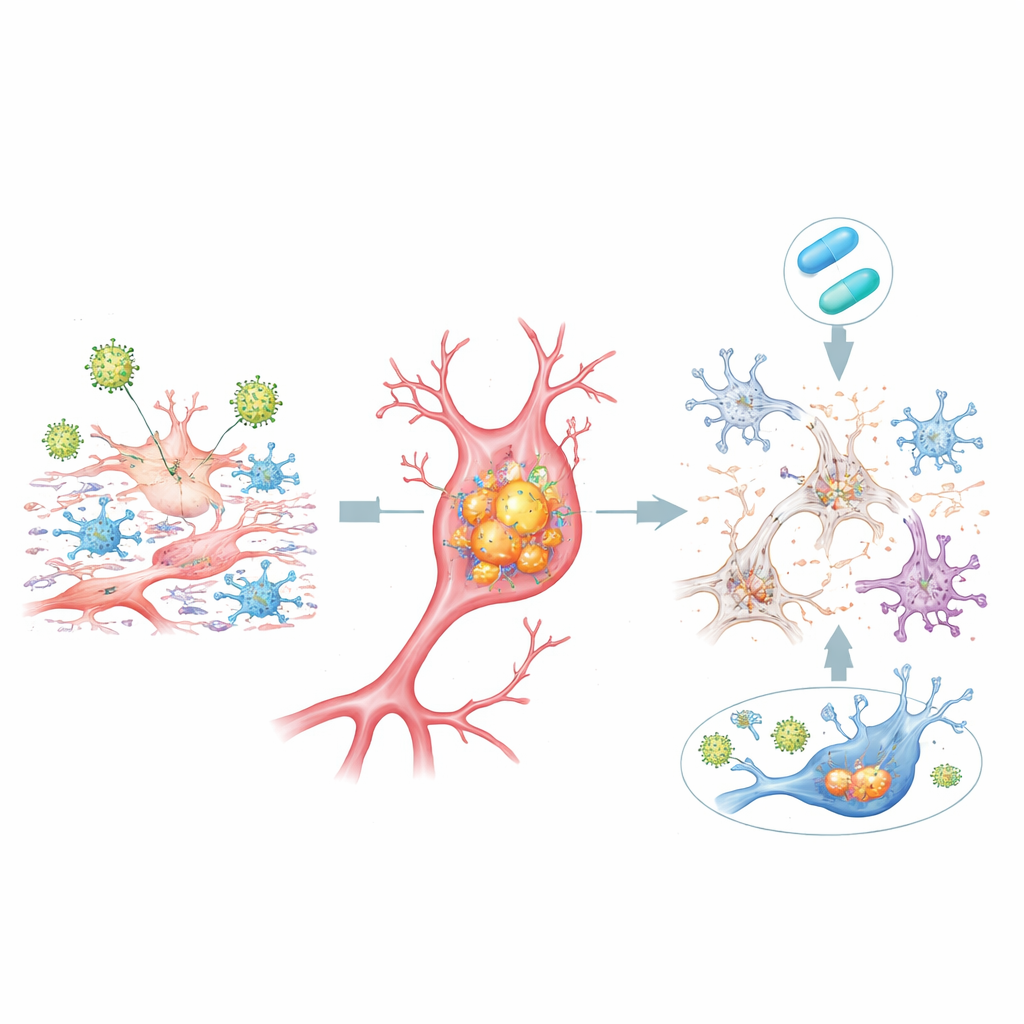
Genaktivität verbindet das Modell mit menschlichem Alzheimer
Als die Forschenden die Genaktivität über das gesamte Genom betrachteten, stellten sie fest, dass HSV‑1‑Infektion in dcOrgs viele Gene an‑ und ausschaltete, die zuvor in großen genetischen Studien mit Alzheimer‑Risiko verknüpft worden waren. Diese Veränderungen waren in einfacheren Stammzellkulturen oder in influenza‑infizierten dcOrgs nicht zu sehen, was auf ein spezifisches Zusammenspiel zwischen HSV‑1 und der gemischten gehirnähnlichen Umgebung hindeutet. Einzelzellsequenzierung zeigte, dass einige der Alzheimer‑assoziierten Genverschiebungen aus Zellen stammten, die dem Virus ausgesetzt waren, aber selbst nur geringe oder keine virale genetische Material enthielten — ein Hinweis darauf, dass Signale infizierter Nachbarzellen schädliche inflammatorische Programme verbreiten können.
Was antivirale Behandlung kann und nicht kann
Die Zugabe des antiviralen Medikaments Acyclovir kurz nach HSV‑1‑Exposition verringerte die virale Genexpression, dämpfte viele entzündliche Antworten, reduzierte die Anhäufung toxischen Beta‑Amyloids und Tau innerhalb der Zellen und stellte teilweise das Gleichgewicht der verschiedenen Zelltypen wieder her. Für einen erheblichen Anteil der Alzheimer‑assoziierten Gene kehrten die Aktivitätsniveaus wieder in Richtung Normalbereich zurück. Nicht alle Veränderungen waren jedoch reversibel: Eine beachtliche Gruppe menschlicher Gene blieb unverändert oder wurde durch die Behandlung sogar stärker gestört, besonders wenn das Medikament weniger wirksam beim Blockieren späte viraler Gene war. Das unterstreicht, dass das Stoppen der Virusreplikation zwar helfen kann, aber den biologischen Kaskadenprozess nicht unbedingt vollständig rückgängig macht, sobald er einmal in Gang gesetzt wurde.
Was das für das Verständnis von Alzheimer bedeutet
Für Nicht‑Spezialisten lautet die Schlussfolgerung, dass ein humanes Lippenherpes‑Virus, agierend innerhalb einer realistischen Mischung menschlicher Gehirnzellen, schnell viele Kennzeichen der Alzheimer‑Erkrankung hervorrufen kann – von Proteinansammlungen und sterbenden Neuronen bis hin zu genetischen Mustern, die bereits bei Patientinnen und Patienten beobachtet wurden. Das hier entwickelte flache, organoid‑basierte System ist schnell, quantitativ und skalierbar und damit ein leistungsfähiges Testfeld für antivirale Medikamente und andere Therapien zur Beruhigung von Gehirn‑Entzündungen. Obwohl dies nicht beweist, dass Herpes‑Infektionen bei jedem Patienten Alzheimer verursachen, stärkt es die These, dass für eine Teilgruppe von Menschen chronische oder reaktivierte Virusinfektionen ein wichtiger Baustein des Puzzles — und ein potenzielles Ziel für Prävention — sein könnten.
Zitation: Olson, M.N., Barton, N.J., Feng, L. et al. A high-throughput, quantitative platform using 2D dissociated human cerebral organoids to model neuroinflammation in Alzheimer’s disease. npj Dement. 2, 20 (2026). https://doi.org/10.1038/s44400-026-00066-y
Schlüsselwörter: Alzheimer‑Krankheit, Herpes-simplex‑Virus, Gehirn‑Organoide, Neuroinflammation, antivirale Therapie