Clear Sky Science · de
15 Jahre longitudinale genetische, klinische, kognitive, bildgebende und biochemische Messungen im DIAN
Warum das für Familien und die Zukunft der Alzheimer‑Behandlung wichtig ist
Die meisten Menschen denken bei Alzheimer an eine Krankheit, die spät im Leben und oft ohne Vorwarnung auftritt. In einer kleinen Anzahl von Familien jedoch führen bestimmte vererbte Genveränderungen nahezu sicher dazu, dass eine Person relativ jung Alzheimer entwickelt. Die Observationsstudie des Dominantly Inherited Alzheimer Network (DIAN) hat 15 Jahre lang diese Familien weltweit genau begleitet. Indem sie beobachtet, wie sich die Krankheit lange vor dem Auftreten von Gedächtnisproblemen entwickelt, zeigt DIAN eine detaillierte zeitliche Abfolge von Hirnveränderungen auf, die Ärzten helfen könnte, Alzheimer bei deutlich mehr Menschen früher zu erkennen, zu verhindern oder zu verzögern.
Eine globale Initiative, die Familien mit hohem Risiko verfolgt
DIAN verfolgt Erwachsene aus Familien, die seltene Mutationen in drei Genen tragen, die mit einer vererbten Form von Alzheimer assoziiert sind. Einige Teilnehmende tragen die Mutation, andere nicht; der Studienstatus wird ihnen jedoch nur mitgeteilt, wenn sie sich für einen separaten klinischen Test entscheiden. Das Projekt begann 2008 mit 10 Standorten in drei Ländern und ist auf 23 Leistungszentren in 11 Ländern angewachsen, in denen in sieben Sprachen gearbeitet wird. Über 660 Personen haben sich eingeschrieben, mehr als 300 nehmen weiterhin aktiv teil. Bei regelmäßigen Besuchen durchlaufen Freiwillige medizinische und Gedächtnisuntersuchungen, Hirnscans, Untersuchungen von Liquor und Blut und — sofern zugestimmt — eine Hirnspende nach dem Tod. Nicht‑trägerische Verwandte dienen als ungewöhnlich gut passende Vergleichsgruppe und helfen Forschern, normales Altern von krankheitsbedingten Veränderungen zu unterscheiden.
Die Krankheit bereits Jahrzehnte vor den Symptomen sehen
Da das Alter, in dem Symptome typischerweise beginnen, innerhalb jeder Familie relativ berechenbar ist, können Forschende abschätzen, wie viele Jahre ein Mutationsträger von seinem wahrscheinlichen Beginn entfernt ist. Dadurch lassen sich Personen entlang einer „Krankheitsuhr“ anordnen — von mehr als 20 Jahren vor Auftreten bis zu vielen Jahren danach. Die Ergebnisse von DIAN zeigen, dass Alzheimer kein plötzliches Ereignis ist, sondern ein langer Prozess. Klebrige Proteinablagerungen, sogenannte Amyloid‑Plaques, beginnen 15 bis 20 Jahre vor den Symptomen im Gehirn zu akkumulieren; sie sind in speziellen PET‑Scans sichtbar und spiegeln sich in sinkenden Werten einer Amyloidform im Liquor wider. Etwa 10 bis 15 Jahre vor dem erwarteten Beginn treten weitere Warnzeichen auf: abnorme Tau‑Proteine steigen im Liquor an, der Stoffwechsel des Gehirns verlangsamt sich und subtile Ausdünnungen der Großhirnrinde werden in MRT‑Aufnahmen sichtbar. Erst mehrere Jahre später werden Veränderungen im Denken und in der Alltagsfunktion in detaillierten kognitiven Tests nachweisbar.
Eine lebende Bibliothek aus Messungen und Proben
Um diese Beobachtungen in breit nutzbare Wissenschaft zu verwandeln, hat DIAN eine der umfangreichsten Sammlungen von Alzheimer‑bezogenen Daten und Geweben weltweit aufgebaut. Acht spezialisierte Kerne verwalten klinische Informationen, kognitive Tests, Hirnbildgebung, Flüssigkeits‑Biomarker, Genetik, Hirnpathologie, Statistik und die Gesamtverwaltung. Blut‑ und Liquorproben werden in einem zentralen Biobanken verarbeitet, wo fortgeschrittene Verfahren Dutzende von Proteinen messen, die mit Amyloid, Tau, Entzündung und Nervenzellschädigung verbunden sind. Genetische und „Multi‑omics“-Analysen untersuchen DNA, RNA, Proteine, Fette und andere Moleküle in Blut, Hirngewebe und aus Teilnehmenden abgeleiteten Zellmodellen. Ein wachsendes neuropathologisches Programm untersucht gespendete Gehirne sorgfältig, um Diagnosen zu bestätigen und das Krankheitsstadium zu bestimmen. All diese Informationen werden bereinigt, qualitätsgeprüft und in jährliche Datensätze eingefroren, die externe Forschende unter strengen Datenschutzbestimmungen anfordern können.
Treiber für klinische Studien und nächste Generation von Werkzeugen
DIAN ist nicht nur eine Studie des natürlichen Krankheitsverlaufs; sie bildet auch das Rückgrat eines begleitenden klinischen Studienprogramms, das Arzneimittel testet, die darauf abzielen, vererbtes Alzheimer zu verlangsamen oder zu verhindern. Da Beobachtungs‑ und Behandlungsstudien harmonisierte Verfahren verwenden, lassen sich ihre Ergebnisse kombinieren und vergleichen. Die detaillierte DIAN‑Zeitleiste der Hirnveränderungen hat bereits internationale Kriterien dafür mitgeprägt, Alzheimer biologisch zu definieren — basierend auf Amyloid-, Tau‑ und Neurodegenerationsmarkern statt allein auf Symptomen. Mit Blick auf die Zukunft erweitert das Netzwerk seine Reichweite auf Fernbewertungen mittels Smartphone‑Apps, Hausbesuchen durch Gesundheitspersonal und tragbare Geräte, um sehr frühe Veränderungen des Denkens zu erkennen und die Alltagsfunktion zu verfolgen. Es investiert außerdem stark in blutbasierte Tests und tiefere molekulare Profilierungen, um neue Therapieziele zu finden und zu verstehen, warum die Krankheit bei Individuen und Bevölkerungsgruppen unterschiedlich verläuft.
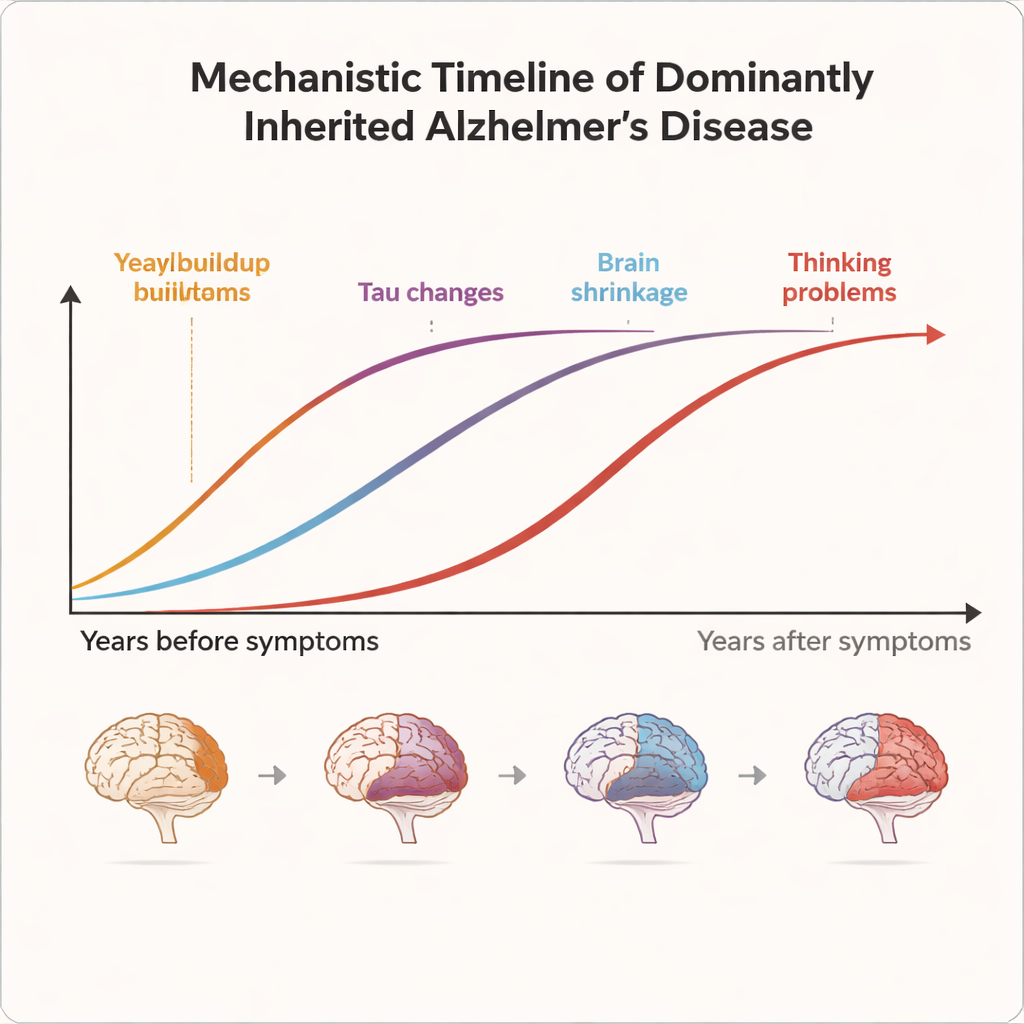
Was das für Menschen bedeutet, die sich Sorgen um Alzheimer machen
Die DIAN‑Studie zeigt, dass sich bei vererbtem Alzheimer das Gehirn bereits viele Jahre vor dem Versagen des Gedächtnisses verändert — und dass sich diese verborgenen Verschiebungen im Blut, im Liquor und in Bildgebungen messen lassen. Obwohl die untersuchten Mutationen selten sind, ähnelt der zugrunde liegende Krankheitsprozess offenbar sehr stark der weitaus häufiger auftretenden spät auftretenden Form von Alzheimer. Das macht DIAN zu einem kraftvollen Modell für das gesamte Forschungsfeld. Indem die Studie die Schritt‑für‑Schritt‑Reise vom gesunden Gehirn zur Demenz kartiert und ihre sorgfältig gesammelten Ressourcen weltweit bereitstellt, hilft DIAN Wissenschaftlern, frühere und präzisere Interventionen zu entwickeln. Für Familien mit vererbtem Risiko und für die Millionen, die insgesamt von Alzheimer betroffen sind, eröffnen diese Erkenntnisse einen klareren Weg zu früherer Erkennung, besserer Überwachung und letztlich wirksamerer Prävention und Behandlung.
Zitation: Daniels, A.J., McDade, E., Llibre-Guerra, J.J. et al. 15 years of longitudinal genetic, clinical, cognitive, imaging, and biochemical measures in DIAN. npj Dement. 2, 13 (2026). https://doi.org/10.1038/s44400-025-00047-7
Schlüsselwörter: Alzheimer-Krankheit, genetische Demenz, Hirn-Biomarker, longitudinale Studie, früherkennung