Clear Sky Science · de
Kodierung funktionaler Kanten in Graphen zur Modellierung räumlich variabler Beziehungen im Tumormikromilieu
Warum die Karte der Krebs-Nachbarschaft wichtig ist
Krebs wächst nicht isoliert. Tumorzellen leben in einem lebhaften Umfeld aus Immunzellen, Stütz‑ und Gefäßzellen sowie chemischen Signalen, die räumlich dicht beieinander liegen. Wie diese Nachbarn angeordnet sind und wie stark sie sich gegenseitig beeinflussen, kann darüber entscheiden, ob ein Tumor sich ausbreitet, auf eine Behandlung anspricht oder kontrolliert bleibt. Dieser Artikel stellt SPIFEE vor, ein neues KI‑Framework, das mikroskopische Bilder und molekulare Landkarten von Tumoren in Netzwerke übersetzt und Forschern hilft, jene Zell‑ und Signalweg‑Interaktionen zu identifizieren, die am stärksten mit Krankheitsform und Patientenergebnis verknüpft sind.
Gewebe in eine Netzwerkkarte verwandeln
Moderne Krebsstudien messen weit mehr als nur das mikroskopische Erscheinungsbild eines Tumors. Manche Methoden heben Dutzende Proteine in einzelnen Zellen hervor, andere liefern detaillierte Färbungen der Gewebestruktur, und neuere Techniken erfassen, welche Gene an Tausenden Stellen einer Tumor‑Schnittfläche aktiv sind. SPIFEE behandelt all diese Daten als verschiedene Blickwinkel auf dieselbe Nachbarschaft. Jede Probe wird als Graph dargestellt: Knoten stehen für zentrale Entitäten im Tumormikromilieu — etwa Zelltypen, visuelle Gewebemuster oder molekulare Signalwege — während Kanten erfassen, wie diese Entitäten räumlich miteinander interagieren. Entscheidend ist, dass SPIFEE eine Interaktion nicht auf eine einzelne Zahl wie „Abstand" reduziert. Stattdessen speichert jede Kante eine kleine Kurve, die beschreibt, wie stark sich zwei Entitäten über einen Bereich von Distanzen mischen oder abstoßen, wodurch wesentlich reichhaltigere räumliche Details erhalten bleiben.
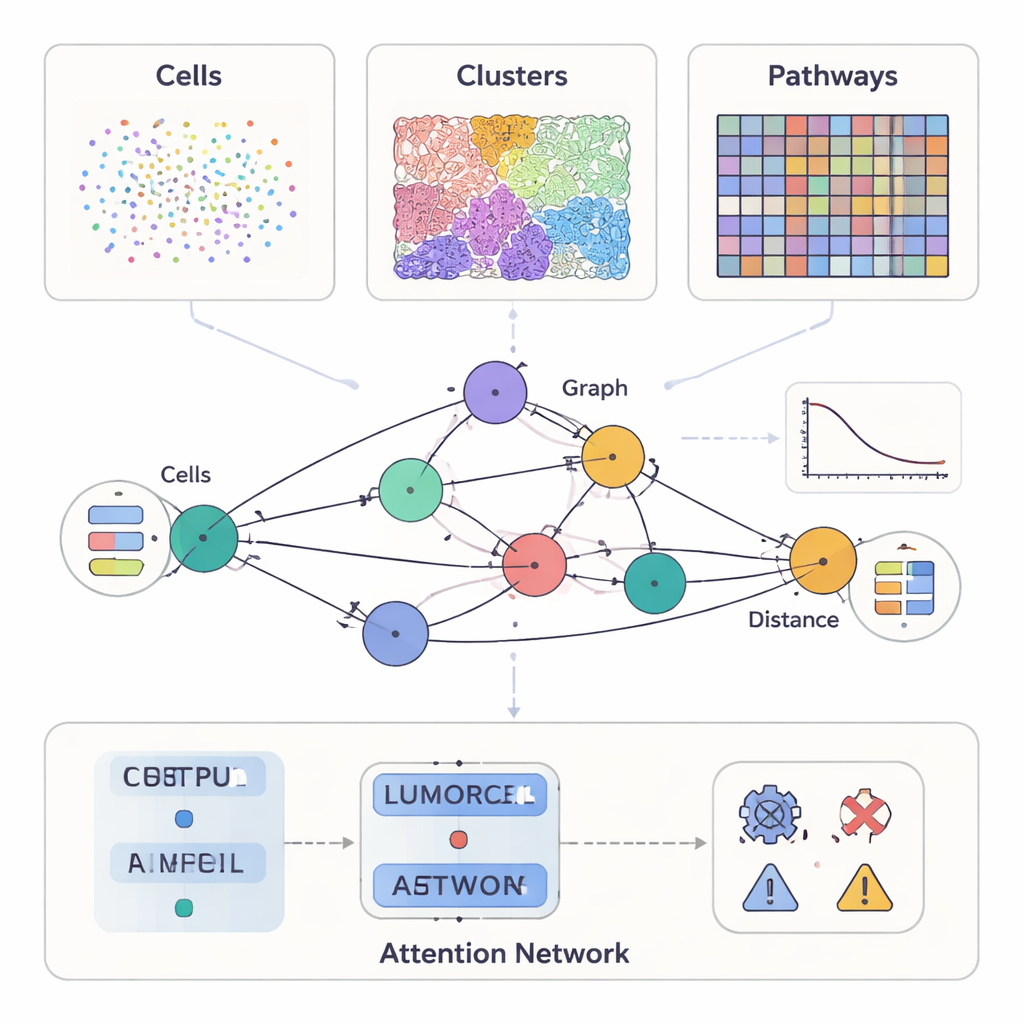
Eine flexible Linse für viele Arten von Krebsdaten
Die Autoren testeten SPIFEE an mehreren großen, unabhängigen Krebsdatensätzen, die unterschiedliche Technologien und Skalen abdecken. Bei Pankreaserkrankungsproben, die mit multipler Immunfluoreszenz markiert wurden, repräsentierte jeder Knoten einen Zelltyp, und Knotenmerkmale stammten aus Single‑Cell‑RNA‑Sequencing, das zusammenfasst, wie diese Zellen typischerweise kommunizieren. In Lungenkrebspräparaten, gefärbt mit der routinemäßigen Hämatoxylin‑Eosin‑Methode, standen Knoten für wiederkehrende visuelle Gewebemuster, die automatisch von einem selbstüberwachten Lernsystem entdeckt wurden. In einem dritten Setting wurden Standard‑Lungenpräparate von einem Deep‑Learning‑Tool in virtuelle räumliche Transkriptomik übersetzt, und SPIFEE‑Knoten repräsentierten molekulare Signalwege wie Hypoxie, Östrogen- oder JAK–STAT‑Signaling, mit Merkmalen abgeleitet aus Genaktivität. In all diesen Konstellationen konnte dasselbe Framework verschiedene Knotentypen verarbeiten und dennoch vergleichbare räumliche Graphen erstellen.
Die Interaktionen finden, die Gesundheitsverläufe trennen
Sobald SPIFEE einen Graphen konstruiert hat, führt es ihn durch ein graph‑aufmerksamkeitsbasiertes Netzwerk (Graph Attention Network), eine Form neuronaler Netze, die nicht nur ein Ergebnis vorhersagen kann — etwa Subtyp des Krebses, Überlebensrisiko oder Krankheit versus nicht‑tumoröse Entzündung —, sondern auch hervorhebt, welche Kanten für diese Vorhersage am wichtigsten waren. Im Pankreasgewebe unterschied SPIFEE chronische Pankreatitis von duktalem Adenokarzinom mit höherer Genauigkeit als frühere graphbasierte Methoden. Das Modell konzentrierte sich konsistent auf Interaktionen, an denen epitheliale (tumorähnliche) Zellen sowie regulatorische T‑Zellen, antigenpräsentierende Zellen und Helfer‑T‑Zellen beteiligt waren, was auf eine immununterdrückende Nachbarschaft hinweist, die bei Krebs stärker ausgeprägt ist als bei Entzündungen. In Lungenadenokarzinom‑Schnitten identifizierte SPIFEE bestimmte Stroma‑Tumor‑Muster, deren Interaktionen mit besserem oder schlechterem Überleben korrelierten, was nahelegt, dass die „Grenzzonen" zwischen Tumor und stützendem Gewebe wichtige prognostische Hinweise enthalten, die Standardanalysen übersehen könnten.
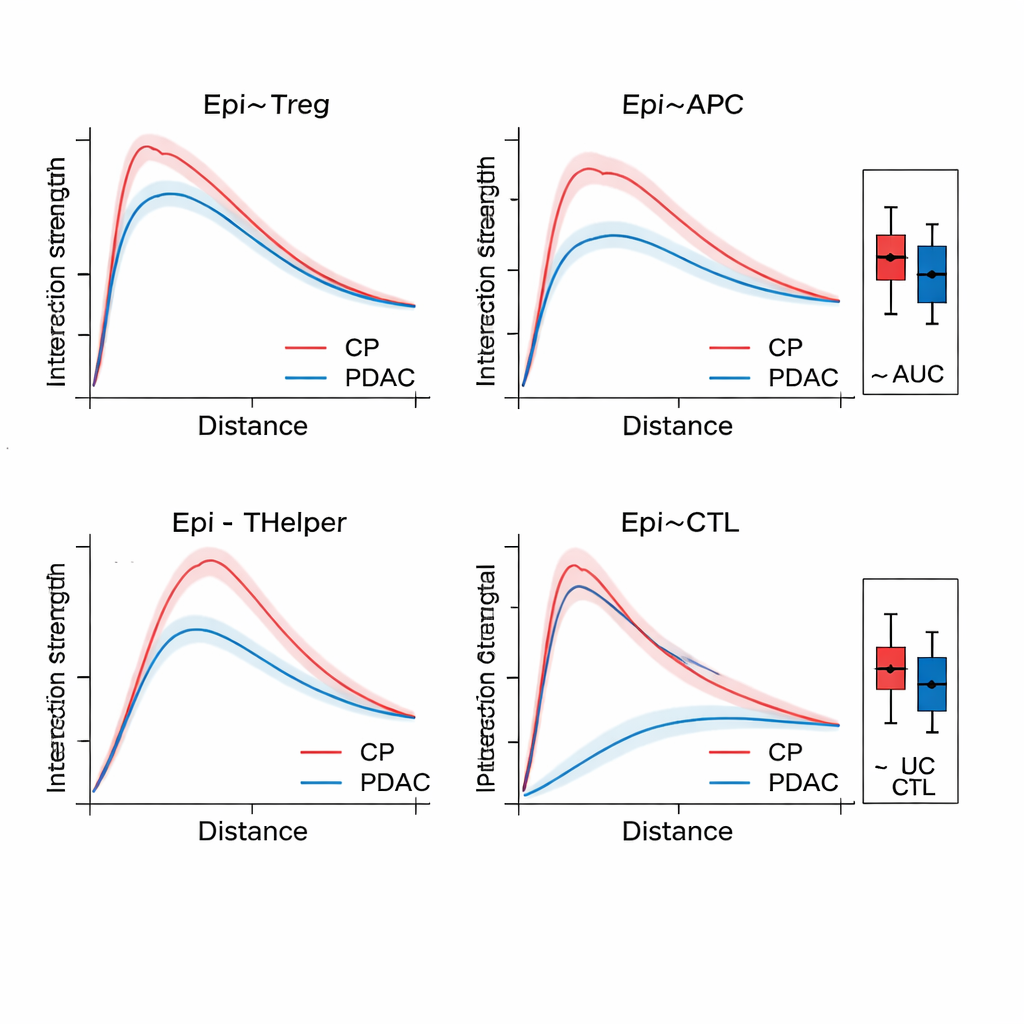
Molekularen Dialog aus Routineschnitten lesen
Besonders bemerkenswert war, dass SPIFEE sinnvolle Wechselwirkungen zwischen Signalwegen aus normalen pathologischen Bildern ableiten konnte, sobald diese in prognostizierte Genaktivitätskarten übersetzt wurden. Indem Signalwege als Knoten und ihre räumliche Ko‑Vorkommen als funktionale Kanten behandelt wurden, hob die Methode Paarungen wie Hypoxie mit EGFR oder JAK–STAT mit PI3K hervor — Kombinationen, die bereits dafür bekannt sind, Immunflucht und Medikamentenresistenz bei Lungenkrebs zu fördern. Sie bewertete außerdem östrogenbezogene Wege in Lungenadenokarzinomen sowie bestimmte Immun‑ und Stresswege in Plattenepithelmetastomen höher, Befunde, die mit Mustern in Bulk‑RNA‑Sequencing und in einem unabhängigen, echten räumlichen Transkriptomik‑Datensatz übereinstimmten. Das deutet darauf hin, dass selbst approximierte molekulare Messungen in Routineschnitten noch wiedergewinnbare Signale darüber enthalten, wie zentrale Signalwege in lebenden Tumoren miteinander interagieren.
Was das für die künftige Krebsversorgung bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft, dass SPIFEE eine neue Möglichkeit bietet, das „gesellschaftliche Leben" von Krebszellen direkt aus Bildern und molekularen Karten zu lesen. Indem es kodiert, wie Beziehungen mit der Distanz variieren, statt sie auf einzelne Werte zu reduzieren, und indem es auf aufmerksamsbasierten Netzwerken beruht, die Interaktionen nach ihrer Bedeutung sortieren, kann das Framework Kombinationen aus Zellen, Gewebemustern und Signalwegen aufdecken, die Krebsarten unterscheiden und Überleben vorhersagen. Obwohl diese Befunde noch biologisch und klinisch validiert werden müssen, weisen Ansätze wie SPIFEE in eine Zukunft, in der Routine‑Tumorproben nicht nur statische Momentaufnahmen liefern, sondern dynamische Karten von Interaktions‑Hotspots, die Diagnose, Risikostratifizierung und schließlich personalisierte Therapieentscheidungen unterstützen können.
Zitation: Tsang, A.P., Krishnan, S.N., Kulkarni, R. et al. Encoding functional edges in graphs to model spatially varying relationships in the tumor microenvironment. npj Artif. Intell. 2, 27 (2026). https://doi.org/10.1038/s44387-026-00075-5
Schlüsselwörter: Tumormikromilieu, räumliche Transkriptomik, graphneuronale Netze, Krebspathologie, Zell-Zell-Interaktionen