Clear Sky Science · de
Ein stoffwechselinformiertes neuronales Netzwerk identifiziert Wege, die die Wirksamkeit und Toxizität antimikrobieller Kombinationen beeinflussen
Warum das für die tägliche Gesundheit wichtig ist
Da immer mehr Infektionen nicht mehr auf unsere Standardantibiotika ansprechen, greifen Ärztinnen und Ärzte zunehmend zu Wirkstoffkombinationen. Das Mischen von Medikamenten ist jedoch ein zweischneidiges Schwert: Das richtige Paar kann hartnäckige Bakterien beseitigen, während die falsche Kombination Organe wie Nieren und Leber schädigen kann. Diese Studie stellt einen neuen computerbasierten Ansatz namens CALMA vor, der Wissenschaftlern und Klinikerinnen helfen soll, Kombinationen zu finden, die sowohl wirksam gegen Keime als auch schonender für Patientinnen und Patienten sind.
Bakterien bekämpfen ohne Trial-and-Error
Traditionell bedeutete die Suche nach guten Antibiotikakombinationen, eine enorme Anzahl von Wirkstoffpaaren oder -trios im Labor und bei Patientinnen zu testen. Die Anzahl möglicher Mischungen wächst mit jedem zusätzlichen Wirkstoff explosionsartig, sodass ein vollständiges experimentelles Screening unrealistisch wird. Hinzu kommt, dass die meisten bestehenden Werkzeuge nur darauf abzielen, wie stark Kombinationen Bakterien abtöten, und dabei außer Acht lassen, wie sie menschliches Gewebe schädigen könnten. Die Autorinnen und Autoren argumentieren, dass zur Entwicklung besserer Therapien beide Seiten berücksichtigt werden müssen: Wirksamkeit gegen Erreger und Sicherheit für Menschen.
Ein intelligentes Modell, das Zellchemie versteht
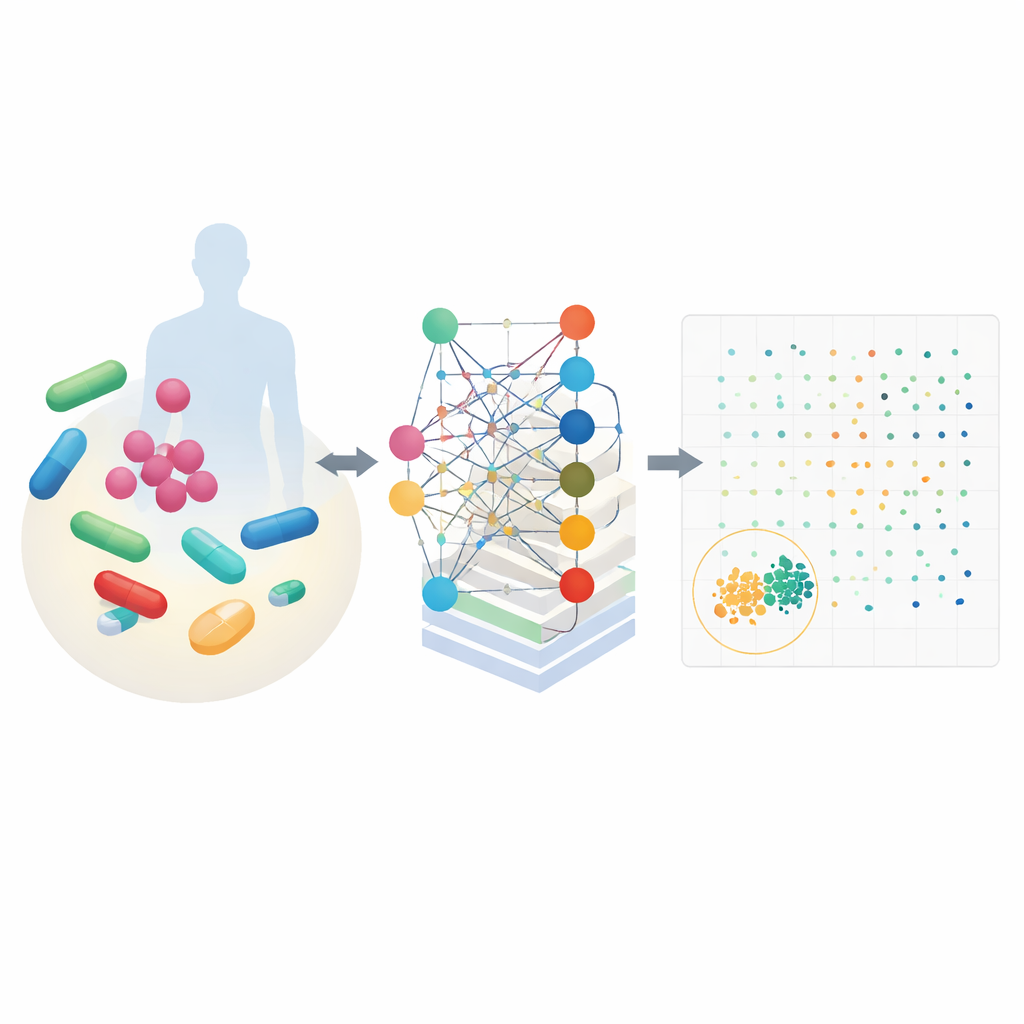
CALMA vereint zwei starke Ideen. Erstens nutzt es detaillierte Karten des zellulären Stoffwechsels, die beschreiben, wie Organismen Nährstoffe in Energie und Bausteine umwandeln. Diese Karten, erstellt für Bakterien wie Escherichia coli und den Tuberkuloseerreger, simulieren, wie tausende chemische Reaktionen sich verändern, wenn ein Medikament vorhanden ist. Zweitens speist CALMA diese Simulationen in ein künstliches neuronales Netzwerk, dessen Struktur metabolischen Wegen nachempfunden ist. Indem Informationen entsprechend bekannter biologischer Pfade gruppiert werden – etwa Energiegewinnung oder Nukleotid-Recycling – lernt das Modell Muster, die bestimmte Wege entweder mit effektiver bakterizider Wirkung oder mit schädlichen Nebenwirkungen in menschlichen Zellen verknüpfen.
Die Landschaft möglicher Wirkstoffmischungen absuchen
Anhand von Daten aus früheren Experimenten und großen Sicherheitsdatenbanken trainierten die Forschenden CALMA so, dass jede Wirkstoffkombination zwei Werte erhält: einen für die Stärke der antibakteriellen Wirkung und einen für die Wahrscheinlichkeit, beim Menschen toxisch zu sein. Das Auftragen dieser Werte erzeugt eine Landschaft, in der die besten Kandidaten unten links liegen – stark gegen Mikroben und schonend für menschliche Zellen. Als sie CALMA auf 35 klinisch relevante Wirkstoffe anwandten, reduzierte das Tool knapp 600 mögliche Paare auf eine kleine Auswahl vielversprechender Optionen und verkleinerte den experimentellen Suchraum um etwa 97 Prozent. Zu den Top-Vorschlägen gehörten Kombinationen mit gängigen Antibiotika wie Azithromycin, Vancomycin, Isoniazid und Trimethoprim.
Von Computerprognosen zu Labortests und echten Patientinnen
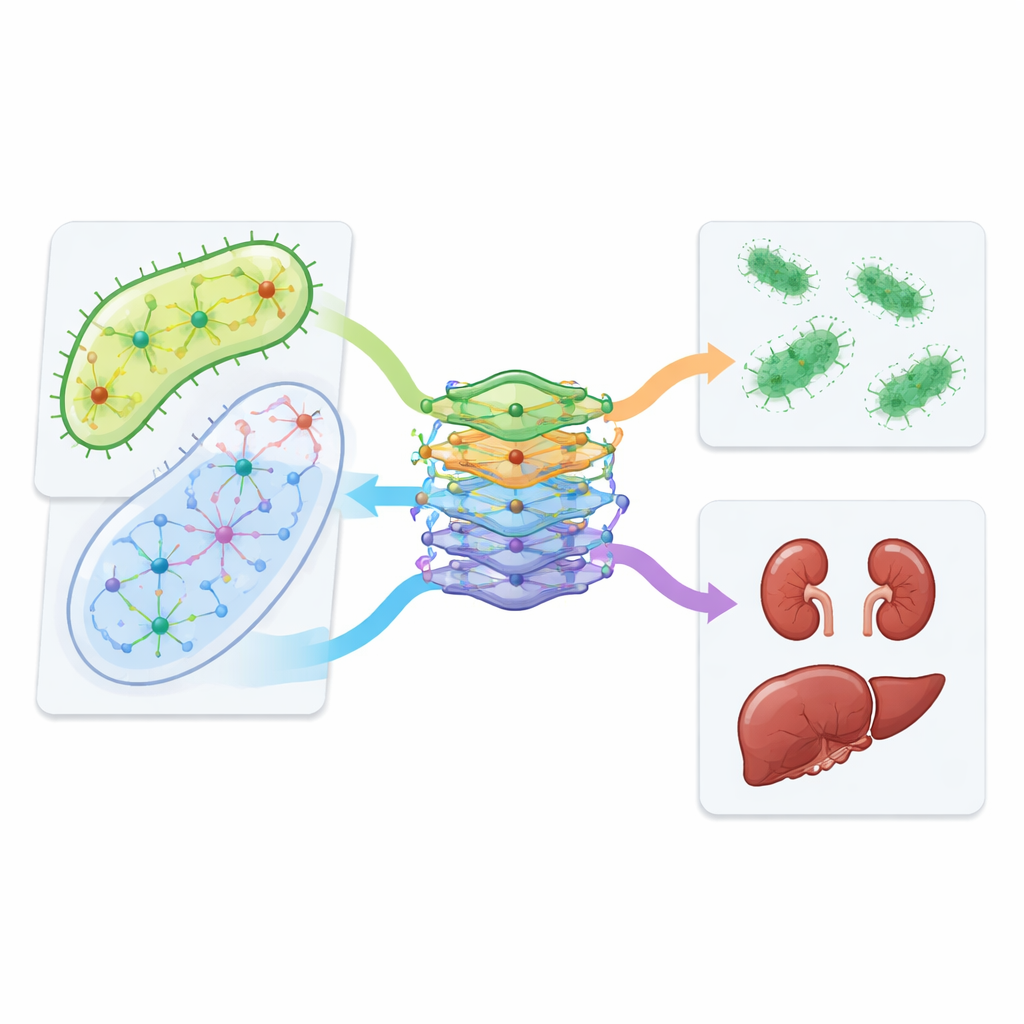
Das Team ging über Simulationen hinaus und testete mehrere vorhergesagte Kombinationen in Nieren- und Leberzelllinien. Sie fanden, dass bestimmte Paare, darunter Azithromycin mit Vancomycin und Isoniazid mit Trimethoprim, für menschliche Zellen weniger toxisch waren als die Einzelwirkstoffe, während sie weiterhin gegen E. coli aktiv blieben. Das Design von CALMA erlaubte den Forschenden außerdem zu untersuchen, welche metabolischen Wege die Toxizität antreiben. Ein Weg, der DNA-Bausteine recycelt – bekannt als Nukleotid-Salvage – erwies sich als Schlüsselfaktor: dessen Modifikation in Zellversuchen veränderte die Schädlichkeit einiger Kombinationen. Schließlich untersuchten die Autorinnen und Autoren Gesundheitsdaten von Hunderttausenden Patientinnen und Patienten und beobachteten, dass Personen, die Azithromycin zusammen mit Vancomycin erhielten, seltener dokumentierte Nierenprobleme aufwiesen als ähnliche Patienten, die nur Vancomycin bekamen – ein Befund, der die Laborergebnisse spiegelte.
Was das für künftige Behandlungen bedeutet
Für Nicht-Spezialistinnen und Nicht-Spezialisten lässt sich CALMA als intelligenter Filter begreifen, der genug biologische Informationen enthält, um vorzuschlagen, welche Wirkstoffmischungen als Erstes getestet werden sollten. Anstatt Antibiotika blind zu kombinieren und auf das Beste zu hoffen, können Forschende sich auf Kombinationen konzentrieren, die das Modell voraussichtlich auf bakterielle Schwachstellen zielen lassen und gleichzeitig empfindliche menschliche Wege schonen. Zwar hängt die Methode von verfügbaren Daten ab und ist nicht perfekt, doch sie bietet einen rationaleren Weg zur Gestaltung von Kombinationstherapien. Mit der Zeit könnten Werkzeuge wie CALMA Ärztinnen und Ärzten helfen, resistente Infektionen sicherer zu behandeln, Trial-and-Error in der Arzneimittelentwicklung zu reduzieren und sogar auf andere Erkrankungen übertragen werden, bei denen Kombinationstherapien und Nebenwirkungen eine große Rolle spielen.
Zitation: Arora, H.S., Lev, K., Robida, A. et al. A Metabolism-Informed Neural Network Identifies Pathways Influencing the Potency and Toxicity of Antimicrobial Combinations. npj Drug Discov. 3, 11 (2026). https://doi.org/10.1038/s44386-026-00042-9
Schlüsselwörter: Antibiotikakombinationen, Arzneimitteltoxizität, künstliche neuronale Netzwerke, Stoffwechsel, antimikrobielle Resistenz