Clear Sky Science · de
Abschluss auf Signalwegstörungen aus histopathologischen Bildern mittels logisch-eingeschränktem Gen‑Pathway-heterogenem Wissensgraphen
Verborgene zelluläre Signale in Krebspräparaten erkennen
Wenn Ärztinnen und Ärzte Krebs unter dem Mikroskop betrachten, sehen sie überwiegend Formen und Farben, nicht die komplexen molekularen "Unterhaltungen", die innerhalb der Zellen stattfinden. Doch diese unsichtbaren Signal‑"Dialoge" zwischen Genen und Signalwegen bestimmen oft, wie ein Tumor wächst und wie er auf Therapien reagiert. Diese Studie stellt ein neues KI‑System vor, das routinemäßige Pathologiebilder ausliest und ableitet, welche zellulären Kommunikationswege bzw. Signalwege fehlreguliert sind — und so eine Möglichkeit bietet, molekulares Verhalten ohne zusätzliche Labortests zu erahnen.
Von einzelnen Genhinweisen zum größeren Zusammenhang
Traditionelle Ansätze versuchen, den Status einzelner Gene aus Gewebsbildern vorherzusagen: Ist ein bestimmtes Gen mutiert oder nicht? Das ist nützlich, doch Krebs hängt selten von einem einzelnen fehlerhaften Gen ab. Stattdessen arbeiten Genverbünde zusammen, um ganze Signalwege zu stören, die Wachstum, Überleben und Immunität steuern. Die Autoren argumentieren, dass die Fokussierung auf Einzelgene dieses kooperative Verhalten übersieht und deshalb nicht erklären kann, warum Tumoren unter dem Mikroskop so aussehen und sich so verhalten, wie sie es tun.
Eine Landkarte zwischen Bildern, Genen und Signalwegen erstellen
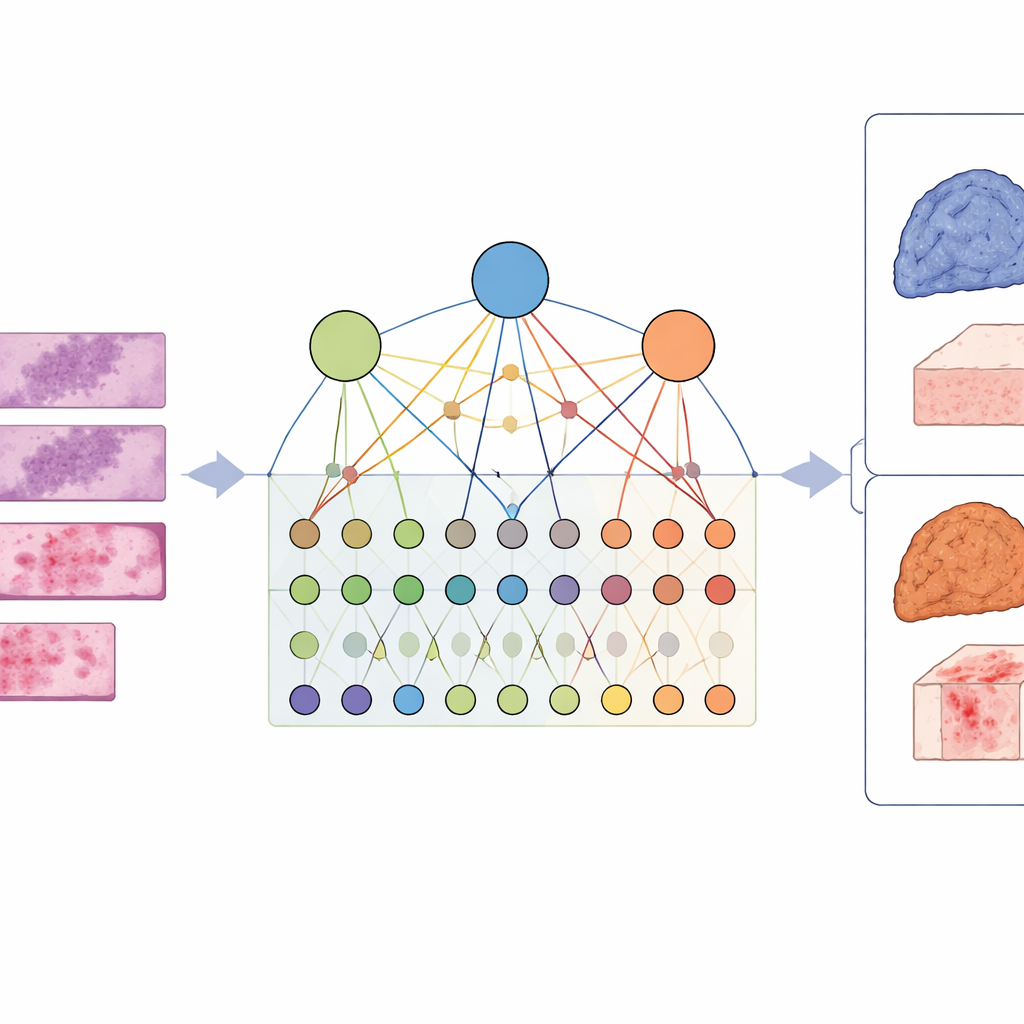
Um diese Komplexität zu erfassen, entwarfen die Forschenden ein Framework namens LCG‑HGNN, das drei Informationsebenen verbindet. Zunächst zerlegen sie jede Ganzschnittaufnahme eines Lungenadenokarzinoms in viele kleine Patches und stellen diese Patches als Graph dar, wobei benachbarte oder ähnlich aussehende Regionen verbunden werden. Als Nächstes verknüpfen sie Genmarker mit Signalwegen unter Nutzung etablierter biologischer Datenbanken und bauen einen zweiten Graphen auf, der abbildet, welche Gene zu welchen Wegen gehören. Schließlich lassen sie ein KI‑Modell Informationen durch diesen kombinierten Graphen fließen, sodass Bildmuster, Gene und Signalwege sich gegenseitig beeinflussen, statt isoliert behandelt zu werden.
Das System mit bekannter Biologie lehren
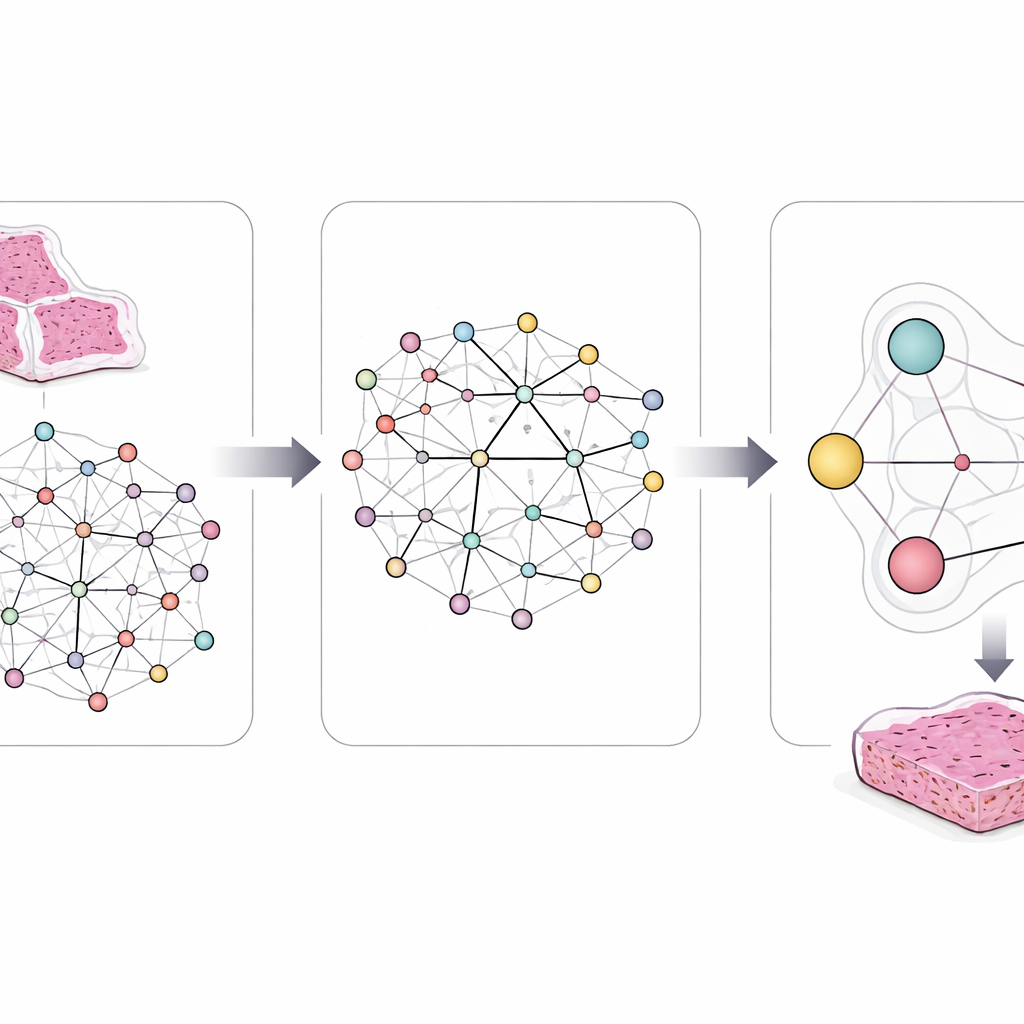
Eine zentrale Neuerung ist, dass das Modell nicht ungerichtet ohne Vorgaben lernen darf. Die Autoren betten klare, regelartige Aussagen ein, die aus Jahrzehnten der Krebsforschung stammen. Zum Beispiel treten manche Mutationen fast nie gemeinsam in demselben Tumor auf, und einige Signalwege liegen stromauf- oder stromabwärts von anderen. Solche Regeln kodieren sie als logische Einschränkungen, die die internen Verbindungen und Vorhersagen der KI sanft lenken. Wenn das Modell eine Kombination aus Gen‑ und Signalwegänderungen vorschlägt, die mit bekannter Biologie oder mit Ähnlichkeiten zwischen Patientenpräparaten kollidiert, drängen diese Regeln es zu realistischeren Alternativen.
Genauigkeit im Vergleich zu bestehenden Methoden prüfen
Das Team evaluierte sein System an über 1.600 Lungenkrebs‑Präparaten, die mit genetischen Daten verknüpft waren. Sie verglichen es mit Standard‑Deep‑Learning‑Modellen, die sich auf Einzelgene konzentrieren, und mit fortgeschritteneren Methoden, die viele Gene gleichzeitig behandeln, jedoch die Wegstruktur ignorieren. Über mehrere wichtige Signalwege hinweg, einschließlich solcher, die Wachstums‑Signale und das stützende Gewebe betreffen, sagte das neue Modell Genverbandsänderungen und Pathway‑Anomalien genauer vorher. Es erzeugte zudem Bildpatches, deren Erscheinungsbild gut mit klinisch bekannten Beispielen für bestimmte Mutationen übereinstimmte, was darauf hindeutet, dass es sich auf sinnvolle mikroskopische Muster statt auf zufällige Bildartefakte konzentrierte.
Warum das für Patientinnen und Patienten wichtig ist
Für Nicht‑Fachleute ist das wichtigste Ergebnis, dass dieser Ansatz eine Routine‑Pathologiefolie in eine reichhaltige Quelle molekularer Einsichten verwandelt. Anstatt für jedes mögliche Ziel separate, oft teure Gentests anzuordnen, könnten Ärztinnen und Ärzte solche Modelle künftig nutzen, um gestörte Signalwege direkt aus den bereits erhobenen Bildern zu screenen. Zwar benötigt die Methode noch größere, real‑weltliche Validierungen und ersetzt die Genomik bislang nicht, sie weist jedoch in Richtung einer Zukunft, in der die Mikroskopansicht zugleich ein Fenster in die innere Verdrahtung des Tumors ist — und so präzisere und biologisch fundiertere Krebsbehandlungen unterstützen kann.
Zitation: Yu, Y., Shi, W., Chen, X. et al. Inferring signaling pathway abnormalities from histopathological images via logic-constrained gene-pathway heterogeneous knowledge graph. npj Biomed. Innov. 3, 23 (2026). https://doi.org/10.1038/s44385-026-00078-6
Schlüsselwörter: Krebswege, Histopathologie KI, Graph-Neuronale Netze, Lungenadenokarzinom, Digitale Pathologie