Clear Sky Science · de
Verwendung von in-vitro-Kokulturmodellen zur Information der bakteriellen Entwicklung für die Behandlung solider Tumoren
Warum Bakterien bei Krebs für Sie wichtig sein könnten
Krebsbehandlungen wie Operationen, Chemotherapie und Strahlentherapie retten Leben, gehen aber oft mit starken Nebenwirkungen einher und führen zu häufigem Therapieversagen. Eine faszinierende neue Idee besteht darin, lebende Bakterien als präzise Werkzeuge einzusetzen, die feste Tumoren von innen aufspüren und angreifen können. Dieser Artikel erklärt, wie Wissenschaftler Labortestsysteme entwickeln — in denen menschliche Zellen und Bakterien gemeinsam wachsen —, um sicherere, intelligentere bakterielle Therapien zu entwerfen, bevor sie je an Patienten angewendet werden.
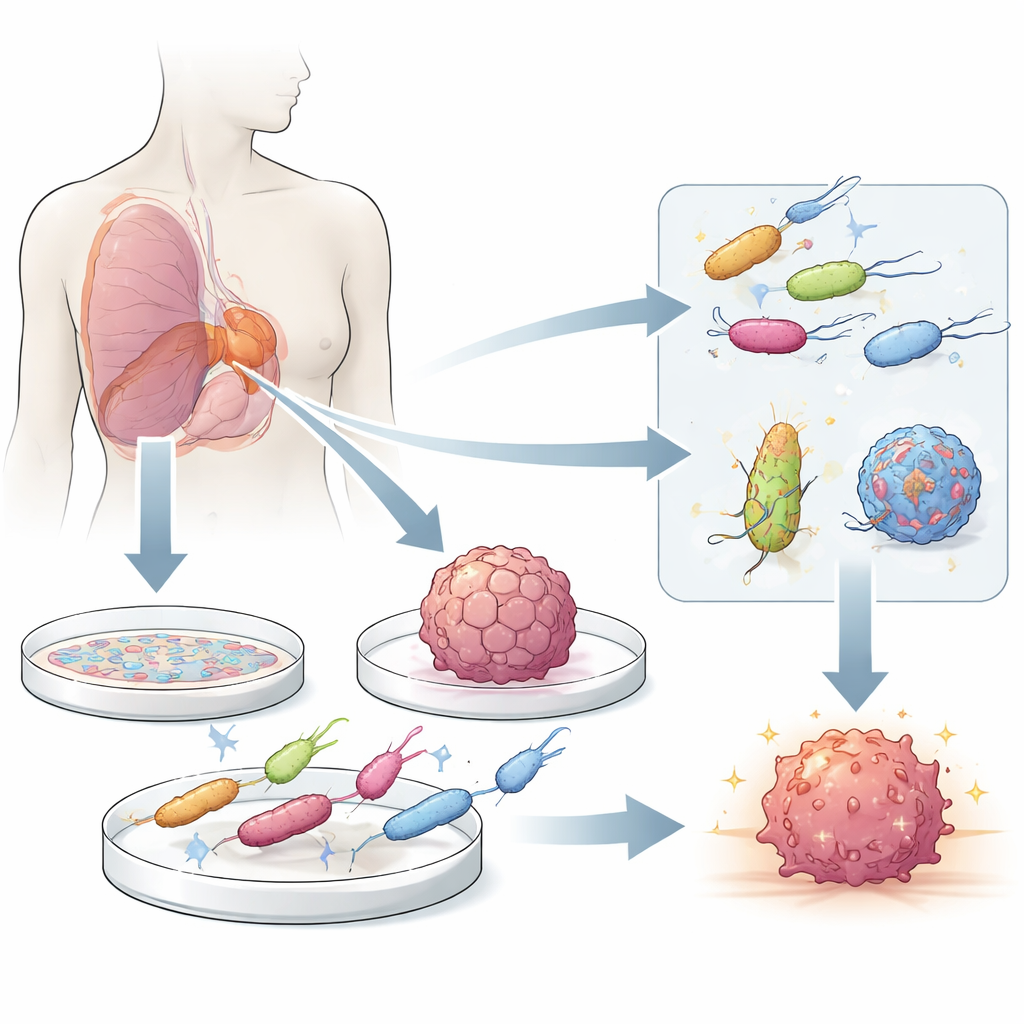
Kleine Helfer, die Tumoren anvisieren
Bestimmte Bakterien bevorzugen von Natur aus die harsche, sauerstoffarme Umgebung in festen Tumoren gegenüber gesundem Gewebe. Nachdem sie durch undichte Tumorblutgefäße geschlüpft sind oder mit Immunzellen mitgereist sind, wandern diese Mikroben in Richtung toter und sterbender Zellen im Tumorkern, wo sie sich vermehren und manchmal Krebszellen abtöten und lokale Immunreaktionen auslösen können. Moderne Gentechnik verwandelt diese natürlichen „Tumor-homing“-Stämme in lebende Lieferfahrzeuge, die Medikamente, Immunstimulanzien oder andere Nutzlasten genau dort freisetzen können, wo sie am meisten gebraucht werden, während Maßnahmen zur Abschwächung ihrer schädlichen Eigenschaften die Sicherheit verbessern.
Reale Labor-Mini-Tumoren erzeugen
Um diese lebenden Arzneimittel zu verstehen und zu verbessern, benötigen Forscher Testfelder, die das Geschehen im menschlichen Körper so genau wie möglich nachbilden. Einfache zweidimensionale Zellschichten sind leicht zu züchten und nützlich für schnelles Screening, aber sie erfassen nicht die komplexe Struktur und die Sauerstoffgradienten realer Tumoren. Dreidimensionale Modelle, wie Sphäroide aus Krebszelllinien und aus Patientenmaterial gezüchtete Organoide, reproduzieren besser zentrale Merkmale wie eine lebende Außenhülle, eine stille Innenzone und einen toten Kern. Werden Bakterien direkt mit diesen Mini-Tumoren vermischt, können Forschende beobachten, wie sie eindringen, wo sie sich ansammeln und wie gut gentechnisch gesteuerte Wirkstoffschaltungen unter patientennahen Bedingungen funktionieren.
Zellen trennen, um Signale zu untersuchen
Andere Kokulturansätze konzentrieren sich weniger auf physischen Kontakt und mehr auf die unsichtbaren chemischen Austauschvorgänge zwischen Bakterien und menschlichen Zellen. In Transwell-Systemen trennt eine poröse Membran zwei Kammern, sodass kleine Moleküle hindurchdiffundieren können, während Zellen an ihrem Platz bleiben. So können Wissenschaftler beispielsweise testen, wie ein Bakterienstamm eine harmlose Verbindung in ein tumortötendes Gas umwandelt, das zu benachbarten Krebszellen diffundiert. Mikrofluidische Chips — winzige Geräte mit Kanälen und Kammern — fügen eine zusätzliche Realitätsebene hinzu. Sie ermöglichen die Steuerung von Flüssigkeitsfluss, Sauerstoffgehalt und Timing, sodass gentechnisch veränderte Bakterien wachsen, synchronisierte Absterbezyklen durchlaufen und Krebszellen wiederholt mit therapeutischen Molekülen überziehen können, wobei beide Partner über die Zeit genau beobachtet werden können.
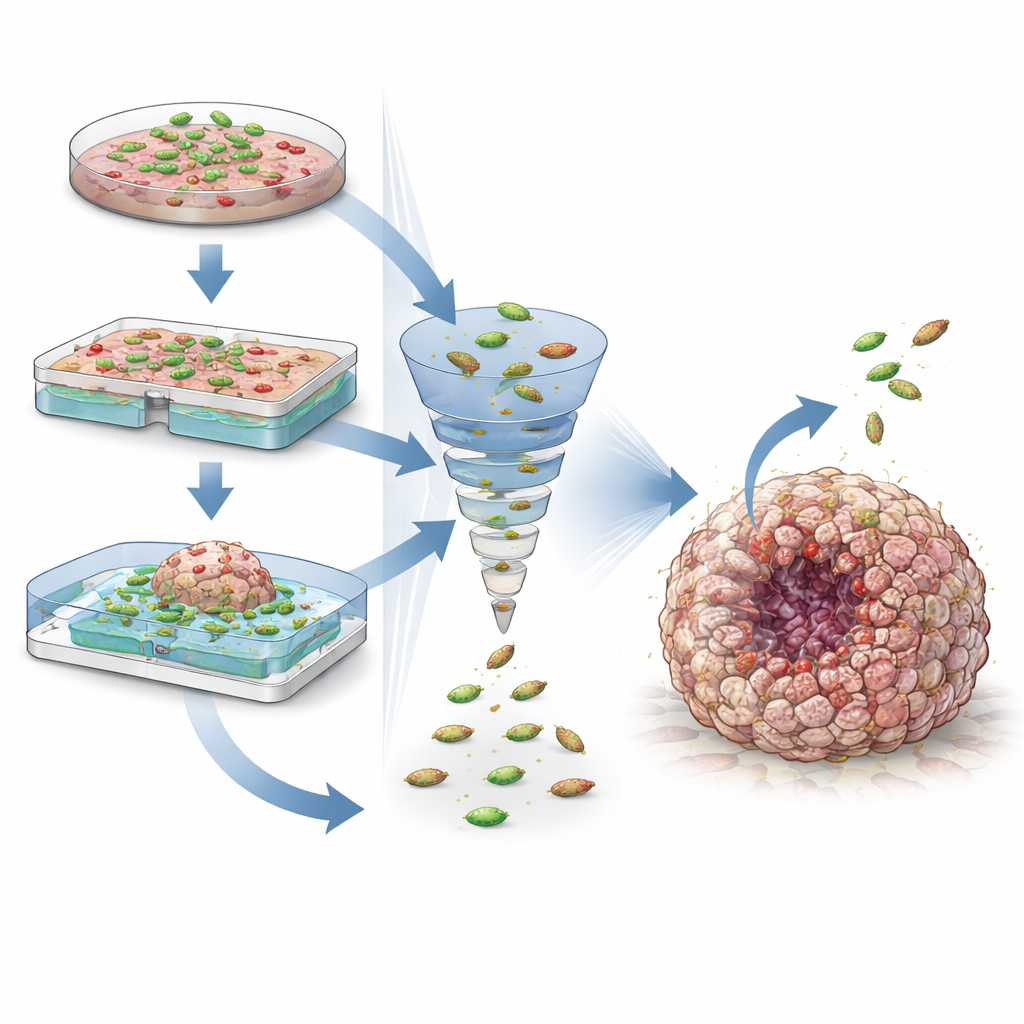
Einblick in das Tumorökosystem
Kokulturmodelle werden auch verwendet, um zu untersuchen, wie Bakterien mit dem weiteren Tumorökosystem interagieren. Aus einzelnen Patienten gewonnene Organoide können viele der genetischen Besonderheiten und Arzneimittelantworten ihres Ursprungstumors bewahren und eröffnen so personalisierte Tests bakterieller Therapien. Das Hinzufügen von Immunzellen zu diesen Kulturen zeigt, wie Bakterien die Anti-Krebs-Immunität stärken oder dämpfen können und wie sie mit Checkpoint-Inhibitoren kombiniert werden könnten. Gleichzeitig machen diese Modelle Sicherheitsbedenken sichtbar, etwa bakterielle Toxine, die DNA schädigen und möglicherweise selbst zur Krebsentstehung beitragen könnten. Durch Anpassung der Kulturbedingungen, des Sauerstoffgehalts und der Messmethoden — von Live-Bildgebung bis hin zur DNA-Sequenzierung — können Forschende diese Nutzen und Risiken systematisch erkunden.
Vom Labortisch ans Krankenbett
Trotz vielversprechender Ergebnisse im Tierversuch haben bisher nur sehr wenige bakterielle Krebstherapien klare Vorteile in klinischen Studien gezeigt. Die Autorinnen und Autoren argumentieren, dass ein klügerer Einsatz von Kokultursystemen diese Lücke überbrücken kann. Indem sie Patient-zu-Patient-Unterschiede, Tumorkomplexität und Vorbehandlungen besser erfassen, können diese Modelle aufzeigen, welche gentechnisch veränderten Stämme am vielversprechendsten sind, wie man sie mit bestehenden Medikamenten kombiniert und wo sie scheitern könnten. Sie betonen auch die Notwendigkeit gemeinsamer Standards, damit Labore weltweit Ergebnisse vergleichen und Regulierungsbehörden Sicherheit und Wirksamkeit verlässlicher beurteilen können. Einfach gesagt: Sorgfältig gestaltete Labor-Mini-Tumoren, die Seite an Seite mit Bakterien gezüchtet werden, bieten einen mächtigen Weg, diese „intelligenten Keime“ zu verfeinern und die Chancen zu erhöhen, dass künftige Patientinnen und Patienten bakterielle Therapien erhalten, die sowohl sicherer als auch wirksamer sind.
Zitation: Foschini, S., Wright, J.A., Woods, S.L. et al. Use of in vitro co-culture models to inform bacterial engineering for the treatment of solid tumours. npj Biomed. Innov. 3, 21 (2026). https://doi.org/10.1038/s44385-026-00075-9
Schlüsselwörter: bakterielle Krebstherapie, Tumor-Organoide, Kokulturmodelle, synthetische Biologie, Tumormikroumgebung