Clear Sky Science · de
3D-biogewebte in vitro-Modelle als neue methodische Ansätze für tierversuchsfreie Alternativen
Neu denken, wie wir neue Medikamente testen
Fast ein Jahrhundert lang wurden die meisten neuen Arzneimittel vor Studien am Menschen in Tieren erprobt. Dennoch scheitern mehr als 9 von 10 Wirkstoffkandidaten, die in Tieren unbedenklich erscheinen, später in Menschen. Dieser Artikel untersucht, wie eine neue Generation 3D‑"biogedruckter" menschlicher Gewebe diese Bilanz verändern könnte – indem sie genauere, humanere Wege bietet, vorherzusagen, wie unser Körper auf Medikamente reagiert, und damit potenziell sicherere Therapien schneller zu Patientinnen und Patienten zu bringen.

Von Versuchstieren zu menschorientierten Tests
Eine jüngere US‑Gesetzesänderung, bekannt als FDA Modernization Act 2.0, hat die automatische Vorschrift aufgehoben, wonach jedes neue Medikament zwangsläufig an Tieren getestet werden muss. Stattdessen können Aufsichtsbehörden nun "New Approach Methodologies" akzeptieren – testsysteme mit menschlicher Relevanz, die bessere Vorhersagen für reale Patientenreaktionen liefern sollen. Auffällig darunter ist das 3D‑Bioprinting. Dabei werden spezialisierte Drucker eingesetzt, um lebende menschliche Zellen und weiche, gelartige Materialien in komplexe Formen zu platzieren, die echte Gewebe und Mini‑Organe nachbilden. Der Prozess beginnt häufig mit medizinischen Bildern wie CT‑ oder MRT‑Scans, die als Blaupause dienen. Wissenschaftler wählen dann passende Biomaterialien, mischen die richtigen Zelltypen zu einer druckbaren "Bioink" und drucken schichtweise oder volumetrische Strukturen, die in Bioreaktoren zu funktionalen Gewebemodellen heranreifen.
Wie 3D‑Bioprinting lebende Gewebe aufbaut
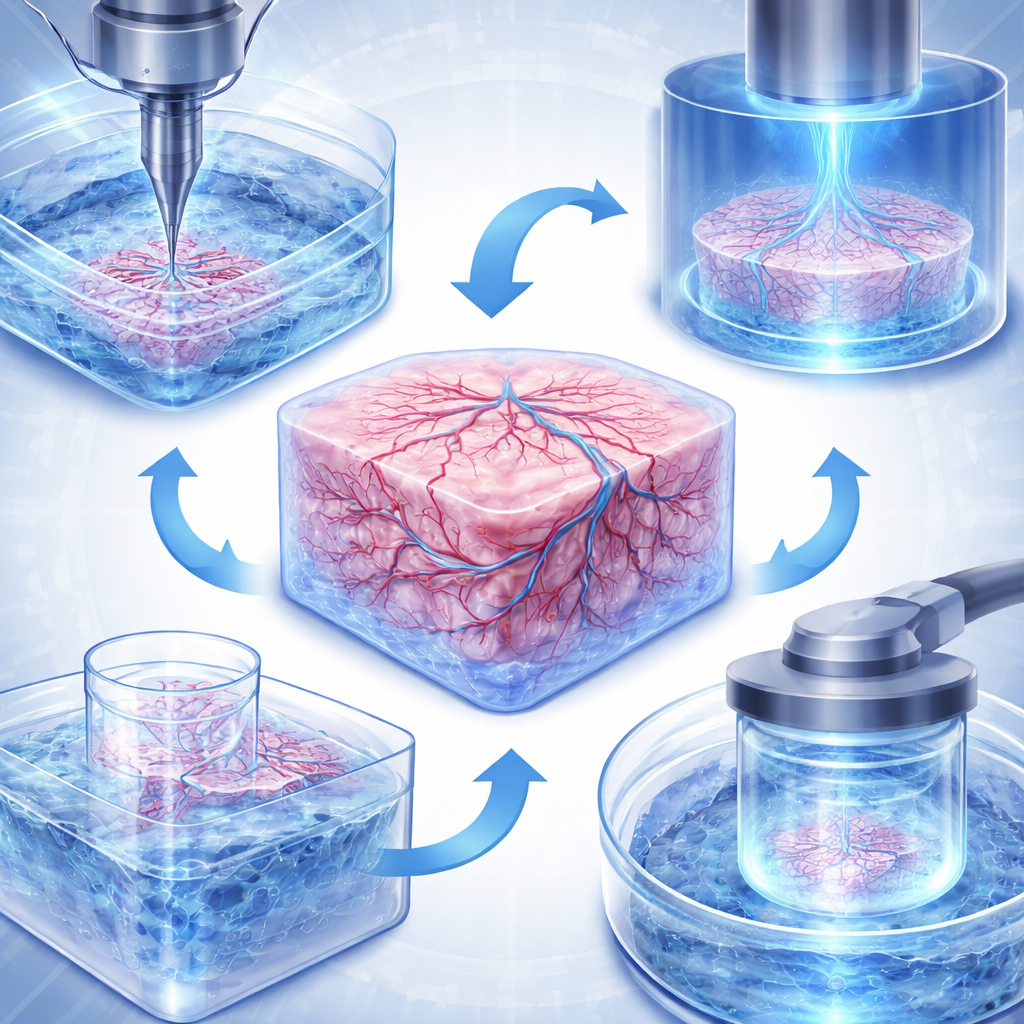
Bioprinting ist keine einzelne Technologie, sondern eine Familie von Verfahren. Inkjet‑artige Drucker versprühen winzige Tröpfchen mit zellhaltiger Flüssigkeit, um dünne Schichten mit feiner Detailauflösung zu erzeugen; dadurch eignen sie sich für Miniaturgewebe wie Hautpflaster oder Lungenbarrieren. Extrusionsdrucker pressen kontinuierliche Stränge dickerer Bioinks heraus, die viele Zellen und Stützfasern enthalten können, und erlauben so den Aufbau größerer, robusterer Strukturen wie Herzklappen, Lebertumormodelle oder Gefäßnetzwerke. Eine neuere Klasse, genannt Vat‑Photopolymerisation, richtet gemustertes Licht in eine Flüssigkeit, um komplexe Formen zu verfestigen, ohne Zellen durch Düsen pressen zu müssen. Varianten dieses Verfahrens können Mikrostrukturdetails formen, ein komplettes kleines Organ in Sekunden drucken oder Gewebe in einem transparenten Bad gestalten – und dabei die Zellen am Leben halten.
Ersetzen und Verfeinern von Arzneimitteltests
Diese gedruckten Gewebe werden bereits genutzt, um die Arzneimittel‑Pipeline neu zu denken. In der frühen Wirkstoffsuche erlauben patienten‑ oder krankheitsspezifische Konstrukte – etwa biogedruckte Tumormodelle – das Testen vieler Wirkstoffkandidaten in realistischen 3D‑Umgebungen, die der menschlichen Krankheit näherkommen als flache Zellschichten in einer Schale. In der präklinischen Prüfung erweisen sich gedruckte Haut-, Lungen‑ und Lebergewebe als genauer als Tierversuche, wenn es darum geht, menschspezifische Toxizitäten oder Nebenwirkungen zu erkennen. Manche Studien gehen noch weiter und drucken "klinische Studien auf einem Chip", bei denen Gewebe aus Zellen verschiedener Spender parallel einem Wirkstoff ausgesetzt werden, sodass sich abzeichnet, wer profitieren oder geschädigt werden könnte. Aufsichtsbehörden ermutigen Unternehmen inzwischen, Daten aus diesen Modellen neben Tierversuchen einzureichen, um die Evidenz für eine breitere Akzeptanz aufzubauen.
Organe ohne Körper entwerfen
Trotz schneller Fortschritte bleiben mehrere Hürden, bevor biogedruckte Gewebe routinemäßig Tierversuche ersetzen können. Eine große Herausforderung ist die Blutversorgung: Echte Organe enthalten Gefäßnetzwerke, die von großen Arterien bis zu haarfeinen Kapillaren reichen, während gedruckte Konstrukte die natürliche Grenze überwinden müssen, wie weit Sauerstoff und Nährstoffe durch Diffusion gelangen. Forscher begegnen dem mit neuen Druckstrategien, die verzweigende Kanäle erzeugen, mit Stützbädern, die weiche Gewebe an Ort und Stelle halten, während winzige Gefäße geformt werden, und mit blitzschnellen volumetrischen Druckern, die dicke, zellreiche Strukturen herstellen, bevor die Zellen Schaden nehmen. Eine weitere Herausforderung ist Realismus: Lebende Gewebe bestehen aus Mischungen vieler Zelltypen, sind von komplexen chemischen Signalen umgeben und werden oft vom Mikrobiom und entfernten Organen beeinflusst. Fortgeschrittene Modelle kombinieren heute mehrere Zellpopulationen, gesteuerte Gradienten von Sauerstoff und pH sowie sogar verknüpfte "Multi‑Organ"‑Systeme, die Darm, Leber, Immun‑ und Gehirngewebe über strömende Flüssigkeiten verbinden, um Ganzkörperreaktionen nachzuahmen.
Eine humane, vorhersagende Zukunft für die Arzneimittelentwicklung
Zusammen genommen deuten diese Fortschritte auf eine Zukunft hin, in der hochrealistische, humanbasierte Gewebemodelle zentral dafür werden, wie wir Medikamente bewerten. Der Artikel schließt mit der Feststellung, dass 3D‑Bioprinting sich von einer Nischen‑Labortechnik zu einem Kernwerkzeug für den Aufbau standardisierter, aufsichtsbehördenfähiger Testsysteme entwickelt. Um dieses Versprechen voll einzulösen, müssen Wissenschaftler und Regulatoren sich darauf einigen, wo und wie diese Modelle eingesetzt werden sollen, nachweisen, dass sie zuverlässig menschliche Ergebnisse vorhersagen, und verbleibende technische Probleme lösen, etwa den Aufbau stabiler Gefäßstrukturen und anatomisch komplexer Organe. Gelingt dies, könnte die Verlagerung die Abhängigkeit von Tierversuchen verringern, teure Fehlschläge in späten Entwicklungsphasen reduzieren und sicherere, wirksamere Therapien liefern – bei gleichzeitiger besseren Abbildung der Biologie, die am wichtigsten ist: unserer eigenen.
Zitation: Hua, W., Gaharwar, A.K. 3D biofabricated in vitro models as new approach methodologies for animal alternatives. npj Biomed. Innov. 3, 20 (2026). https://doi.org/10.1038/s44385-026-00073-x
Schlüsselwörter: 3D-Bioprinting, Alternativen zu Tierversuchen, Arzneimittelentwicklung, Gewebemodelle, volumetrisches Bioprinting