Clear Sky Science · de
Makrophagen für die Krebsimmuntherapie entwickeln: neue Einblicke und therapeutisches Potenzial
Die Aufräumtruppe des Körpers zu Krebsbekämpfern machen
Unser Körper ist voller Makrophagen – umherziehende „Aufräum“zellen, die Erreger und abgestorbenes Gewebe aufnehmen. Dieser Übersichtsartikel beleuchtet, wie Forschende lernen, diese Zellen gegen Krebs umzulenken. Da Makrophagen in Tumoren häufig zahlreich sind, auch in solchen, die gegen die heute führenden Immuntherapien resistent sind, könnte ihr Verständnis und gezieltes Engineering neue Optionen für Patientinnen und Patienten mit schwer behandelbaren Krebserkrankungen eröffnen.
Die vielen Gesichter eines Zelltyps
Makrophagen sind kein starrer Zelltyp; sie sind Gestaltwandler. Sie können aus dem Blut stammen oder bereits im Gewebe ansässig sein und reagieren, sobald sie sich niedergelassen haben, auf lokale Signale. In Tumoren können diese tumorassoziierten Makrophagen entweder helfen, Krebszellen zu töten, oder – paradox – das Tumorwachstum und die Ausbreitung fördern. Früher versuchten Forschende, sie in zwei Kategorien zu pressen – „M1“ (Angriffsmodus) und „M2“ (Reparatur- oder Unterstützungsmodus). Neue genetische und räumliche Kartierungswerkzeuge zeigen inzwischen ein weitaus reichhaltigeres Spektrum von Zuständen, mit mehreren Untergruppen und Verhaltensweisen, die von Tumor zu Tumor und je nach Lokalisation variieren. Selbst Zellen, die einst als fest „pro-tumoral“ eingestuft wurden, können in bestimmten Kontexten T‑Zellen mobilisieren und die anti-krebs Immunität unterstützen.
Die Umgebung spüren und Krebszellen „fressen“
Makrophagen lauschen nicht nur chemischen Signalen; sie nehmen auch die physische Welt um sie herum wahr. Wenn sie durch das dichte Proteinnetz eines Tumors kriechen, sich zwischen Zellen zwängen und Strömungskräfte ertragen, spüren sie Steifigkeit und Dehnung über spezialisierte Rezeptoren wie Piezo1. Diese mechanischen Hinweise können zusammen mit klassischen Immunreizen Makrophagen in eine stärker entzündliche oder eher beruhigende Richtung lenken. Funktionell können Makrophagen Krebszellen aufnehmen, sie dann zersetzen und Fragmente (Antigene) T‑Zellen präsentieren, wodurch angeborene und adaptive Immunität verknüpft werden. Krebszellen wehren sich, indem sie „fress mich nicht“-Signale aussenden, vor allem über das Oberflächenmolekül CD47, das eine Bremse an Makrophagen aktiviert. Wirkstoffe, die diese Interaktion blockieren, werden in vielen klinischen Studien untersucht; sie steigern die Eliminierung von Krebszellen, müssen aber sorgfältig dosiert werden, um gesunde Zellen nicht zu schädigen.
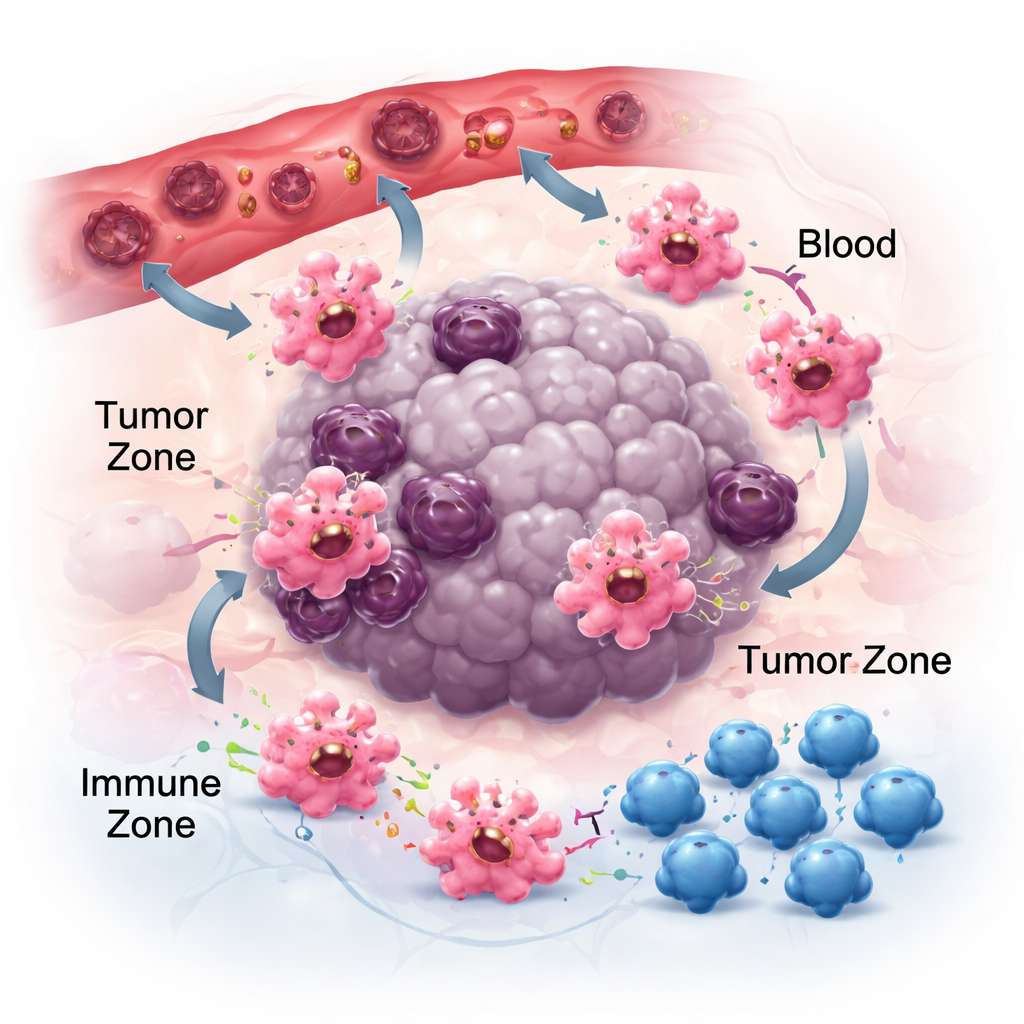
Bewegen, haften und kommunizieren in der Tumornachbarschaft
Damit Makrophagen in der Krebsbekämpfung wirken, müssen sie zuerst Tumoren erreichen und sich dann in den richtigen Nischen positionieren. Sie folgen chemischen Spuren – Chemokinen und Wachstumsfaktoren –, die von Krebs- und Nachbarzellen freigesetzt werden. Paare wie CCR2–CCL2 helfen, sie in Tumoren anzuziehen, und Wirkstoffe, die diese Signale blockieren, können die Anreicherung von Makrophagen verringern, wenn auch nicht vollständig, was auf andere Lockstoffe wie CSF‑1 und VEGF hinweist. Einmal vor Ort, beeinflusst auch, wie Makrophagen an die lokale Matrix haften, ihr Verhalten. Ihre Adhäsionsrezeptoren, Integrine genannt, wirken nicht nur als Klebstoff; sie verstärken entzündliche Signale und können Zellen in eine tumorbekämpfende Richtung stoßen. Gleichzeitig geben Makrophagen winzige Pakete, sogenannte extrazelluläre Vesikel, ab, die RNA und Proteine zu benachbarten Zellen transportieren. Je nach Tumortyp können diese Vesikel die Immunantwort dämpfen und die Ausbreitung fördern oder die Anti-Tumor-Antworten stärken – ein Hinweis auf die kontextabhängige Natur der Makrophagenkommunikation.
Makrophagen mit Genen und Materialien umprogrammieren
Da Makrophagen von Natur aus solide Tumoren besser infiltrieren als viele T‑Zellen, bauen Forschende sie inzwischen zu lebenden Therapeutika um. Eine genetische Strategie übernimmt das Konzept der chimären Antigenrezeptoren (CAR) aus der CAR‑T‑Zelltherapie: ein synthetischer Rezeptor wird eingefügt, um CAR‑Makrophagen (CAR‑M) zu erzeugen. Diese Designerzellen erkennen Tumormarker, nehmen Krebszellen effizienter auf, bauen die umgebende Matrix ab, geben entzündliche Signale ab und aktivieren T‑Zellen, indem sie Tumorantigene präsentieren. Erste klinische Studien mit HER2‑gerichteten CAR‑M zeigen ermutigende Sicherheits- und biologische Aktivität, obwohl noch mehr Arbeit nötig ist, um überzeugende, dauerhafte Vorteile nachzuweisen. Parallel dazu nutzen nicht‑genetische Ansätze Partikel und „Rucksäcke“ aus Lipiden oder Polymeren. Makrophagen können mit Wirkstoff beladene Nanopartikel aufnehmen und wie Trojanische Pferde tief in Tumoren transportieren oder Oberflächenpanele tragen, die langsam immunstimulierende Signale freisetzen und ihnen helfen, eine tumorbekämpfende Identität zu bewahren, ohne ihr Inneres zu überlasten. Auch von Makrophagen stammende Vesikel werden als natürliche, zellfreie Liefervehikel erprobt.
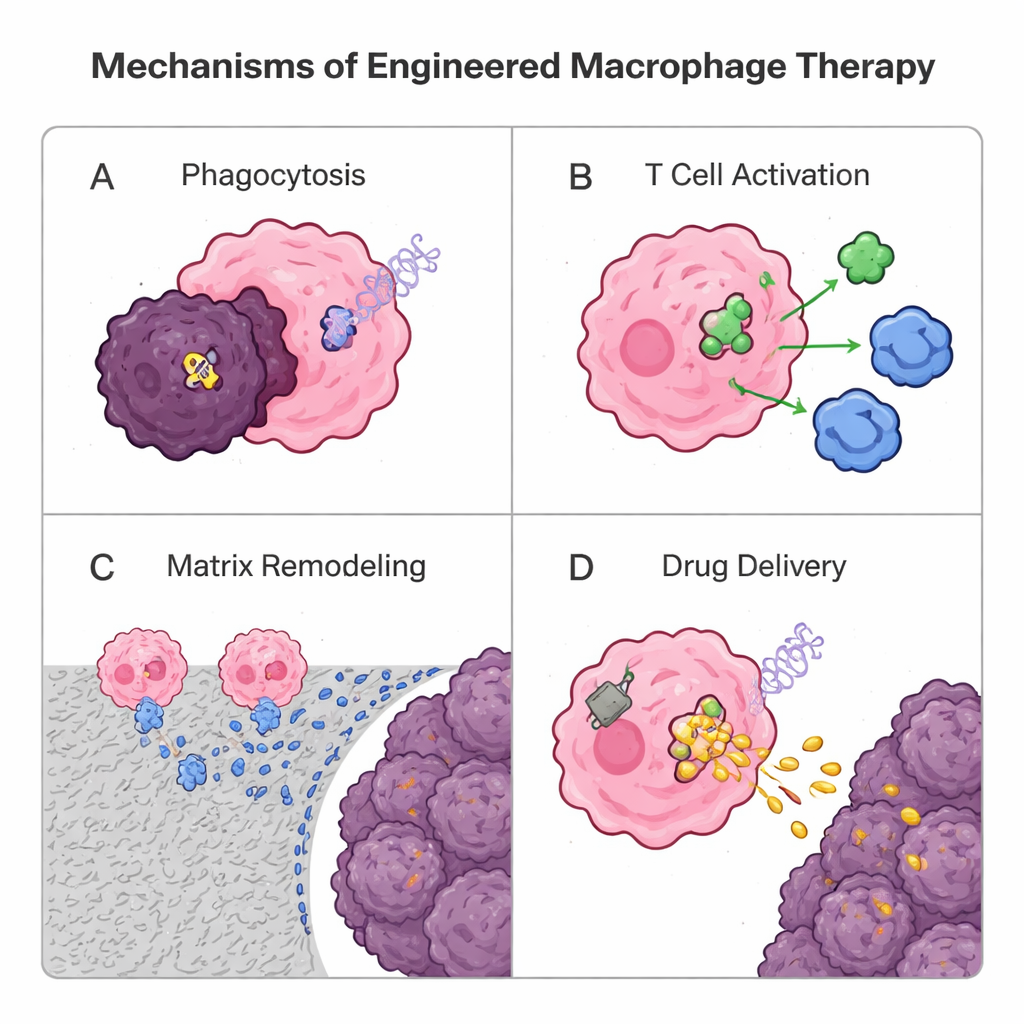
Herausforderungen und Gründe für Zuversicht
Trotz ihres Versprechens müssen Makrophagen‑Therapien praktische Hürden überwinden. Es ist zeitaufwendig und kostspielig, genügend konsistente Zellen von Patientinnen und Patienten zu gewinnen, und einmal infundiert, leben diese Zellen nicht oder vermehren sich nicht unbegrenzt. Ihre eingebaute Flexibilität, biologisch nützlich, erschwert es, sie in einem komplexen, unterdrückenden Tumormikromilieu dauerhaft in einem Anti‑Tumor‑Modus zu halten. Die Autorinnen und Autoren argumentieren, dass fortgeschrittene bioingenieurtechnische Modelle – 3D‑Kulturen, Organoide und Organs‑on‑a‑Chip‑Systeme, die echte Gewebemechanik nachahmen – entscheidend sein werden, um zu verstehen und vorherzusagen, wie entwickelte Makrophagen im Patienten verhalten. Dennoch deuten ihre natürliche Fähigkeit, in solide Tumoren einzudringen, Krebszellen zu verzehren und T‑Zellen zu aktivieren, kombiniert mit ersten Sicherheitsdaten, darauf hin, dass Makrophagenbasierte Therapien zu einer wichtigen neuen Waffe werden könnten, insbesondere gegen „kalte“ Tumoren, die derzeit den meisten Immunbehandlungen widerstehen.
Zitation: Block, A., Liu, X., Zhang, D. et al. Engineering macrophages for cancer immunotherapy: emerging insights and therapeutic potential. npj Biomed. Innov. 3, 18 (2026). https://doi.org/10.1038/s44385-026-00072-y
Schlüsselwörter: Makrophagen-Immuntherapie, tumor Mikroumgebung, CAR-Makrophagen, Phagozytose, Nanopartikel-Arzneimittelabgabe