Clear Sky Science · de
Nukleinsäurebasierte Therapeutika zur Wiederherstellung der Gelenk‑Homöostase bei altersbedingter und posttraumatischer Arthritis
Warum schmerzende Gelenke neue Arzneien brauchen
Osteoarthritis, die häufigste Form der Arthritis, wird oft als schlichtes „Verschleißphänomen“ abgetan, ist aber tatsächlich eine komplexe Erkrankung, bei der das natürliche Gleichgewicht zwischen Schädigung und Reparatur im Gelenk zusammenbricht. Da Menschen länger leben und auch im höheren Alter aktiv bleiben, werden schmerzhafte, steife Gelenke zu einer wichtigen Ursache von Behinderung, und die heutigen Behandlungen unterdrücken meist nur Symptome oder enden in kostspieligen Gelenk‑Ersatzoperationen. Dieser Übersichtsartikel untersucht eine neue Klasse von Therapien, die auf genetischen Anweisungen basieren — winzige RNA‑Stränge — und darauf abzielen, nicht nur Schmerzen zu lindern, sondern das gesunde Gleichgewicht in geschädigten Gelenken wiederherzustellen.
Vom abgenutzten Knorpel zum Zusammenbruch des ganzen Gelenks
Osteoarthritis wird heute als Ganz-Gelenk-Erkrankung verstanden, nicht nur als Problem des dünner werdenden Knorpels. In einem arthritischen Knie etwa nutzt sich der glatte Knorpel, der die Knochen polstert, ab, der Meniskus kann ausfransen, der Knochen darunter verdickt sich und die Gelenkinnenhaut entzündet sich. Diese niedriggradige, chronische Entzündung nährt die Krankheit über Jahre hinweg. Die Autoren beschreiben, wie Alter, Verletzungen, Übergewicht und genetische Faktoren zusammenwirken und das Gelenk zugunsten „kataboler“ Prozesse verschieben, die Gewebe abbauen, während die „anabolen“ Reparaturmechanismen überfordert werden. Da bei jedem Patienten ein etwas anderer Mischmasch dieser Faktoren vorliegt, variieren die Reaktionen auf gängige Behandlungen wie Schmerzmittel, Injektionen oder sogar Operationen stark, und bislang kann kein Medikament die Osteoarthritis wirklich stoppen oder umkehren.
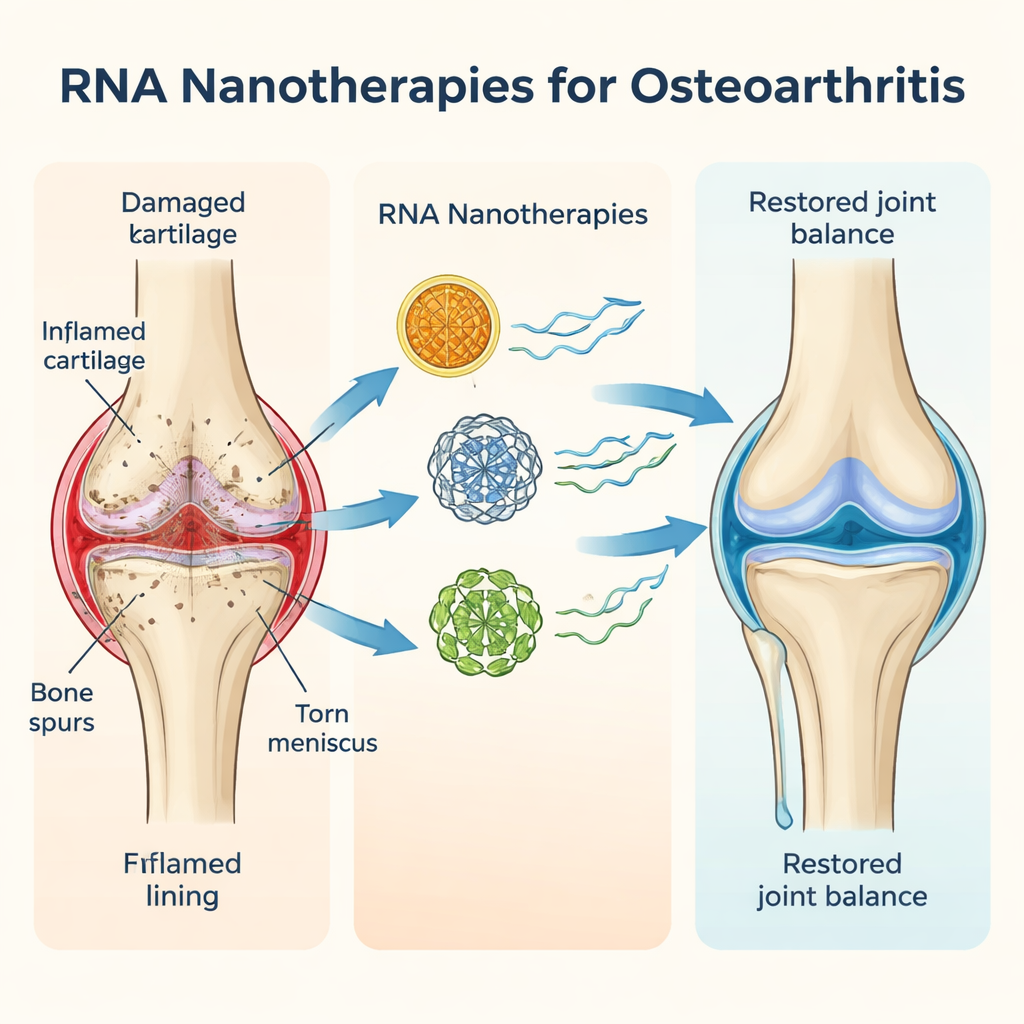
Warum traditionelle Behandlungen nicht ausreichen
Die Übersicht skizziert viele derzeitige Optionen — von rezeptfreien Schmerzmitteln und Steroidinjektionen bis zu Physiotherapie, Orthesen und fortgeschrittenen Verfahren wie Knorpelimplantaten. Jede hat Vorteile, aber auch deutliche Nachteile. Schmerzmittel können Magen oder Herz belasten, Steroide können bei wiederholter Anwendung Knorpel schädigen, und regenerative Ansätze wie plättchenreiches Plasma oder Stammzellen sind teuer und liefern keinen langfristigen Nachweis. Vor allem aber adressieren fast alle verfügbaren Medikamente nur eine Seite des Problems: Sie versuchen entweder, die Entzündung zu dämpfen und den Abbau zu verlangsamen, oder die Reparatur zu fördern. Nur wenige Ansätze greifen beide Seiten gleichzeitig an, was wahrscheinlich erklärt, warum sie die Krankheit kaum nachhaltig verändern.
RNA‑Medikamente: Das innere Skript des Gelenks neu schreiben
RNA‑basierte Therapien wirken auf einer anderen Ebene. Statt Proteine nach ihrer Herstellung zu blockieren, greifen sie in die kurzlebigen genetischen Botschaften ein, die Zellen sagen, welche Proteine sie produzieren sollen. Die Autoren konzentrieren sich auf drei Typen. Small interfering RNA (siRNA) kann ein einzelnes schädliches Gen mit hoher Präzision abschalten. MicroRNA (miRNA) kann ganze Gennetzwerke feinjustieren und mehrere schädliche Wege zugleich abschwächen. Messenger‑RNA (mRNA) bewirkt das Gegenteil: Sie liefert die Bauanleitung für nützliche Proteine, etwa Wachstumsfaktoren, die die Knorpelreparatur anregen, oder Moleküle, die entzündliche Signale blockieren. Weil RNA nur vorübergehend wirkt und die DNA nicht verändert, sind ihre Effekte reversibel und prinzipiell sicherer als dauerhafte Geneditierung. Aufbauend auf dem Erfolg der COVID‑19‑mRNA‑Impfstoffe testen Forscher inzwischen ähnliche Ideen in Tiermodellen der Arthritis.
Nanopartikel: Zerbrechliche Botschaften an die richtigen Zellen bringen
Eine große Herausforderung ist, dass nackte RNA fragil ist und nicht leicht in Zellen gelangt. Die Übersicht beschreibt, wie Wissenschaftler RNA in schützende „Nanoplattformen“ verpacken — winzige Träger aus Lipiden, Polymeren oder kurzen Peptiden. Diese Nanopartikel schützen die RNA vor Abbau, helfen ihr, die dichte Knorpelmatrix zu durchdringen, und fördern die Aufnahme durch Zellen der Gelenkinnenhaut und des Knorpels. In präklinischen Studien wurden mit siRNA beladene Partikel genutzt, um Gene auszuschalten, die Entzündung, oxidativen Stress und Gewebeabbau antreiben, während mRNA‑beladene Partikel schützende Proteine verstärkten, die Schmierung und Reparatur fördern. Erste Experimente zeigen weniger Knorpelschäden und geringere Schmerzen in Tiermodellen, was darauf hindeutet, dass sorgfältig designte Kombinationen aus anti‑abbauenden und pro‑reparativen RNAs eines Tages echte krankheitsmodifizierende Therapien sein könnten.
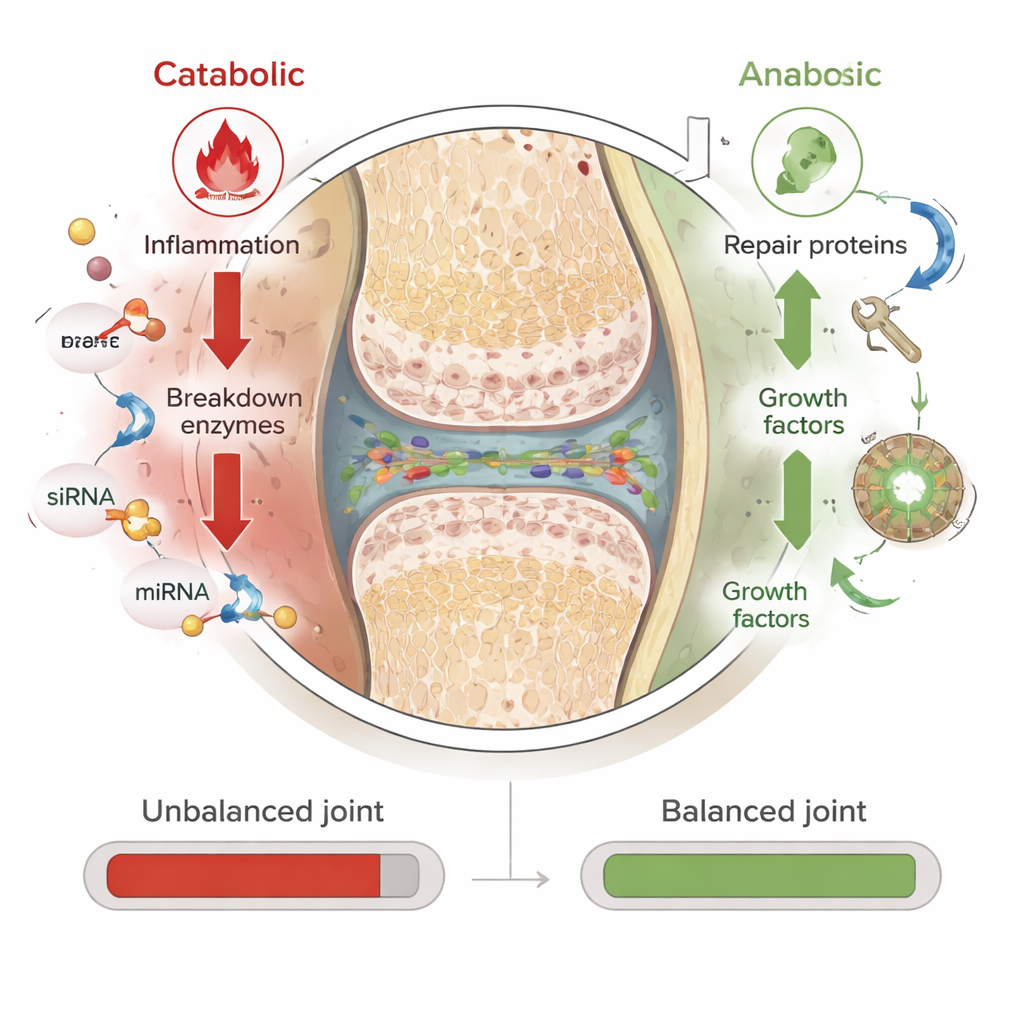
Hürden auf dem Weg zur Klinik
Trotz ihres Potenzials stehen RNA‑Nanomedikamente für Osteoarthritis noch vor wichtigen Hindernissen. Das Immunsystem kann sowohl die RNA als auch ihren Träger als Eindringlinge fehlinterpretieren und unerwünschte Entzündungen in ohnehin irritierten Gelenken auslösen. Injektionen ins Gelenk werden innerhalb von Tagen bis Wochen entfernt, sodass dauerhafte Effekte wahrscheinlich intelligentere Depot‑Systeme oder wiederholte Gaben erfordern. Die großskalige Herstellung hochwertiger RNA und Nanopartikel ist kostenintensiv, und Regulierungsbehörden haben nur begrenzte Erfahrung mit der Bewertung solcher Wirkstoffe für langsam fortschreitende Gelenkerkrankungen. Schließlich erfordert die große Variabilität der Osteoarthritis bessere Methoden, um spezifische RNA‑Kombinationen auf das individuelle Muster von Gelenkschäden und Entzündung jedes Patienten abzustimmen.
Was das für Menschen mit Arthritis bedeutet
Kurz gesagt argumentiert dieser Artikel, dass zukünftige Behandlungen Menschen mit Osteoarthritis wirklich helfen müssen, indem sie mehr tun als nur Schmerzen abzufedern — sie müssen das verlorene Gleichgewicht des Gelenks wiederherstellen, indem sie die Gene herunterregulieren, die Schaden verursachen, und die Gene hochregulieren, die Reparaturprozesse unterstützen. RNA‑basierte Medikamente, geliefert durch ausgeklügelte Nanopartikel‑Träger, bieten ein flexibles Instrumentarium, genau dies zu erreichen. Obwohl sie noch nicht klinisch verfügbar sind und wichtige Fragen zu Sicherheit, Wirkdauer, Kosten und Zulassung offen bleiben, sehen die Autoren in ihnen einen realistischen Weg zu personalisierten, minimalinvasiven Therapien, die den Bedarf an Gelenkersatz bei altersbedingter und verletzungsbedingter Arthritis verzögern oder sogar verhindern könnten.
Zitation: Rai, M.F., Pham, C.T., Hou, K. et al. Nucleic acid-based therapeutics to restore joint homeostasis in age-related and post-traumatic arthritis. npj Biomed. Innov. 3, 17 (2026). https://doi.org/10.1038/s44385-026-00068-8
Schlüsselwörter: Osteoarthritis, RNA-Therapeutika, Nanomedizin, Gelenkregeneration, siRNA mRNA miRNA