Clear Sky Science · de
Beschleunigte personalisierte Medizin: miniaturisierte patientenabgeleitete Organoid-Drug-Screenings zur Vorhersage von Krebsbehandlungsreaktionen und darüber hinaus
Das Labor schneller an die Krankenbettkante bringen
Für viele Menschen mit fortgeschrittenem Krebs kann das wochenlange Warten darauf, ob eine Chemotherapie wirkt, qualvoll sein. Diese Studie untersucht einen Weg, diese Zeitspanne mithilfe winziger, im Labor gezüchteter Nachbildungen des Tumors eines Patienten – sogenannten Organoiden – zu verkürzen, um Medikamente vorab zu testen. Durch Verkleinerung und Automatisierung des Testverfahrens wollen die Forschenden vorhersagen, welche Behandlungen wahrscheinlich helfen, und zwar mit deutlich weniger Gewebe und in kürzerer Zeit als bei den derzeitigen Methoden.
Mini-Tumoren in der Schale
Patientenabgeleitete Organoide sind dreidimensionale Zellverbände, die aus dem eigenen Tumor einer Person gezüchtet werden. Im Gegensatz zu herkömmlichen zweidimensionalen Zellkulturen bewahren diese Mini-Tumoren einen Großteil der genetischen Vielfalt und des Verhaltens des ursprünglichen Krebses. Frühere Arbeiten haben gezeigt, dass Organoid-Antworten – bzw. deren Ausbleiben – auf ein Medikament im Labor häufig den klinischen Reaktionen der Patienten entsprechen. Das Problem ist, dass Standardtests mit Organoiden Hunderte von Organoiden pro Vertiefung einsetzen, viel Biopsiematerial erfordern und viele Wochen dauern, was ihren praktischen Einsatz für Patienten, die schnell mit einer Behandlung beginnen müssen, einschränkt.
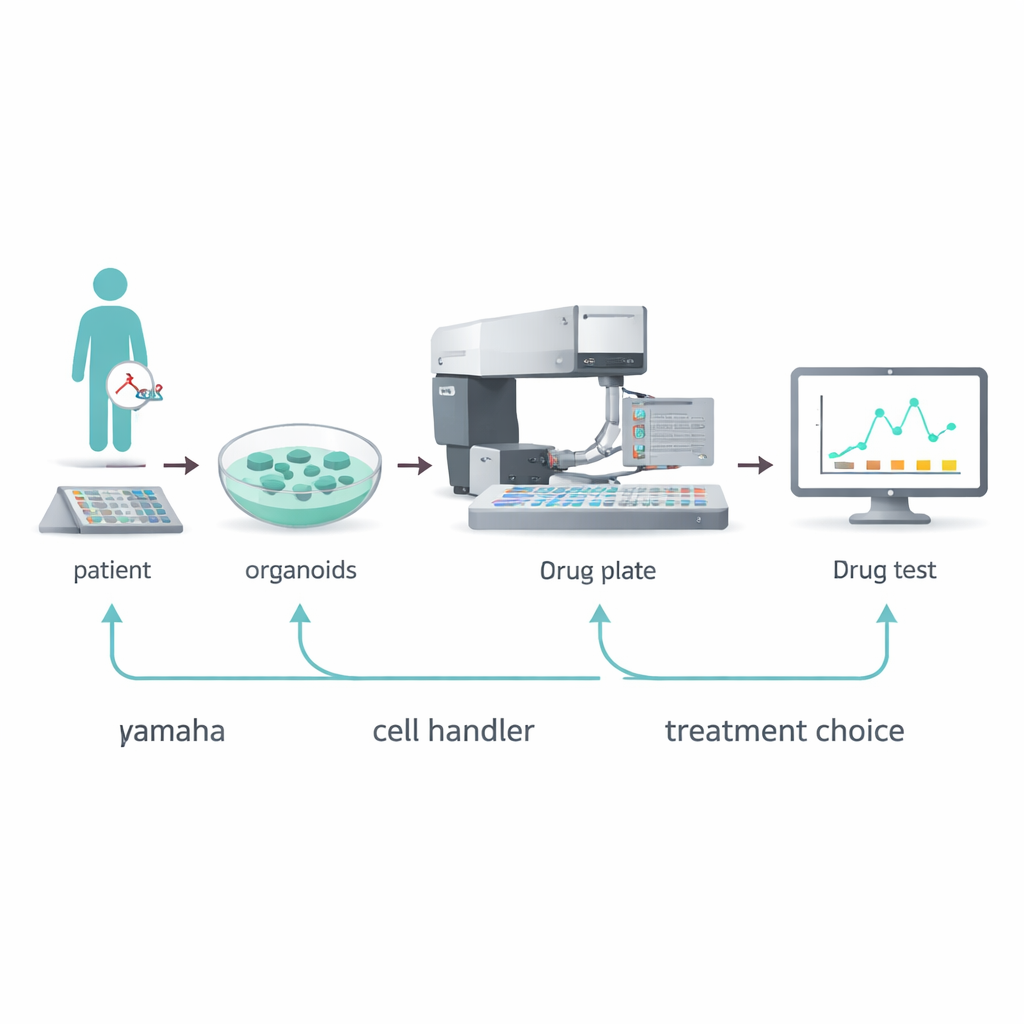
Ein Roboter-Picker für winzige Tumoren
Das Team setzte ein automatisiertes Gerät, den Yamaha Cell Handler, ein, um diese Engpässe zu überwinden. Dieser Roboter nutzt eine Kamera, um einzelne Organoide in einer Quellplatte zu erkennen, analysiert deren Größe und Form, hebt ausgewählte Organoide schonend an und setzt sie in die winzigen Vertiefungen einer 384-Well-Platte ab. Durch Feinabstimmung der Anzahl der ausgesäten Organoide, ihrer Unterstützung in einer gelartigen Matrix sowie der verwendeten Farbstoffe und Messparameter stellten die Forschenden fest, dass bereits 5 bis 10 Organoide pro Vertiefung für verlässliche Wirkstofftests ausreichten. Sie optimierten außerdem einen DNA-basierten Fluoreszenztest, der berichtet, wie viele Zellen nach der Medikamentenexposition noch leben, und damit einige Fallstricke älterer energiebasierter Tests vermeidet.
Mehr erreichen mit weit weniger Zellen
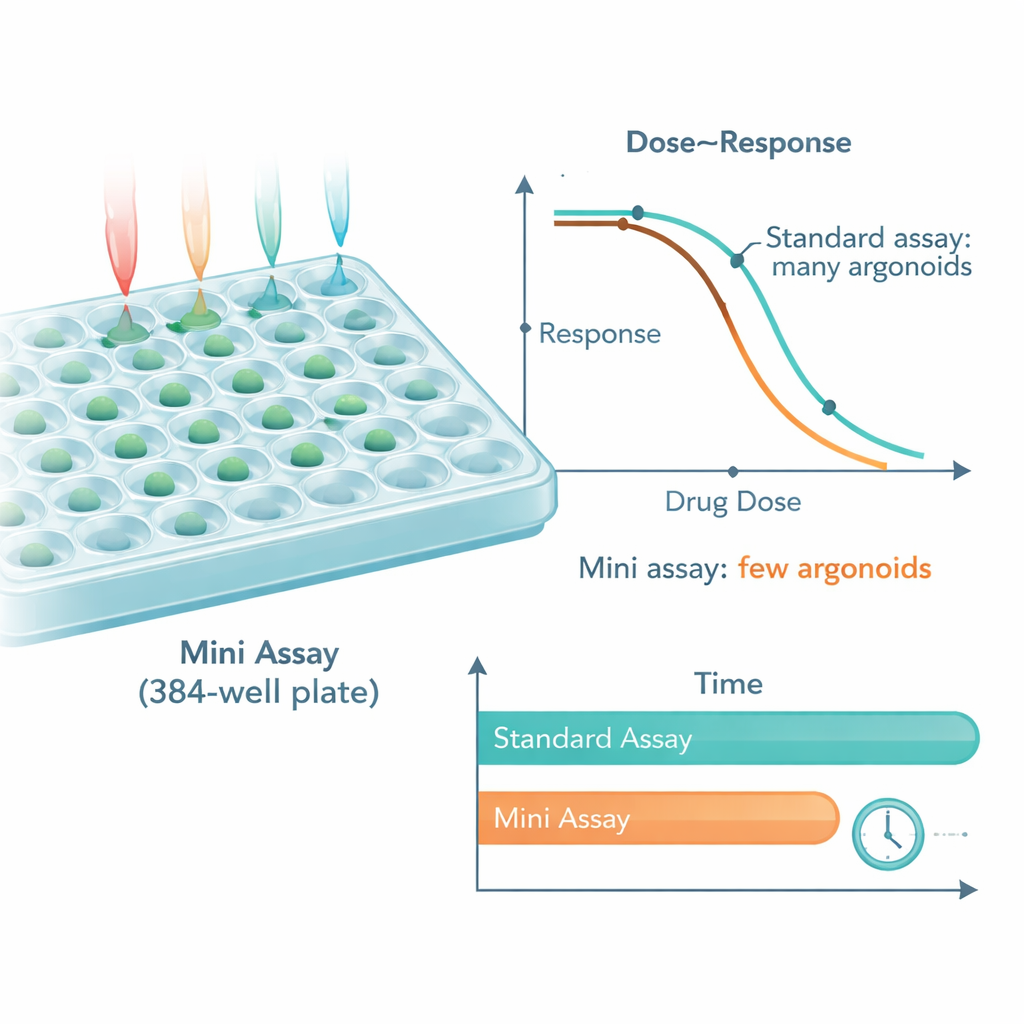
Nach der Optimierung benötigte das miniaturisierte System nur noch zwischen etwa 0,5 % und etwa 5 % des Materials, das für konventionelle Screens erforderlich ist, und senkte damit den Organoid-Bedarf um das 25-Fache. Trotz dieser drastischen Verkleinerung stimmten die Muster der gemessenen Wirkstoffempfindlichkeit mit 10 Organoiden pro Vertiefung eng mit denen überein, die bei 250 Organoiden pro Vertiefung beobachtet wurden. Die Plattform konnte sogar verborgene Unterschiede innerhalb eines einzigen Tumormodells eines Patienten aufdecken, etwa Untergruppen von Organoiden, die empfindlich bzw. resistent gegenüber einer gängigen Chemotherapie waren. In einem Beispiel mit einer zielgerichteten Antikörpertherapie verhielten sich Organoide aus Tumoren mit einer bekannten Resistenzmutation wie erwartet – sie reagierten nicht –, während Organoide ohne diese Mutation stark gehemmt wurden, unabhängig davon, ob sie im Standard- oder im miniaturisierten Format getestet wurden.
Von Laborsignalen zu Patientenergebnissen
Die Forschenden fragten dann, ob dieser schlankere Test noch reale Patientenerfahrungen widerspiegelt. Sie testeten Organoide von Menschen mit metastasiertem kolorektalem Krebs, die klinisch Standardchemotherapien erhalten hatten. Sowohl für 5‑Fluorouracil als auch für Oxaliplatin stimmten die in miniaturisierten Assays gemessenen Arzneimittelreaktionen (mit nur 5–10 Organoiden pro Vertiefung und weniger Wirkstoffkonzentrationen) stark mit den Ergebnissen größerer, traditioneller Screens überein. Wichtiger für die Patienten war, dass die Empfindlichkeit der Organoide im Mini-Assay mit der Zeit korrelierte, in der die Krebserkrankungen unter Kontrolle blieben, und in vielen Fällen mit dem Gesamtüberleben. Die Reduktion der Organoidzahl schwächte diese Zusammenhänge nicht, was darauf hindeutet, dass der straffere Ansatz weiterhin klinisch aussagekräftig ist.
Was das für Patienten bedeuten könnte
Indem die Studie zeigt, dass genaue Wirkstoffreaktionstests mit deutlich weniger Organoiden und einem schnelleren Arbeitsablauf möglich sind, rückt sie die organoidbasierte Präzisionsmedizin näher an die routinemäßige klinische Praxis. Die neue automatisierte Plattform reduziert sowohl die benötigte Zellzahl als auch die Durchlaufzeit um ungefähr die Hälfte, wodurch es realistischer wird, Organoide aus einer Biopsie zu züchten, mehrere Therapien zu testen und Ergebnisse rechtzeitig zur Steuerung von Behandlungsentscheidungen zurückzugeben. Obwohl weitere Validierungen über mehr Krebsarten hinweg nötig sind, bietet diese miniaturisierte Organoid-Screening-Strategie einen praktischen Weg, Krebsmedikamente auf Grundlage des Verhaltens des individuellen Tumors im Labor auszuwählen, statt sich allein auf Durchschnittswerte aus der Population zu stützen.
Zitation: Abouleila, Y., Smabers, L.P., Voskuilen, T. et al. Accelerating personalized medicine: miniaturized patient-derived organoid drug screening for predicting cancer treatment responses and beyond. npj Biomed. Innov. 3, 16 (2026). https://doi.org/10.1038/s44385-026-00067-9
Schlüsselwörter: Krebs-Organoide, personalisierte Medizin, Wirkstoffscreening, kolorektaler Krebs, Automatisierung in der Onkologie