Clear Sky Science · de
Optimierung der Auslösung von Entzündungen in aus Frühgeborenen stammenden intestinalen Epithel-Organoiden
Warum das für verletzliche Neugeborene wichtig ist
Sehr früh geborene Babys stehen vor einer gefährlichen Kombination: ein unreifer Darm und eine sich schnell verändernde Mikrobiota. Zusammen können diese eine außer Kontrolle geratene Entzündung auslösen, die den Darm schädigt und zu lebensbedrohlichen Zuständen wie der nekrotisierenden Enterokolitis führt. Da direkte Experimente an Frühgeborenen nicht möglich sind, brauchen Forschende realistische Labormodelle ihres Darms, um zu prüfen, was Entzündungen antreibt und wie man sie stoppen kann. Diese Studie verfeinert ein solches Modell mit winzigen, im Labor gezüchteten Darmgeweben und bietet eine klarere Methode, um zu untersuchen, welche mikrobiellen Signale das Gleichgewicht von normaler Abwehr zu schädlicher Entzündung kippen.
Ein Darm aus der Petrischale
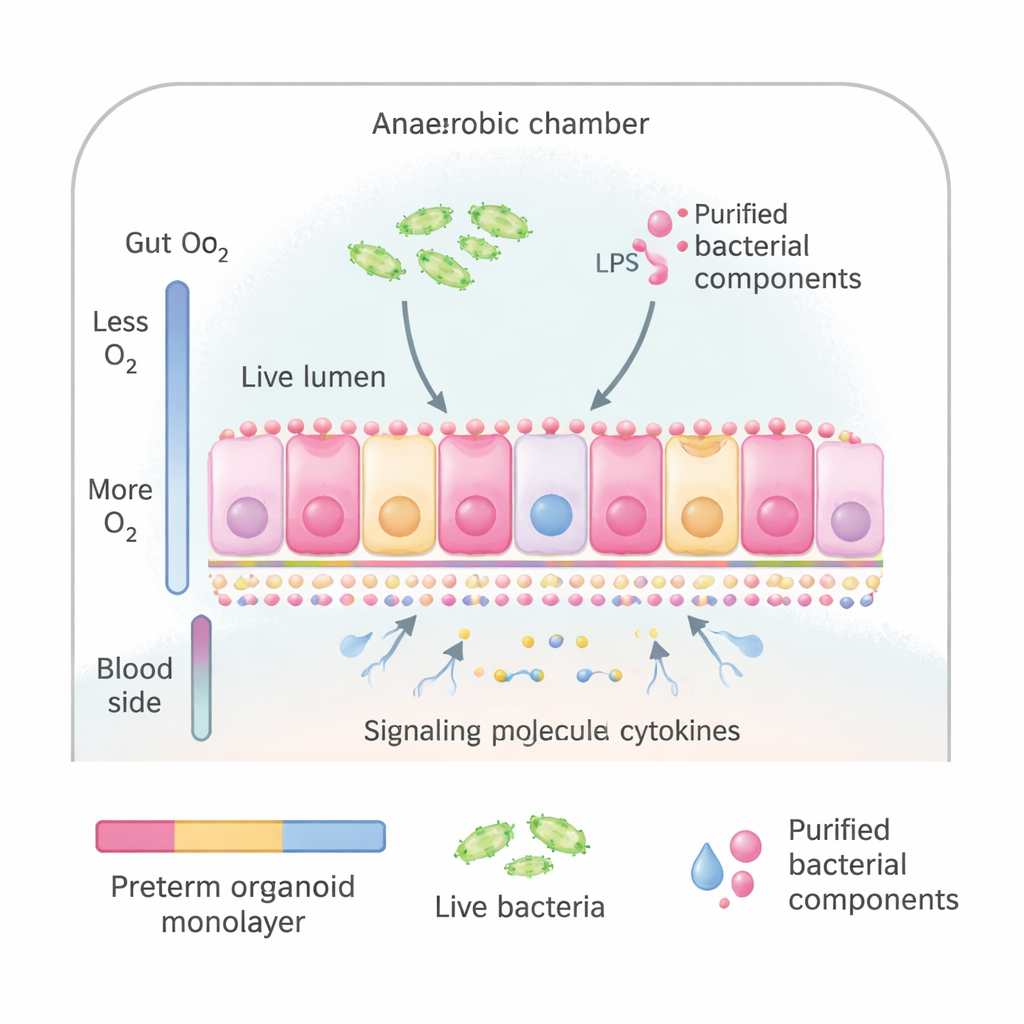
Die Forschenden nutzten intestine Organoide—miniaturisierte Versionen der Darmschleimhaut, gezüchtet aus Stammzellen, die bei Operationen von Frühgeborenen entnommen wurden. Diese Organoide lassen sich zu einer dünnen Zellschicht ausbreiten, die der inneren Oberfläche des Dünndarms in Aussehen und Funktion sehr ähnelt, einschließlich der korrekten Orientierung (oben: zum Darminhalt, unten: zum Blut). Das Team platzierte diese Zellschichten in einem speziellen Kultursystem, das das natürliche Sauerstoffgefälle des Darms nachahmt: niedrige Sauerstoffwerte an der mikrobenexponierten Seite und höhere Werte an der blutzugewandten Seite. So konnten sie die „Darm“-Oberfläche entweder ganzen Bakterien entnehmen, die von Frühgeborenen stammten, oder gereinigten bakteriellen Komponenten aussetzen, die das Immunsystem bekanntlich alarmieren.
Testen, was am stärksten einen Entzündungsalarm auslöst
Die Wissenschaftler verglichen mehrere Methoden, Entzündungen zu provozieren: ein Gemisch lebender Bakterien, das häufig bei kranken Frühgeborenen gefunden wird; dieselben Bakterien nach Hitzetötung; und zwei gereinigte bakterielle Signale, Lipopolysaccharid (LPS) aus bakteriellen Zellwänden und Flagellin aus bakteriellen Geißeln. Sie maßen die Freisetzung von IL‑8, einem Signalmolekül, das Immunzellen anzieht und als allgemeiner Marker für Entzündung dient, und führten groß angelegte Proteinanalysen durch, um zu sehen, wie sich die zellulären Abläufe veränderten. Überraschenderweise erhöhten lebende oder tote Bakterien in diesem System IL‑8 nicht stark, selbst nach 24 Stunden. Im Gegensatz dazu lösten Flagellin und besonders die Kombination aus Flagellin und LPS bereits nach drei Stunden einen deutlichen Anstieg von IL‑8 aus, was zeigt, dass diese gereinigten Signale zuverlässig einen entzündlichen Zustand aktivieren können.
Das realistischste und effizienteste Setup finden
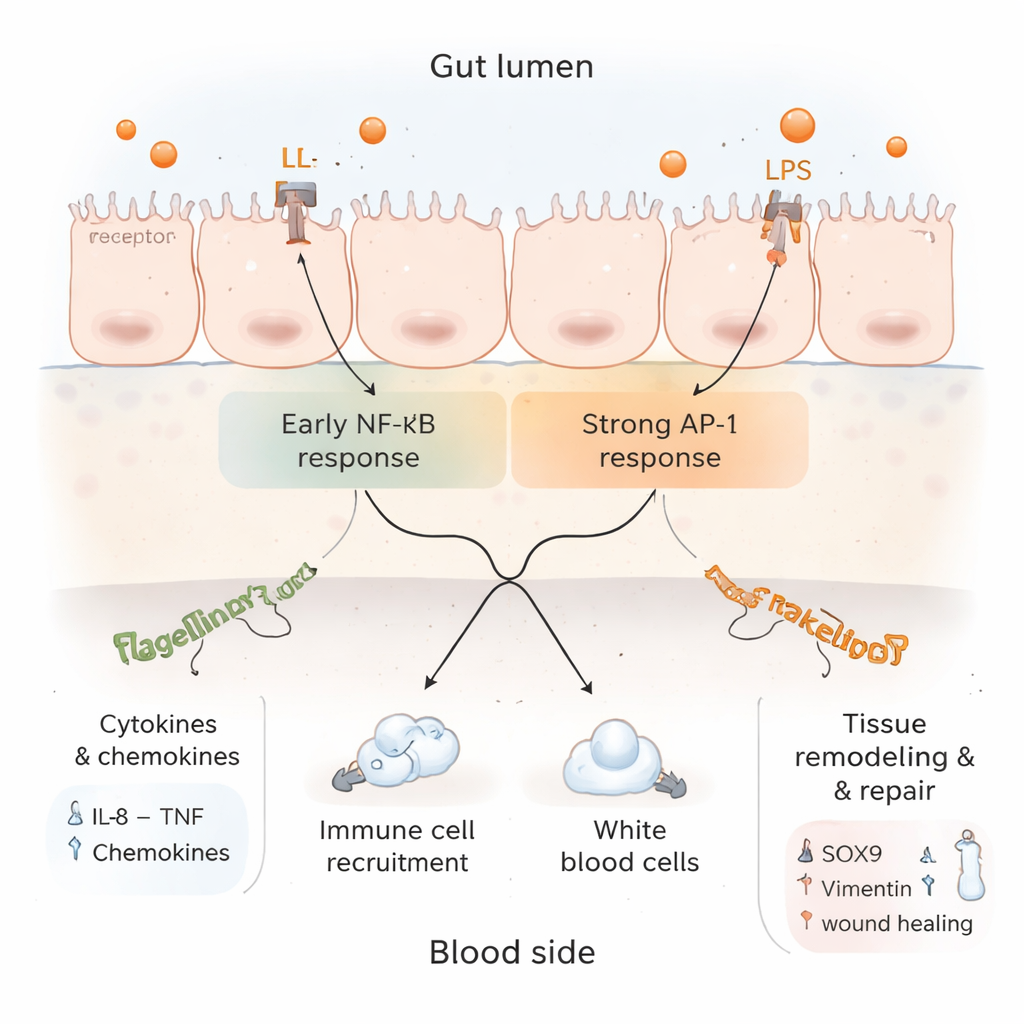
Um der echten Darmbiologie näherzukommen, achtete das Team als Nächstes darauf, wo jedes Signal natürlicherweise wirkt. LPS wird üblicherweise auf der zum Darminhalt gewandten Seite der Schleimhaut wahrgenommen, während Flagellin überwiegend von der gewebezugewandten Seite erkannt wird. Mit deutlich niedrigeren, physiologisch realistischeren Dosen als in früheren Experimenten applizierten sie LPS an die obere (luminal gerichtete) Seite und Flagellin an die untere (blutgerichtete) Seite der Organoid-Schicht. Diese einfache Änderung erzeugte innerhalb von drei Stunden eine starke und breit gefächerte Reaktion: mehrere entzündliche Botenstoffe—darunter IL‑8, TNF und mehrere Chemokine—wurden von beiden Seiten des Gewebes ausgeschüttet. Gleichzeitig veränderte sich die Menge von Hunderten zellulärer Proteine, was auf eine großflächige Aktivierung von Abwehrwegen hinweist.
Entzündung, Bremsen und Reparatur im selben Modell
Ein Blick tiefer in die Proteindaten offenbarte ein komplexes Bild. Einerseits waren Marker aktiver Entzündung und Rekrutierung von Immunzellen erhöht, und Signalwege, die mit TNF und IL‑17 verbunden sind—beide zentral für die Darmimmunabwehr—wurden aktiviert. Andererseits waren mehrere Komponenten des klassischen NF‑κB-Wegs, der viele entzündliche Gene antreibt, herunterreguliert, während ein alternativer Weg über AP‑1 weiter aktiv blieb. Das deutet darauf hin, dass das Gewebe nach dem ersten Alarm versucht, Bremsen zu betätigen, um unkontrollierte Schäden zu verhindern. Gleichzeitig waren Proteine erhöht, die mit Geweberegeneration, struktureller Umgestaltung und kontrolliertem Zelltod assoziiert sind, was darauf hindeutet, dass die Darmschleimhaut nicht nur entzündet ist, sondern auch versucht, sich umzubauen und zu heilen.
Was das für künftige Therapien bedeutet
Durch den systematischen Vergleich verschiedener mikrobieller Stimuli, Dosen, Positionen und Expositionszeiten kommen die Autoren zu dem Schluss, dass eine dreistündige Exposition gegenüber niedrig dosiertem LPS auf der Darmseite zusammen mit Flagellin auf der Blutseite die robusteste und reproduzierbarste Methode ist, Entzündungen in aus Frühgeborenen stammenden intestinalen Organoiden auszulösen. Dieses verfeinerte Modell erfasst nicht nur das Aufflammen der Entzündung, sondern auch die eingebauten Bremsen, Toleranzmechanismen und Reparaturreaktionen des empfindlichen Frühgeborenendarms. Es bietet ein praktisches Vorbild für andere Laboratorien, um zu untersuchen, wie spezifische Mikroben, Medikamente oder Nährstofffaktoren Darmentzündungen bei sehr frühgeborenen Säuglingen verschlechtern oder beruhigen könnten—ein entscheidender Schritt hin zu sichereren, zielgerichteten Strategien zur Vorbeugung verheerender Darmerkrankungen in dieser verletzlichen Gruppe.
Zitation: Chapman, J.A., Frey, A.M., Dueñas, M.E. et al. Optimising the induction of inflammation within preterm infant-derived intestinal epithelial organoids. npj Gut Liver 3, 5 (2026). https://doi.org/10.1038/s44355-026-00054-2
Schlüsselwörter: Darm von Frühgeborenen, intestinale Organoide, Darmentzündung, Mikrobiom, nekrotisierende Enterokolitis