Clear Sky Science · de
Ultrasensible enzymfreie Proteinerkennung mittels Proximity‑Immunoassay und photonic resonator absorption microscopy
Warum das Auffinden winziger Proteinspuren wichtig ist
Ärzte und Forscher verlassen sich zunehmend auf Proteine im Blut, um frühzeitig vor Krebs, Herzkrankheiten, Infektionen oder schädlichen Entzündungen zu warnen, oft lange bevor Symptome schwerwiegend werden. Viele dieser molekularen Warnsignale treten jedoch in so geringen Konzentrationen auf, dass Standardlabortests Schwierigkeiten haben, sie schnell oder kostengünstig nachzuweisen. Diese Studie stellt eine neue Testmethode vor, PINATA genannt, die extrem kleine Mengen eines mit Entzündungen verbundenen Proteins erkennen kann, dabei einfache Geräte und Arbeitsschritte bei Raumtemperatur nutzt und so zugänglichere und sensiblere Diagnostik ermöglicht.
Ein neuer Weg, Proteine in ablesbare Signale zu verwandeln
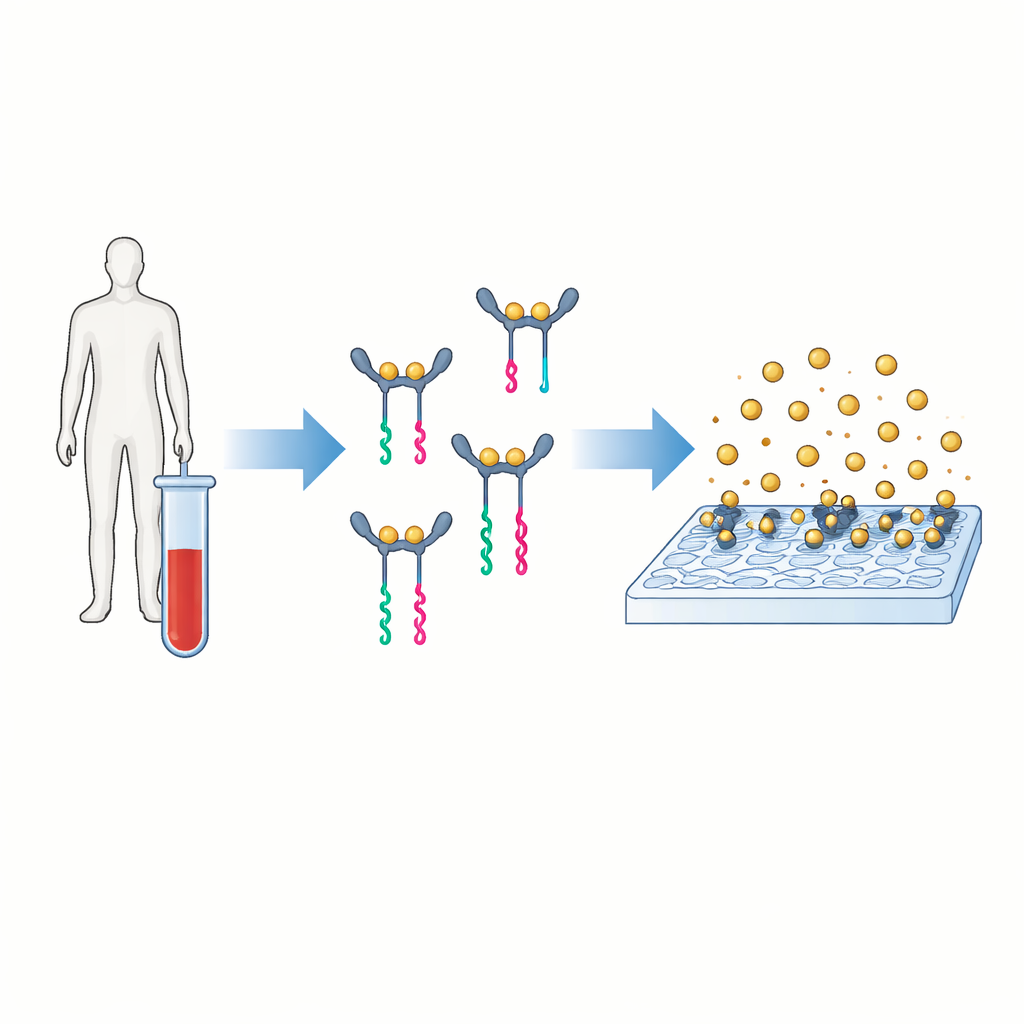
Die Kernidee von PINATA ist, das Vorhandensein eines Proteins in ein kurzes DNA‑Stück zu übersetzen, das sich leicht vervielfältigen und zählen lässt. Die Autoren konzentrieren sich auf Interleukin‑6, ein Botenmolekül im Blut, das bei Zuständen von Infektionen bis hin zu Krebs ansteigt. In herkömmlichen Tests binden zwei Antikörper an das Protein und tragen ein Enzym, das ein farbiges oder fluoreszierendes Signal erzeugt. PINATA behält die grundlegende Idee bei, dass zwei Antikörper dasselbe Protein erkennen, ersetzt die Enzyme jedoch durch kurze DNA‑Stränge, die an jeden Antikörper gekoppelt sind. Wenn beide Antikörper dasselbe Protein binden und sich annähern, wirken ihre DNA‑Partner zusammen, um ein separates DNA‑Fragment freizusetzen, den sogenannten Reporter. Jedes Proteinmolekül kann so die Freisetzung vieler identischer DNA‑Reporter auslösen.
DNA-‚Verkehrsregeln‘ statt Enzyme
Im Zentrum der Methode stehen sorgfältig konstruierte DNA‑Schaltkreise, die wie molekulare Verkehrssysteme funktionieren und steuern, wann Stränge binden, sich lösen oder Partner tauschen dürfen. Diese Schaltkreise sind so aufgebaut, dass der Reporter‑DNA dort blockiert bleibt und kein Signal entsteht, sofern nicht ein Protein die beiden an Antikörper gebundenen DNA‑Teile zusammenführt. Ist das Protein vorhanden, befreit dessen Brückenwirkung den Reporter. Dieser freigesetzte Reporter beteiligt sich dann an einem sekundären Amplifikationsprozess auf einer vorbereiteten Oberfläche. Dort geht er wiederholt Strand‑Austauschreaktionen ein, die es einem einzelnen Reporter ermöglichen, viele Goldnanopartikel an der Oberfläche zu rekrutieren und so ein starkes digitales Signal zu erzeugen — ganz ohne Enzyme oder Temperaturzyklen.
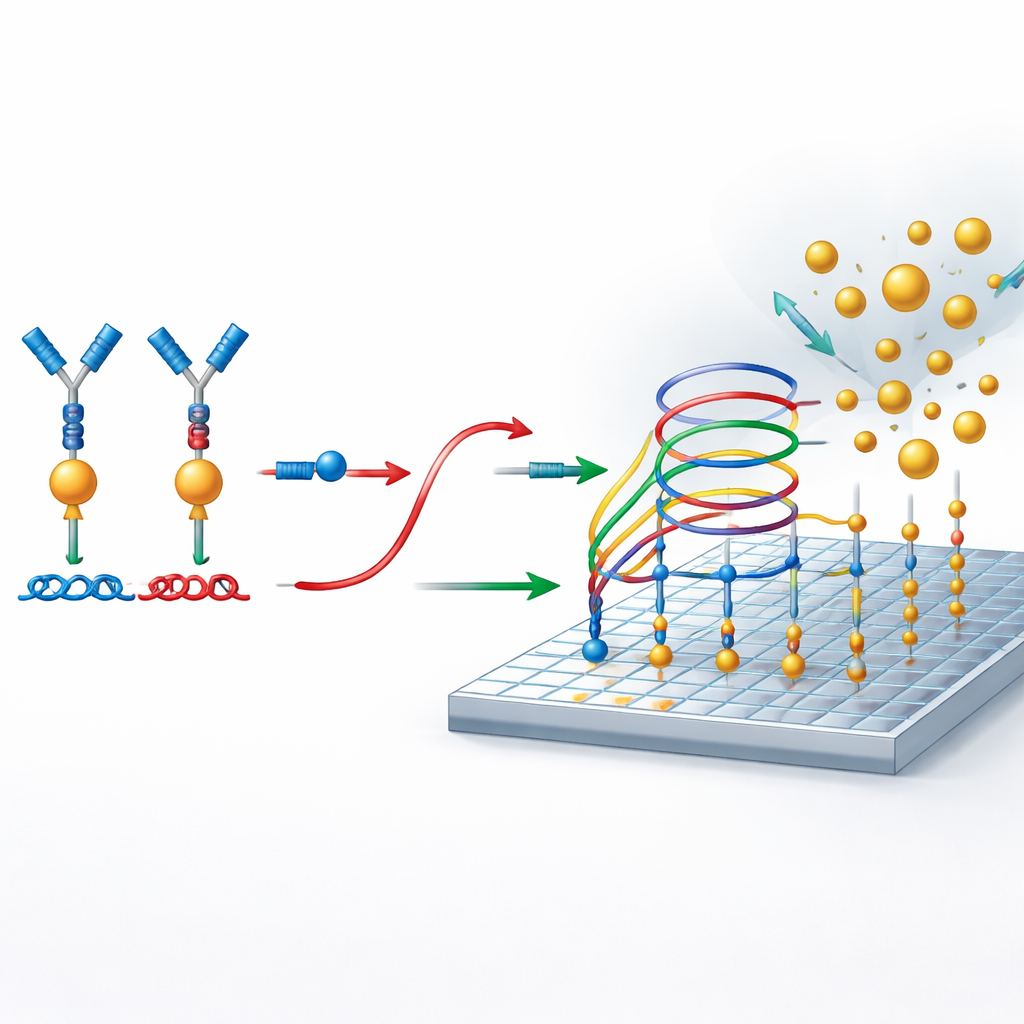
Einzelne Nanopartikel als Ja‑/Nein‑Ereignisse zählen
Zur Auslese nutzen die Forscher photonic resonator absorption microscopy (PRAM). Die Messoberfläche besteht aus einem speziell strukturierten Material, das Licht einer bestimmten Farbe stark reflektiert. Landen Goldnanopartikel auf dieser Oberfläche, absorbieren sie dieses Licht und erscheinen als dunkle Punkte im Mikroskopbild. Da das System so gestaltet ist, dass Nanopartikel nur binden, wenn Reporter‑DNA vorhanden ist, repräsentiert jeder dunkle Punkt ein erfolgreiches Detektionselement, das auf ein Proteinmolekül zurückgeführt werden kann. Eine einfache, kostengünstige optische Ausstattung und Bildverarbeitungssoftware zählen diese Punkte über die Oberfläche und wandeln die Anzahl der Nanopartikel in eine präzise Messung der Proteinkonzentration um.
Wie sensibel und selektiv ist der Test?
Mit diesem Ansatz zeigen die Autoren, dass sie Interleukin‑6 in Konzentrationen von bis zu 37 Femtogramm pro Milliliter nachweisen können — grob gesagt wenige Dutzend Moleküle in einem Tropfen — über einen dynamischen Bereich, der sechs Größenordnungen umfasst. Der Assay arbeitet in einem einfachen zweistufigen, 90‑minütigen Protokoll, das vollständig bei Raumtemperatur durchgeführt wird. Die Autoren demonstrieren außerdem, dass der Test auch dann genau bleibt, wenn Interleukin‑6 in komplexe Proben wie menschliches Serum und Plasma eingemischt ist, die empfindliche Messungen typischerweise stören. Sie bestätigen zudem, dass die gegen Interleukin‑6 gerichteten Antikörper nicht auf andere, verwandte Proteine reagieren, was die Selektivität des Assays unterstreicht.
Was das für die Diagnostik der Zukunft bedeuten könnte
Für Nichtfachleute ist die wichtigste Erkenntnis, dass PINATA eine Möglichkeit bietet, krankheitsrelevante Proteine auf extrem niedrigen Niveaus mit einem kompakten optischen Instrument statt sperriger, teurer Laborgeräte nachzuweisen. Durch die Kombination intelligenter DNA‑Schaltkreise mit digitaler Zählung von Nanopartikeln umgeht die Methode empfindliche Enzyme und Aufheizschritte, erreicht dabei jedoch die Empfindlichkeit vieler fortgeschrittener Proteintests oder übertrifft sie sogar. Mit weiterer Entwicklung und Anpassung an andere Zielmoleküle könnte diese Strategie frühere Diagnosen, häufigeres Monitoring und Point‑of‑Care‑Tests für eine breite Palette von Erkrankungen ermöglichen, bei denen winzige Änderungen des Proteingehalts große klinische Bedeutung haben.
Zitation: Shepherd, S., Bhaskar, S., Xu, H. et al. Ultrasensitive non-enzymatic protein detection using proximity immunoassay with photonic resonator absorption microscopy. npj Biosensing 3, 21 (2026). https://doi.org/10.1038/s44328-026-00090-1
Schlüsselwörter: Nachweis von Protein-Biomarkern, ultrasensible Diagnostik, DNA-Strangverdrängung, Interleukin-6-Assay, digitale Biosensorik