Clear Sky Science · de
Mikrofluidisch nanomagnetisch isolierte aus Neuronen und Astrozyten stammende extrazelluläre Vesikel zur Unterscheidung von Lewy-Körper- und Alzheimer-Erkrankung
Warum das für Familien und Ärztinnen und Ärzte wichtig ist
Demenz ist ein Sammelbegriff für mehrere Hirnerkrankungen, die ähnliche Symptome zeigen, aber sehr unterschiedliche Ursachen haben. Zwei der häufigsten Formen, Alzheimer-Erkrankung und Lewy-Körper-Erkrankung, können klinisch beinahe gleich aussehen, sprechen jedoch unterschiedlich auf Medikamente an und bringen unterschiedliche Risiken mit sich. Heute lässt sich mit Sicherheit feststellen, welche Krankheit vorlag, meist nur durch Untersuchung des Gehirns nach dem Tod. Diese Studie beschreibt einen neuen Bluttest, der winzige Botschaften aus Gehirnzellen liest, mit dem Ziel, diese beiden Demenzformen schon zu Lebzeiten voneinander zu unterscheiden.
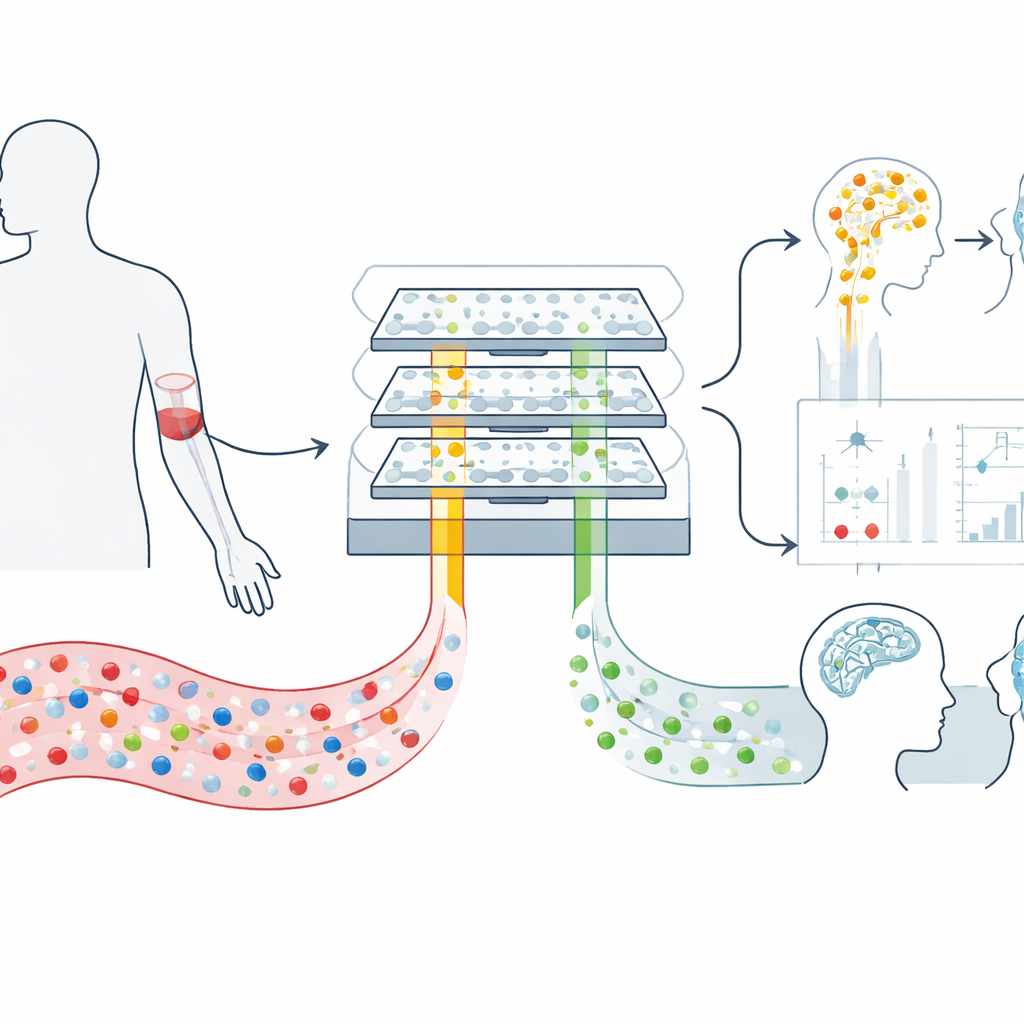
Kleine Pakete, die vom Gehirn ins Blut reisen
Unser Gehirn schleust ständig mikroskopisch kleine Bläschen, sogenannte extrazelluläre Vesikel, ins Blut. Diese Vesikel sind wie gepolsterte Umschläge, die von Nervenzellen und deren Stützzellen verschickt werden und Stücke von genetischem Material und Proteinen transportieren, die widerspiegeln, was im Gehirn vor sich geht. Weil sie die Blut‑Hirn-Schranke passieren und im Kreislauf überdauern können, bieten sie ein seltenes, wenig invasives Fenster zur Gehirnbiologie. Die Herausforderung ist, dass ein Milliliter Blut hunderte Milliarden Vesikel aus dem ganzen Körper enthält, sodass die vom Gehirn stammenden Vesikel zahlenmäßig stark unterrepräsentiert sind und sich mit Standardmethoden nur schwer isolieren lassen.
Ein magnetischer Chip, der Hirnsignale sortiert
Um dieses Problem anzugehen, entwickelten die Forschenden ein mikrofluidisches Gerät namens mTENPO, das einen kreditkartengroßen Chip mit einem starken Magneten kombiniert. Bevor eine Blutprobe in den Chip gelangt, werden die Vesikel mit magnetischen Nanopartikeln markiert, indem Antikörper verwendet werden, die an Oberflächenproteine binden, die typischerweise auf Vesikeln von Nervenzellen (GluR2) bzw. Astrozyten (GLAST) vorkommen. Während das markierte Gemisch durch Millionen winziger Poren im Chip strömt, zieht das Magnetfeld stark markierte Hirnvesikel zu den Porenwänden und hält sie zurück, während der Rest durchwässert. Auf diese Weise kann das Team zwei Vesikelpopulationen unabhängig voneinander anreichern — solche, die überwiegend von Neuronen stammen, und solche, die überwiegend von Astrozyten stammen — direkt aus einer kleinen Plasmamenge.
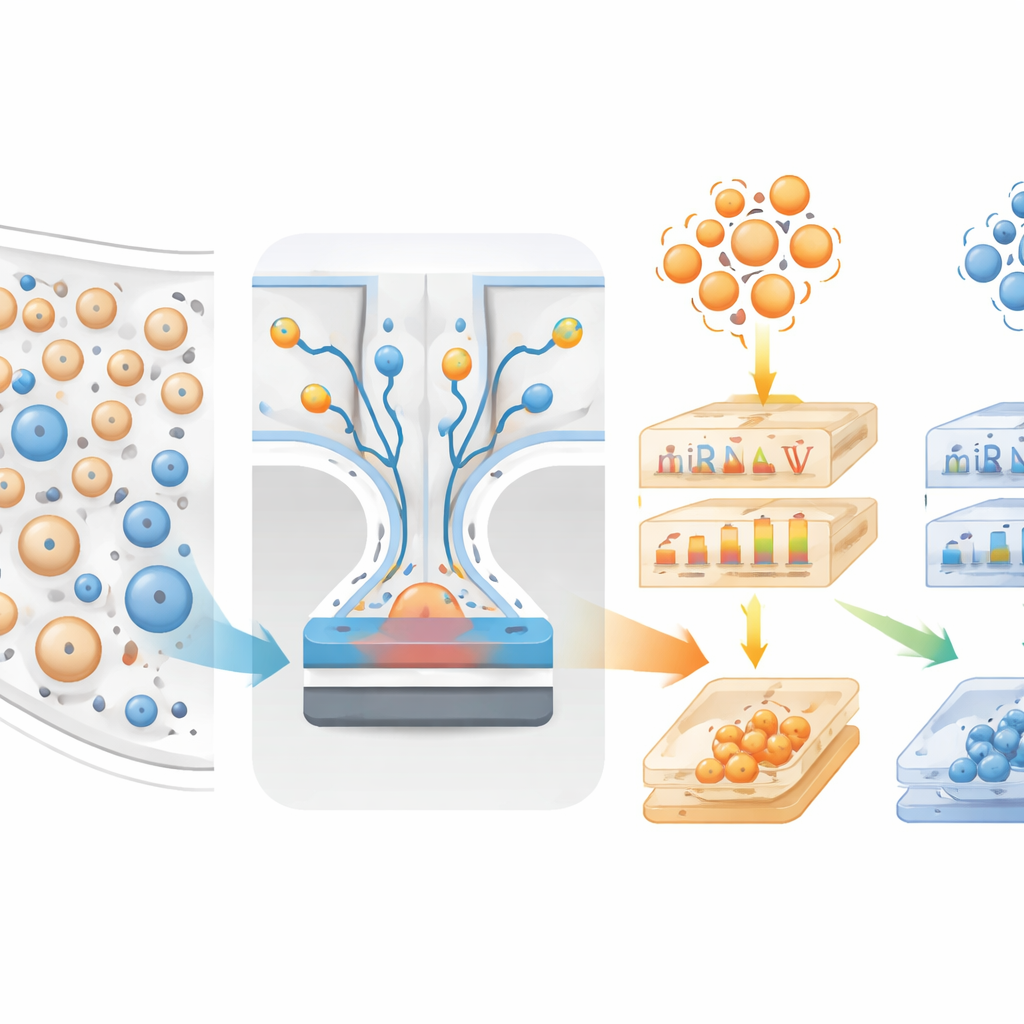
Die molekularen Fingerabdrücke lesen
Von 137 Freiwilligen, deren Gehirndiagnosen nach dem Tod bestätigt wurden, isolierte das Team diese beiden Vesikeltypen und bestimmte zudem klassische Alzheimer-Blutproteine wie verschiedene Formen von Beta‑Amyloid und Tau. Außerdem sequenzierten sie kurze regulatorische RNAs (miRNAs) in den Vesikeln und untersuchten, welche davon sich zwischen Personen mit reiner Lewy‑Körper‑Erkrankung, reiner Alzheimer‑Erkrankung, gemischten Pathologien oder ohne Demenz unterschieden. Mehrere miRNAs in neuronalen und astrozytären Vesikeln sowie mehrere tau‑bezogene Proteine im Plasma zeigten charakteristische Muster zwischen den Lewy‑Körper‑ und Alzheimer‑Gruppen. Als die Forschenden die Gene kartierten, die von diesen miRNAs anvisiert werden, fanden sie starke Verknüpfungen zu Signalwegen, die an Zellüberleben, Entzündung und Proteinverarbeitung beteiligt sind — Prozesse, die bereits mit Neurodegeneration in Verbindung gebracht werden.
Aufbau eines leistungsfähigen kombinierten Bluttests
Da kein einzelner Marker die Krankheiten eindeutig trennte, verwendete das Team Machine‑Learning‑Verfahren, um ein kompaktes Panel der aussagekräftigsten Signale aus allen drei Bereichen zusammenzustellen: neuronale Vesikel, astrozytäre Vesikel und Blutproteine. Das resultierende 15‑Merkmal‑Panel umfasste 14 spezifische Vesikel‑miRNAs sowie zwei phosphorylierte Tau‑Proteine. Mit wiederholter Kreuzvalidierung getestet, um Überanpassung zu reduzieren, unterschied dieses Multi‑Marker‑Panel Lewy‑Körper‑Erkrankung von Alzheimer mit etwa 95 % Genauigkeit und einer Fläche unter der Kurve von 0,96 — deutlich besser als jede einzelne Messgröße für sich. Personen, deren Gehirne Mischformen aufwiesen, zeigten tendenziell Zwischenwerte bei den Markern, was darauf hindeutet, dass solche Panels eines Tages möglicherweise helfen können, gemischte Erkrankungen zu erkennen, anstatt eine Entweder‑Oder‑Klassifikation zu erzwingen.
Vom Machbarkeitsnachweis zur künftigen klinischen Anwendung
Die Studie ist ein früher, aber wichtiger Beleg dafür, dass von Gehirnzellen stammende Vesikel im Blut genügend detaillierte Informationen tragen können, um wichtige Demenztypen zu unterscheiden. Die Arbeit muss noch in größeren, diverseren Gruppen und bei Patienten, die über die Zeit verfolgt werden, bestätigt werden, und die Autoren betonen die derzeitigen Grenzen bei der genauen Bestimmung der Zellherkunft jedes einzelnen Vesikels. Nichtsdestotrotz bietet die Kombination aus einem skalierbaren magnetischen Chip und einem sorgfältig ausgewählten Multimarker‑Panel einen Fahrplan für zukünftige Bluttests, die Behandlungsentscheidungen leiten, klinische Studien verbessern und Familien wesentlich klarere Antworten zur spezifischen Erkrankung hinter der Demenz eines Angehörigen geben könnten.
Zitation: Yang, S.J., Lin, A.A., Shen, H. et al. Microfluidic nanomagnetically isolated neuron- and astrocyte-derived extracellular vesicles to differentiate Lewy body and Alzheimer’s disease. npj Biosensing 3, 19 (2026). https://doi.org/10.1038/s44328-026-00086-x
Schlüsselwörter: extrazelluläre Vesikel, Lewy-Körper-Erkrankung, Alzheimer-Erkrankung, blutbasierte Biomarker, mikrofluidische Diagnostik