Clear Sky Science · de
Surface Transmon Resonance (STR): ein tragbarer Nanospalt‑Biosensor für Echtzeit‑, markierungsfreie Molekülbindungs‑Kinetik
Warum ein winziger elektronischer Sensor für Ihre Gesundheit wichtig ist
Die moderne Medizin stützt sich auf Tests, die Proteine und andere Moleküle im Blut nachweisen, um Krankheiten zu diagnostizieren, Therapien zu steuern und den Gesundheitszustand zu überwachen. Viele der derzeit genauesten Tests verwenden sperrige, teure optische Geräte, die in zentralisierten Laboren stehen. Dieser Artikel stellt eine neue Art von handflächengroßem elektronischem Sensor vor, der dieselben molekularen Bindungsereignisse in Echtzeit ablesen kann, ohne fluoreszierende Marker oder große optische Aufbauten. Können solche Sensoren günstig und mobil hergestellt werden, könnten sie anspruchsvolle Diagnostik aus spezialisierten Laboren in Kliniken, Krankenwagen und sogar Heimanwendungen verlagern.
Eine neue Art, Molekülen „zuzuhören”
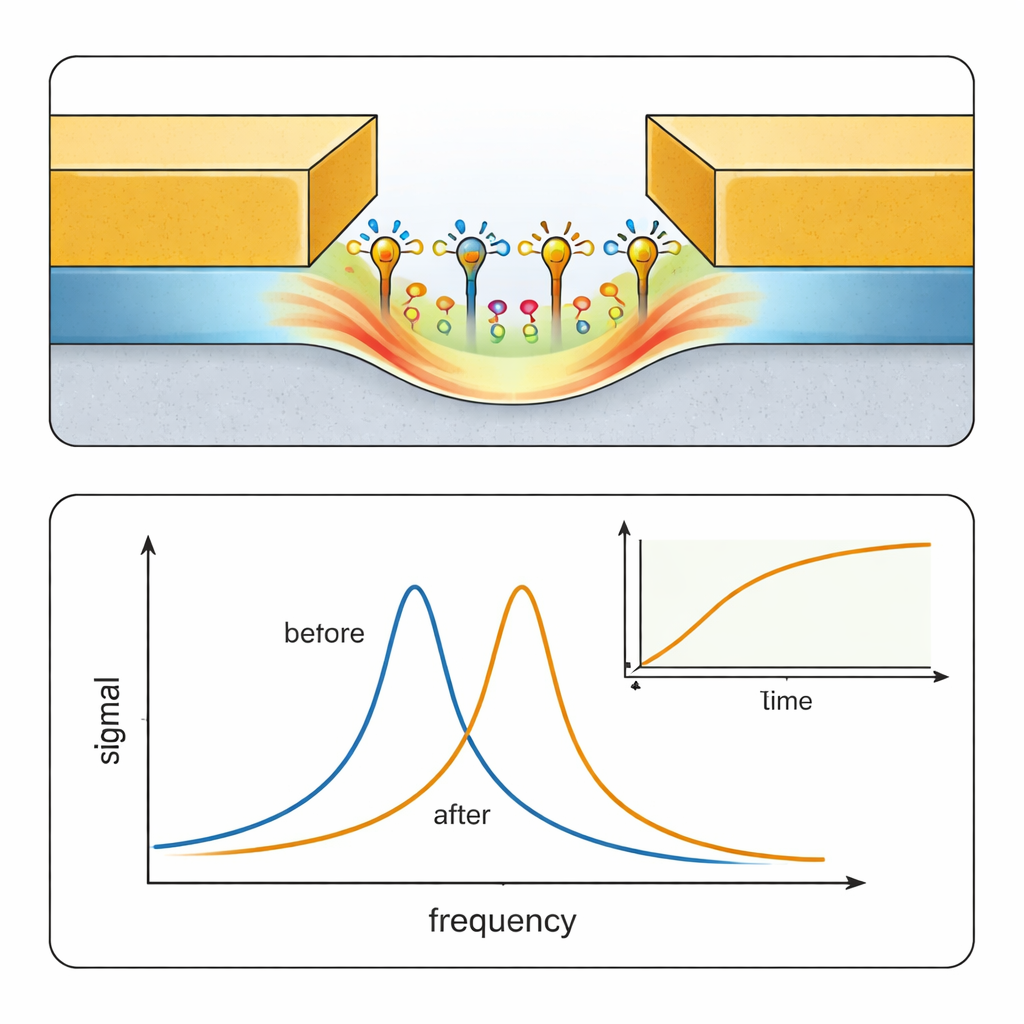
Die Forschenden präsentieren eine Technologie namens Surface Transmon Resonance (STR), einen elektronischen Biosensor, der Ideen aus der Hardware für Quantencomputer aufgreift. Anstelle von Licht nutzt STR hochfrequente Radiowellen, die durch einen winzigen Schaltkreis mit einem nanoskaligen Spalt zwischen zwei Metalllinien geführt werden. Wenn Moleküle an den Oberflächen in diesem Spalt haften, verändern sie subtil die Resonanzeigenschaften des Schaltkreises – ähnlich wie das Hinzufügen von Masse an einer Gitarrensaite deren Tonhöhe verändert. Ein kostengünstiges, tragbares Messgerät – ein nano‑Vector‑Network‑Analyzer – misst diese Verschiebungen in Resonanzphase und ‑frequenz und erzeugt Kurven, die denen der Surface Plasmon Resonance (SPR), dem optischen „Goldstandard“ zur Untersuchung von Biomolekülbindungen, sehr ähnlich sind.

Ein grundlegendes Hindernis der elektronischen Sensorik überwinden
Elektronische Biosensoren haben in salzhaltigen, wässrigen Lösungen wie Blut häufig Probleme, weil gelöste Ionen eine Abschirmungsschicht bilden, die molekulare Ladungen vor der Messelektrode versteckt. Dieser Effekt, bekannt als Debye‑Abschirmung, hat viele transistorbasierte Biosensoren eingeschränkt. STR begegnet diesem Problem durch Betrieb bei Hunderten von Megahertz, einem Bereich, in dem die Ionen mit dem schnell oszillierenden elektrischen Feld nicht Schritt halten können. Dadurch schwächt die Abschirmung ab und das Feld kann eine dünne Molekülschicht an der Oberfläche direkter abtasten. Das Design des Sensors konzentriert das elektrische Feld in einen nanometergroßen Spalt, dessen Größe mit typischen Proteinen vergleichbar ist, sodass selbst eine dünne molekulare Schicht einen erheblichen Anteil des Messvolumens einnimmt und eine messbare Resonanzverschiebung erzeugt.
Proteine bei der Bindung in Echtzeit beobachten
Um zu zeigen, dass STR für ernsthafte biochemische Messungen geeignet ist, untersuchte das Team ein klassisches Testpaar: bovines Serumalbumin (BSA), ein gut bekanntes Protein, und Antikörper, die es erkennen. Zunächst leiteten sie eine Pufferlösung durch einen mikrofluidischen Kanal über den Sensor, um einen Basiswert zu erhalten, injizierten dann BSA, um die Goldoberfläche im Spalt zu beschichten, und brachten schließlich Anti‑BSA‑Antikörper in unterschiedlichen Konzentrationen ein. Der Sensor verfolgte, wie sich seine Resonanzfrequenz im Laufe der Zeit verschob, während Antikörper anhafteten und später beim Zurückspülen mit sauberem Puffer wieder ablösten. Da der Nanospalt so klein ist, haben Bindungsereignisse einen großen Effekt im Vergleich zu einer Kontrollvorrichtung mit einem 10‑Mikrometer‑breiten Spalt, was bestätigt, dass STR hauptsächlich auf oberflächengebundene Moleküle und nicht auf Änderungen der Bulk‑Flüssigkeit reagiert. Durch Anpassung der Bindungs‑ und Lösungskurven extrahierten die Autorinnen und Autoren Assoziations‑ und Dissociationsraten sowie eine Gesamtbindungsaffinität, die eng mit Werten übereinstimmte, die unabhängig mit einem SPR‑Instrument gemessen wurden.
Leistung, die mit optischen Laborgeräten konkurriert
Über die reine Detektion hinaus quantifizierten die Autoren die Empfindlichkeit von STR. Sie zeigten, dass winzige Verschiebungen der Resonanzfrequenz sehr kleinen Änderungen der elektrischen Eigenschaften der Lösung nahe der Oberfläche entsprechen, und bestimmten eine Proteindetektionsgrenze von etwa 7 Nanomolar für den getesteten Antikörper. Diese Leistung ist vergleichbar mit mehreren fortgeschrittenen nanoplasmonischen SPR‑Sensoren aus der Fachliteratur. Wichtig ist, dass dies mit einem Prototyp erreicht wurde, der auf Portabilität und geringe Kosten ausgelegt war, nicht auf maximale Empfindlichkeit. Die Hauptgeräuschquelle war das tragbare Analysegerät selbst; die Autorinnen und Autoren skizzieren jedoch klare Verbesserungswege, wie Erhöhung der Signalleistung, Steigerung der Schärfe (Q‑Faktor) der Resonanz, weitere Verengung des Spalts sowie Verfeinerung der Oberflächenchemie und der Elektronikintegration.
Vom Labortisch zur taschengroßen Diagnostik
Um STR in großem Maßstab praktikabel zu machen, entwickelte das Team zudem einen Wafer‑Level‑Fertigungsansatz, der Arrays von Nanospalt‑Sensoren mit Techniken erzeugen kann, die zur Mainstream‑Mikroelektronik kompatibel sind. Sie stellen sich künftige Versionen vor, bei denen die Sensorelemente und Hochfrequenzschaltungen auf demselben Chip integriert sind und so das Herz tragbarer oder sogar tragbarer Diagnostikgeräte bilden könnten. Weil STR die Art von Echtzeit‑Bindungskurven und quantitativen kinetischen Daten liefert, die bislang großen optischen Instrumenten vorbehalten waren, könnte es molekulare Analysen in Laborqualität an viel mehr Einsatzorte bringen. Für Nicht‑Spezialisten lautet die Quintessenz: Diese Arbeit bringt uns näher an tragbare Geräte, die verfolgen können, wie spezifische Biomoleküle in Echtzeit binden und interagieren — und öffnet damit die Tür zu schnelleren, zugänglicheren und persönlicheren medizinischen Tests.
Zitation: Chantigian, B.K., Oh, SH. Surface Transmon Resonance (STR): a handheld nanogap biosensor for real-time, label-free molecular binding kinetics. npj Biosensing 3, 15 (2026). https://doi.org/10.1038/s44328-026-00080-3
Schlüsselwörter: Biosensor, molekulare Diagnostik, Nanotechnologie, Hochfrequenz‑Sensing, markierungsfreie Detektion