Clear Sky Science · de
Plasmonverstärkter Bioassay zur amplifikationsfreien Erkennung und Quantifizierung von SARS-CoV-2-RNA
Warum schnellere, einfachere Virustests wichtig sind
Die COVID-19-Pandemie machte deutlich, wie stark wir auf laborbasierte Tests angewiesen sind, die langsam, teuer und schwer zu skalieren sind, wenn Millionen von Menschen schnell ein Ergebnis benötigen. Die hier beschriebene Arbeit stellt eine neue Art von Labortest vor, der winzige Mengen des Coronavirus-Genmaterials ohne den üblichen Amplifikationsschritt der PCR nachweisen und zählen kann. Dieser Ansatz zielt darauf ab, die Genauigkeit auf Krankenhausniveau näher an einfache, kostengünstige Tests zu bringen, die bei künftigen Ausbrüchen breiter eingesetzt werden könnten.
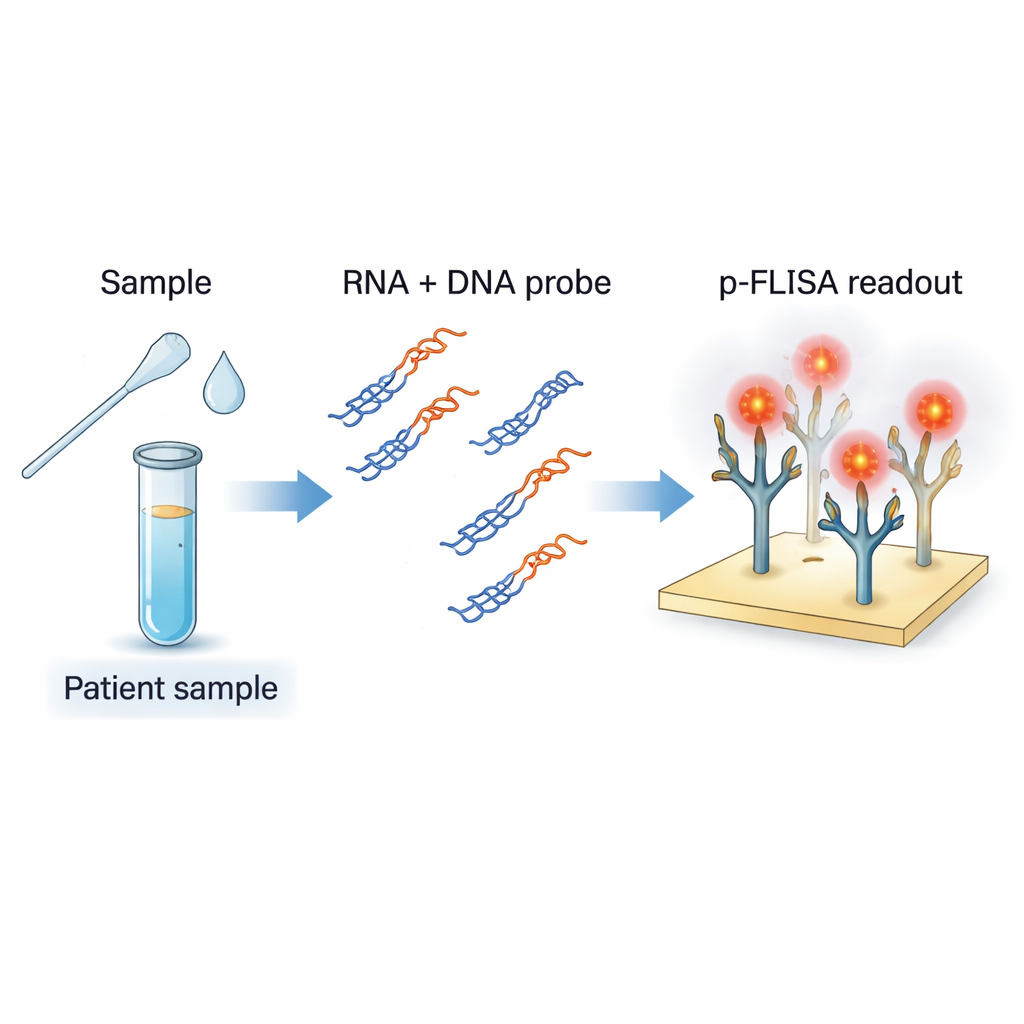
Eine neue Möglichkeit, virale genetische Spuren zu sehen
Die Standarddiagnose von COVID-19 verwendet RT-PCR, die viele Kopien von Fragmenten der viralen RNA herstellt, damit sie nachgewiesen werden können. Zwar sehr sensitiv, erfordert die PCR komplexe Geräte, geschultes Personal und Zeit und liefert meist eine „Ja-oder-Nein“-Antwort statt einer präzisen Viruslast. Die Autoren entwickelten einen Assay, der eher wie eine stark verbesserte Version eines ELISA-Bluttests funktioniert: ein einfaches Plattenformat, aber so abgestimmt, dass es virale RNA direkt erkennt und deren Menge quantifiziert. Ihre Methode zielt auf SARS-CoV-2-RNA in Proben wie Nasenabstrichen und Speichel ab, ist jedoch so konzipiert, dass sie leicht an andere RNA-Viren angepasst werden kann.
RNA in ein fängbares Ziel verwandeln
Das Team verwendet kurze DNA-Stücke, die so entworfen sind, dass sie zu spezifischen Regionen des SARS-CoV-2-Genoms passen. Werden sie mit aus einer Patientenprobe extrahierter RNA gemischt und schonend erhitzt und abgekühlt, paaren sich diese DNA-Sonden mit passenden viralen RNA-Strängen und bilden DNA–RNA-Hybride, ähnlich einem kleinen Reißverschluss mit einem RNA- und einem DNA-Strang. Ein spezieller Antikörper namens S9.6 fungiert als Fänger: Er erkennt und bindet stark an diese Hybride, nicht jedoch an gewöhnliche einzel- oder doppelsträngige DNA oder an nicht verwandte RNA. Indem der Boden einer Platte mit S9.6 beschichtet wird, greift der Assay selektiv nur jene Hybride, die die interessierenden viralen Sequenzen enthalten, und filtert den Rest des genetischen Hintergrunds der Probe heraus.
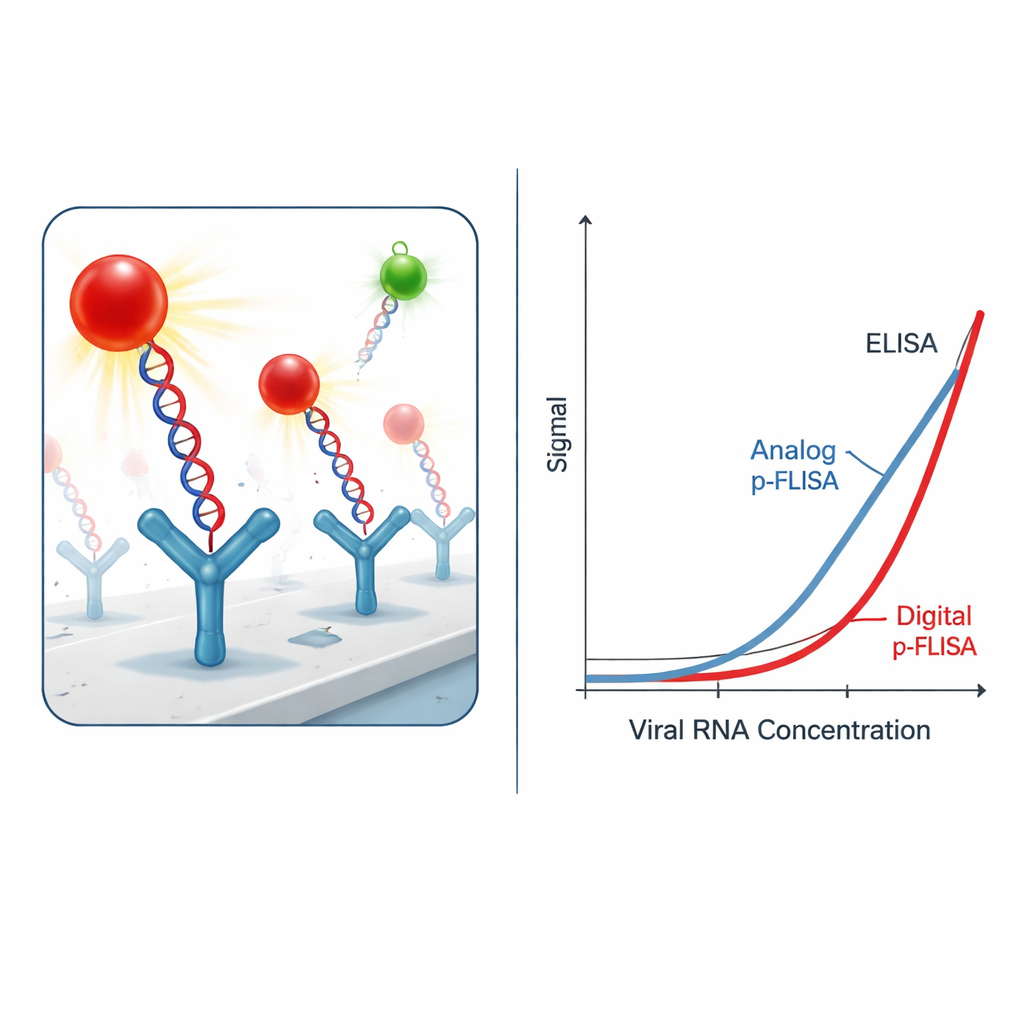
Das Signal ultrastark machen
Allein das Fangen der viralen Hybride reicht nicht aus; die Herausforderung besteht darin, sie über dem Hintergrundrauschen sichtbar zu machen. Statt konventioneller Fluorophore verwenden die Forschenden „plasmonische-Flor“-Nanolabels — konstruierte Nanopartikel, die wie winzige Lichtantennen wirken. Jedes Label kombiniert einen Metallnanostab mit mehreren fluoreszierenden Molekülen und einer Beschichtung, die das Andocken an Biotin-Tags auf der DNA oder dem Antikörper ermöglicht. Diese plasmonischen Label emittieren unter denselben Bedingungen mehr als tausendmal heller als Standardfarbstoffe. In der Praxis bedeutet das, dass weit weniger virale Hybride nötig sind, um ein nachweisbares Leuchten zu erzeugen, was die Sensitivität des Tests deutlich erhöht und die minimale messbare Virus-RNA-Konzentration senkt.
Vom analogen Leuchten zur digitalen Zählung
In seiner einfachsten „analogen“ Form misst der Assay die Gesamthelligkeit aus jedem Well der Platte, ähnlich wie ein klassischer Fluoreszenztest. Selbst in diesem Modus verbessert das plasmonverstärkte System die Nachweisgrenze und das niedrigste zuverlässig quantifizierbare Niveau der SARS-CoV-2-RNA um ein bis drei Größenordnungen gegenüber einem traditionellen ELISA mit Enzymen oder Standardfluorophoren. Die Autoren gehen dann einen Schritt weiter und wechseln zu einem „digitalen“ Format: Statt das Licht über das ganze Well zu mitteln, nehmen sie die Oberfläche mit einem Fluoreszenzmikroskop auf und zählen einzelne helle Nanolabels mit maßgeschneiderter Bildanalyse-Software. Dieser Einzelpartikelzählansatz erzielt nochmals einen zehn- bis dreißigfachen Empfindlichkeitsgewinn, was insgesamt zu etwa 2.300-fach besseren Nachweisgrenzen und 460-fach besseren Quantifizierungsgrenzen gegenüber ELISA führt.
Den Test an realen Proben erproben
Um zu prüfen, ob die Methode außerhalb kontrollierter Laboransätze funktioniert, testeten die Forschenden RNA, die aus Nasenabstrichen und Speichel von COVID-19-Patienten extrahiert wurde, darunter Infektionen mit verschiedenen Varianten wie Alpha/Beta und Delta sowie Proben von Personen mit anderen Atemwegsviren. Ihr plasmonverstärkter Assay detektierte SARS-CoV-2-RNA in allen PCR-positiven Proben, zeigte kein Signal über dem Hintergrund in PCR-negativen Proben oder solchen mit anderen Viren, was auf eine ausgezeichnete klinische Sensitivität und Spezifität hinweist, vergleichbar mit RT-PCR. Zudem zeigten die gemessenen RNA-Konzentrationen eine umgekehrte Beziehung zu den PCR-Cycle-Threshold-Werten: Proben, die weniger PCR-Zyklen benötigten (was auf eine höhere Viruslast hinweist), wiesen höhere RNA-Spiegel im neuen Assay auf — konsistent mit biologischen Erwartungen und ein Hinweis darauf, dass er aussagekräftige quantitative Informationen zur Viruslast liefern kann.
Was das für künftige Ausbrüche bedeuten könnte
Für Nicht-Spezialisten ist die Kernbotschaft, dass dieser Assay eine Möglichkeit bietet, die Menge des vorhandenen Virus abzulesen, ohne den zusätzlichen Vervielfältigungsschritt, der die PCR langsam und geräteintensiv macht. Durch die Kombination eines selektiven Antikörpers für RNA–DNA-Hybride mit ultrastarken nanoskaligen Lichtquellen und digitaler Zählung nähert sich die Methode der Leistung der PCR an, behält aber einen einfachen, plattenbasierten Arbeitsablauf bei. Mit weiterer Validierung und technischer Entwicklung könnten solche plasmonverstärkten Assays an viele RNA-Ziele angepasst und möglicherweise in schnelle Point-of-Care-Formate überführt werden, wodurch Kliniker nicht nur Infektionen diagnostizieren, sondern auch anhand einer absoluten Messung der Virus-RNA Krankheitsstadium und Ansteckungsfähigkeit abschätzen könnten.
Zitation: Liu, L., Seth, A., Liu, Y. et al. Plasmon-enhanced bioassay for amplification-free detection and quantification of SARS-CoV-2 RNA. npj Biosensing 3, 13 (2026). https://doi.org/10.1038/s44328-026-00078-x
Schlüsselwörter: SARS-CoV-2-RNA-Erkennung, plasmonische Nanolabels, digitaler Immunoassay, amplifikationsfreie Diagnostik, Quantifizierung der Viruslast