Clear Sky Science · de
Ein mikro‑Organ-basiertes mikrofluidisches Biosensor-System zur kontinuierlichen Überwachung des Glukosespiegels in vivo
Warum das für Menschen mit Diabetes wichtig ist
Für Menschen mit Typ‑1‑Diabetes benötigen heutige „künstliche Bauchspeicheldrüsen“-Systeme weiterhin ständige Aufmerksamkeit — Mahlzeiten müssen angekündigt, Alarme bearbeitet und nächtliche Hypoglykämien befürchtet werden. Diese Studie untersucht eine radikal andere Art von Glukosesensor, der sich nicht auf ein einzelnes Enzym oder eine Rechenvorschrift stützt, sondern ein winziges, lebendes Stück der körpereigenen Blutzucker‑Regelmaschine nutzt: Cluster pankreatischer Zellen, sogenannte Inseln. Indem diese Mini‑Organe das tun, wozu die Evolution sie optimiert hat, wollen die Forschenden schlauere, sicherere Glukosemonitore entwickeln, die eines Tages autonomer im Hintergrund arbeiten könnten.
Ein winziges Organ als lebender Sensor
Die meisten aktuellen Biosensoren detektieren Chemikalien mit gereinigten Molekülen oder Zelllinien. Sie reagieren auf eine spezifische Substanz und übergeben dann das Rohsignal an Software, die es zu interpretieren versucht. Die Autor:innen argumentieren, dass dieser Ansatz einen leistungsfähigen eingebauten „Computer“ außer Acht lässt: Mikro‑Organe wie Pankreasinseln, die naturgemäß viele Signale gleichzeitig wahrnehmen und in eine koordinierte Antwort übersetzen. Jede Insel enthält mehrere hormonproduzierende Zelltypen, die ständig miteinander kommunizieren. Zusammen halten sie den Blutzucker in einem engen, sicheren Bereich und reagieren nicht nur auf Glukose, sondern auch auf Aminosäuren, Darm‑ und Stresshormone sowie auf die kürzliche Verlaufsgeschichte von Hochs und Tiefs. Diese eingebaute Komplexität, so die Autoren, ließe sich nutzen, um reichhaltigere und verlässlichere Informationen zu liefern als ein einfacher Glukose‑Oxidase‑Sensor.
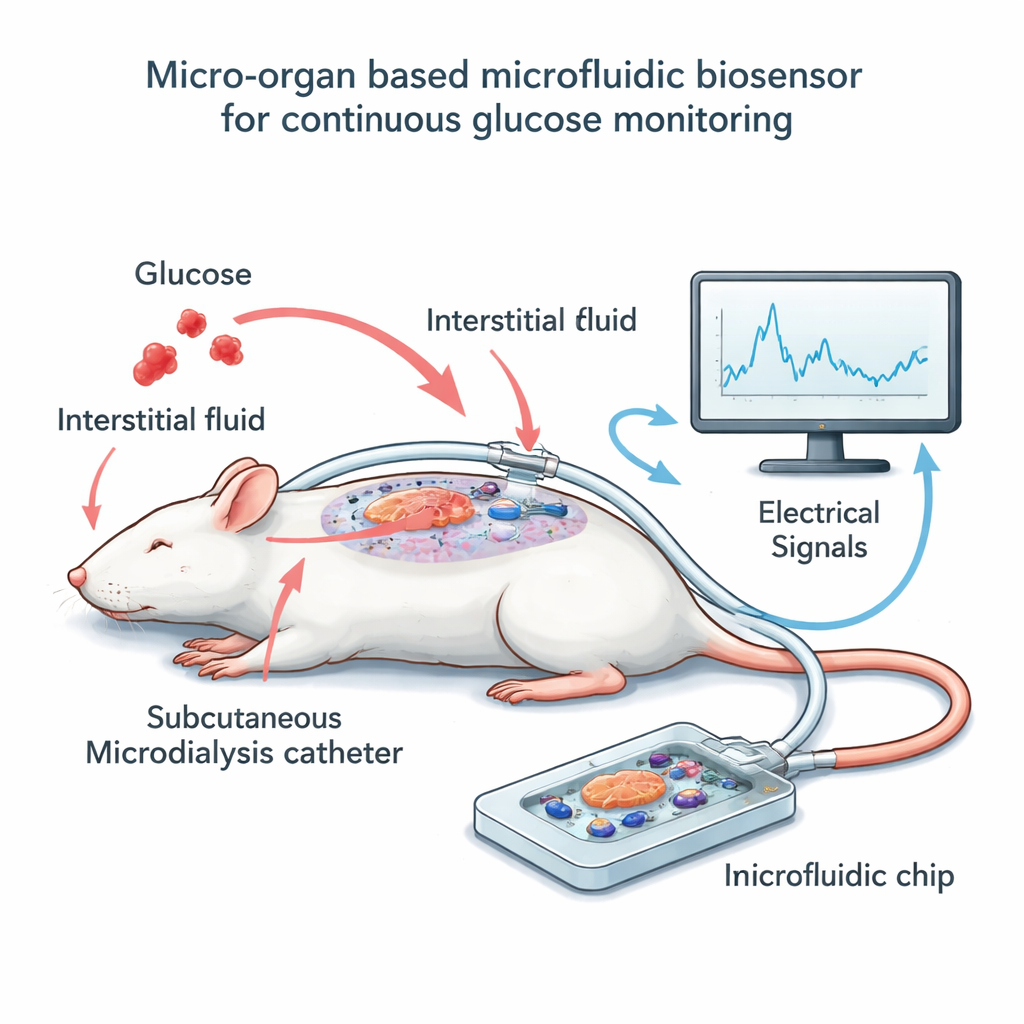
Aufbau des Chip‑und‑Katheter‑Systems
Um die Idee zu testen, baute das Team ein kleines Gerät außerhalb des Körpers, das einige Dutzend Maus‑Inseln auf einem Raster mikroskopischer Elektroden beherbergt. Statt diese Zellen direkt dem Blut auszusetzen, verwendeten sie eine Technik namens Mikro‑Dialyse: Eine dünne flexible Katheter liegt knapp unter der Haut anesthesierter Ratten und sammelt langsam die umgebende Gewebsflüssigkeit, die dem Blutzucker eng folgt, jedoch mit einer kurzen Verzögerung. Ein niedriger, konstanter Fluss transportiert diese Flüssigkeit durch einen engen Kanal über die Inseln auf dem Chip. Wenn die Glukosekonzentration im Dialysat steigt und fällt, ändern die Inseln ihre elektrische Aktivität, die die Elektroden als langsame, wellenartige Signale erfassen. Parallel maßen die Forschenden periodisch die Glukose im Blut der Ratten und im Dialysat, so dass sich die elektrische Messung mit den tatsächlichen Zuckerwerten über die Zeit abgleichen ließ.
Wie der lebende Sensor auf veränderlichen Zucker reagierte
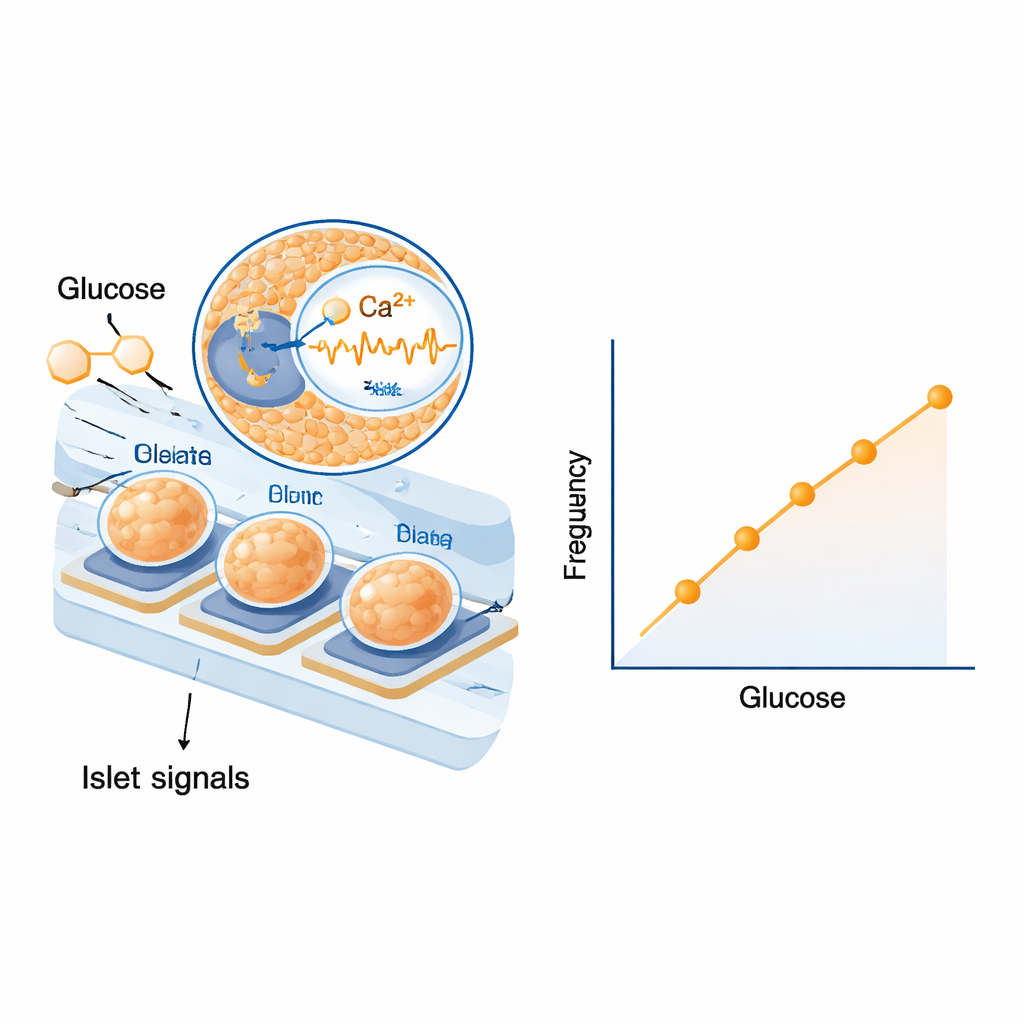
Zunächst prüften die Wissenschaftler:innen, ob Inseln auf den Elektroden auf reale Blutbestandteile und nicht nur auf einfache Laborlösungen reagieren können. Sie setzten sie menschlichem und Rattenserum mit unterschiedlichen Glukosewerten aus und beobachteten deutliche, gestufte Änderungen sowohl in der Häufigkeit als auch in der Größe ihrer elektrischen Wellen. Die Antworten waren stark genug, um kleine Schritte in der Zuckerkonzentration im für Diabetes relevanten Bereich zu unterscheiden. Anschließend gingen sie auf Tierversuche über, verabreichten eine Glukoseinjektion, um den Blutzucker zu erhöhen, und später Insulin, um ihn zu senken. Nach Berücksichtigung der Zeitspanne, die Glukose benötigt, um vom Blut in die Gewebsflüssigkeit und durch die Schläuche zu gelangen, stellten sie fest, dass die Frequenz der langsamen elektrischen Signale der Inseln nahezu im Gleichklang mit dem Blutzucker anstieg und fiel. Statistische Analysen über mehrere Tiere zeigten eine bemerkenswert enge, wiederholbare Beziehung zwischen Signalfrequenz und Glukosespiegel, während die Signalamplitude zwar informativ, aber etwas variabler war.
Biologisch eingebaute Sicherheitsmerkmale
Ein wichtiger Vorteil der Verwendung ganzer Inseln statt eines einzelnen Moleküls besteht darin, dass ihr Verhalten bereits Sicherheitsmechanismen enthält, die durch die Evolution geformt wurden. Frühere Arbeiten und Hinweise aus dieser Studie zeigen, dass Inseln stärker reagieren, wenn die Glukose fällt, als wenn sie steigt — eine Form von „Hysterese“, die vor gefährlicher Hypoglykämie schützt. Die elektrischen Muster werden außerdem von benachbarten Zelltypen geprägt, die die Insulinfreisetzung je nach Bedarf des Körpers verstärken oder dämpfen. Da der Chip diese integrierten Signale einfach „abhört“, ohne Farbstoffe oder genetische Modifikationen hinzuzufügen, kann er Tage lang aufzeichnen, ohne die Zellen zu schädigen. Die Autor:innen nennen technische Herausforderungen, etwa das Vermeiden von Luftblasen, die Sicherstellung einer langfristigen Mikro‑Dialyse‑Performance und die Frage, welche Art von menschlichen oder aus Stammzellen abgeleiteten Inseln schließlich eingesetzt werden sollen. Dennoch deuten Computersimulationen mit einem etablierten Diabetesmodell darauf hin, dass ein solcher Insel‑basierter Sensor heutige Glukosemonitore unter schwierigen Bedingungen einholen oder sogar übertreffen könnte.
Was das für die künftige Diabetesversorgung bedeuten könnte
Diese Arbeit zeigt, dass ein paar pankreatische Mikro‑Organe, auf einem kleinen Chip am Leben erhalten und über einen dünnen Katheter mit dem Körper verbunden, den Blutzucker in lebenden Tieren kontinuierlich anhand ihres natürlichen elektrischen „Gesprächs“ verfolgen können. Für Nicht‑Spezialist:innen ist die Kernbotschaft: Anstatt einen einfachen chemischen Sensor zu bitten, Glukose zu messen und dann einen Computer zu zwingen, daraus zu schließen, was das für den Körper bedeutet, hört dieser Ansatz direkt auf dieselbe Art lebendes Gewebe, das normalerweise entscheidet, wie viel Insulin freigesetzt werden soll. Wenn er verfeinert und für den Menschen praktikabel gemacht wird, könnten solche lebenden Biosensoren zum Kern wirklich autonomer Systeme für künstliche Bauchspeicheldrüsen werden — Geräte, die leise die Bedürfnisse des Körpers antizipieren und die tägliche Belastung der Diabetes‑Versorgung verringern.
Zitation: Puginier, E., Pirog, A., de Gannes, F.P. et al. A micro-organ based microfluidic biosensor for continuous monitoring of glucose levels in vivo. npj Biosensing 3, 12 (2026). https://doi.org/10.1038/s44328-025-00077-4
Schlüsselwörter: kontinuierliche Glukoseüberwachung, künstliche Bauchspeicheldrüse, Pankreasinseln, mikrofluidischer Biosensor, Typ‑1‑Diabetes