Clear Sky Science · de
Ein narrativer Überblick über die Auswirkungen von Apolipoproteinen auf atherosklerotische Koronarplaques
Warum die Fette in Ihrem Blut weiterhin zählen
Herzinfarkte und Schlaganfälle beginnen oft mit stillen Veränderungen in den Blutgefäßen, die das Herz versorgen. Dieser Artikel blickt über das bekannte „gute“ und „schlechte“ Cholesterin hinaus auf die Proteinhüllen, die Fette durch den Blutkreislauf transportieren – die Apolipoproteine. Anhand der Betrachtung, wie vier dieser Proteine das Wachstum, die Zusammensetzung und die Therapie von Koronarplaques – den fetthaltigen Ablagerungen, die Herzkranzgefäße verengen – beeinflussen, zeigen die Autorinnen und Autoren, warum manche Menschen ein hohes Risiko für Herzerkrankungen behalten, selbst wenn ihre Cholesterinwerte ideal erscheinen.
Die versteckten Akteure auf dem Cholesterin
Die meisten von uns kennen LDL- und HDL-Cholesterin, doch jedes dieser Partikel ist von einem oder mehreren Apolipoproteinen umgeben, die mitentscheiden, wohin das Partikel gelangt und wie gefährlich es ist. Diese Übersichtsarbeit konzentriert sich auf vier wichtige Typen: Apolipoprotein(a), Apolipoprotein A‑I, Apolipoprotein B und Apolipoprotein C‑III. Gemeinsam steuern sie, wie fetthaltige Partikel zusammengestellt werden, wie lange sie im Kreislauf verbleiben und wie leicht sie in die Gefäßwand eindringen und Schaden anrichten. Moderne Bildgebungsverfahren – Ultraschall innerhalb der Arterie, hochauflösende lichtbasierte Scans und CT-Angiographie – erlauben es Ärzten inzwischen, nicht nur zu sehen, wie eng eine Arterie ist, sondern ob Plaques weich und rupturgefährdet oder dicht und verkalkt sind. 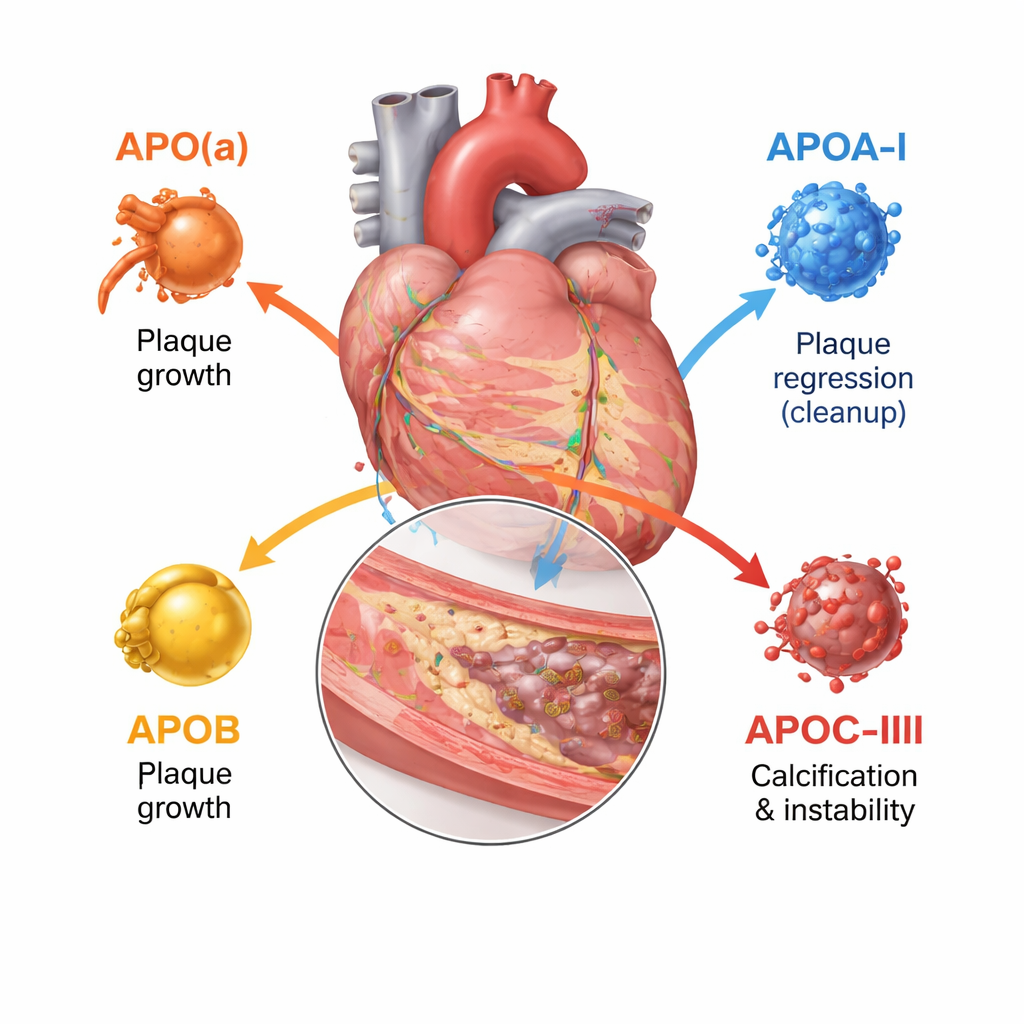
Wie vier Proteine gefährliche Plaques formen
Apolipoprotein B sitzt auf jedem LDL-ähnlichen Partikel und zählt de facto, wie viele atherogene – die Arterien verstopfende – Partikel im Blut vorhanden sind. Je mehr ApoB-tragende Partikel eine Person hat und je länger sie zirkulieren, desto größer ist die Gesamtplaque-Belastung in den Koronararterien. Bildgebende Studien innerhalb der Herzarterien zeigen, dass höhere ApoB-Werte mit größeren Plaques, längeren Läsionsstrecken, mehr weichen, nekrotischen Kernen und weniger stabilisierenden Kalkablagerungen einhergehen. Im Gegensatz dazu hilft Apolipoprotein A‑I, das Hauptprotein auf HDL, Cholesterin aus Plaquezellen zu entfernen und zurück zur Leber zu transportieren. Höhere funktionelle ApoA‑I-Aktivität und ein günstiges Verhältnis von HDL-Cholesterin zu ApoA‑I sind mit langsamerem Plaquewachstum und faserigerem, stabilerem Gewebe verbunden, obwohl die bloße Erhöhung des HDL-Cholesterins im Blut nicht in weniger klinischen Ereignissen mündete.
Ein besonderes Risikoprotein und ein Förderer der Verhärtung
Apolipoprotein(a) bildet ein Partikel namens Lipoprotein(a), oder Lp(a), wenn es sich an einen LDL-ähnlichen Kern anlagert. Lp(a) wird fast vollständig genetisch bestimmt und ist in der Regel unverändert durch die Ernährung. Bildgebende Studien an Tausenden von Patienten zeigen, dass Menschen mit hohem Lp(a) mehr Gesamtplaque, mehr niedrigdichte, lipidreiche Bereiche und mehr fokale „Hochrisiko“-Plaques haben, die zum Aufbrechen neigen – selbst wenn LDL-Cholesterin bereits aggressiv behandelt wird. Die Übersichtsarbeit kommt zu dem Schluss, dass Lp(a) ein bedeutendes „residuelles Risiko“ darstellt, das durch Standard-Cholesterinsenkungstherapien nicht vollständig abgedeckt wird. Apolipoprotein C‑III, überwiegend auf triglyceridreichen Partikeln zu finden, verlangsamt deren Clearance und fördert Entzündungen. Menschen mit höheren ApoC‑III-Werten haben mehr koronare Kalkablagerungen und komplexere, verkalkte Noduli innerhalb der Plaques – Merkmale, die mit fortgeschrittener Erkrankung und Versteifung der Gefäße verknüpft sind.
Neue Medikamente, die die richtigen Ziele anvisieren
Da diese Proteine das Risiko präziser abbilden als Cholesterin allein, werden sie zunehmend direkt als Arzneimittelziele angegangen. Für Lp(a) können mehrere injizierbare genetische Medikamente – Antisense- und small-interfering-RNA-Wirkstoffe – die Werte in frühen Studien um 80–95 % senken, und eine Tablette, die den Zusammenbau des Partikels blockiert, zeigt ebenfalls große Reduktionen. Für ApoC‑III können kürzlich zugelassene Therapien Triglyceride und ApoC‑III selbst stark senken, und frühe Daten deuten darauf hin, dass sie Pankreatitis reduzieren und die Plaquekalkung verändern könnten. 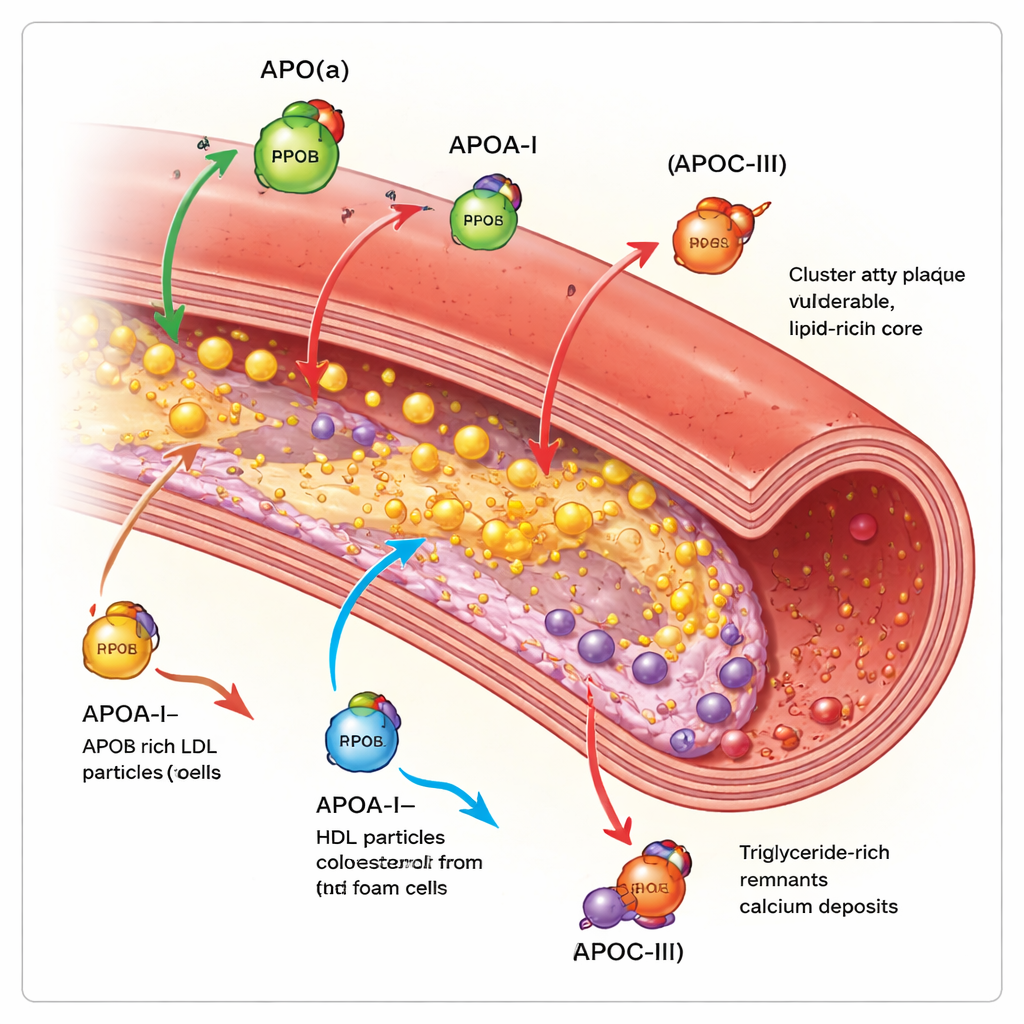
Was das für den Schutz Ihres Herzens bedeutet
Kurz gesagt argumentiert diese Übersichtsarbeit, dass nicht allein die Cholesterinwerte darüber entscheiden, wer einen Herzinfarkt erleidet, sondern die Mischung und das Verhalten der proteinbeschichteten Partikel, die dieses Cholesterin transportieren. ApoB spiegelt wider, wie viele „schädliche“ Partikel die Gefäßwand bombardieren; ApoA‑I steht für das System, das Cholesterin abtransportiert; Lp(a) fügt ein zusätzliches, genetisch festgelegtes Risiko hinzu; und ApoC‑III begünstigt verhärtete, entzündliche Plaques. Neue Wirkstoffe, die gezielt Lp(a) und ApoC‑III absenken, sowie eine präzisere Nutzung von ApoB und ApoA‑I in Routinetests könnten Ärzten erlauben, die Prävention an die individuelle Plaque-Biologie jedes Patienten anzupassen und so versteckte Risiken zu erkennen, die Standard-Lipidprofile übersehen.
Zitation: Fukase, T., Dohi, T. A narrative review of impacts of apolipoproteins on atherosclerotic coronary plaques. npj Cardiovasc Health 3, 4 (2026). https://doi.org/10.1038/s44325-026-00104-x
Schlüsselwörter: lipoprotein(a), apolipoprotein B, apolipoprotein A-I, apolipoprotein C-III, Koronarplaque-Bildgebung