Clear Sky Science · de
Aus dem Fettgewebe stammendes MFG-E8 fördert hepatische Entzündung und Fibrose durch Makrophagenaktivierung in einem Maus‑MASH‑Modell
Warum Bauchfett der Leber schaden kann
Viele Menschen sehen überschüssiges Bauchfett vor allem als kosmetisches Problem, doch es kann die Leber stillschweigend schädigen. Diese Studie untersucht, wie Fett um die Organe im Bauchraum eine schwere Lebererkrankung antreibt: die metabolische Dysfunktion‑assoziierte Steatohepatitis (MASH). Die Forschenden identifizieren ein aus dem Fettgewebe freigesetztes Protein, das zur Leber wandert und Entzündung sowie Vernarbung verstärkt. Das hilft zu erklären, warum Menschen mit großem Anteil an viszeralem Fett ein erhöhtes Risiko für Leberversagen und Leberkrebs haben, selbst wenn der Fettgehalt der Leber ähnlich aussieht wie bei anderen.
Ein versteckter Bote von Fett zur Leber
Ärztinnen und Ärzte beobachten schon lange, dass Menschen mit viel tief sitzendem Bauchfett eher entzündete und vernarbte Lebern entwickeln als Personen mit derselben Menge an Leberfett, aber weniger viszeralem Fett. Dieses Muster deutete darauf hin, dass das Fettgewebe chemische Signale an die Leber sendet, doch die wichtigen Botenstoffe waren bislang unbekannt. In dieser Arbeit verwendeten die Wissenschaftler Mäuse mit fettreicher Ernährung und ein beschleunigtes, diabetesähnliches MASH‑Modell, um nach Proteinen zu suchen, die in viszeralem Fett stark produziert und während der Erkrankung erhöht im Blut nachweisbar sind. Ein Protein stach hervor: MFG‑E8, ein milchfettassoziiertes Protein, das dafür bekannt ist, Immunzellen bei der Erkennung und Beseitigung sterbender Zellen zu unterstützen.
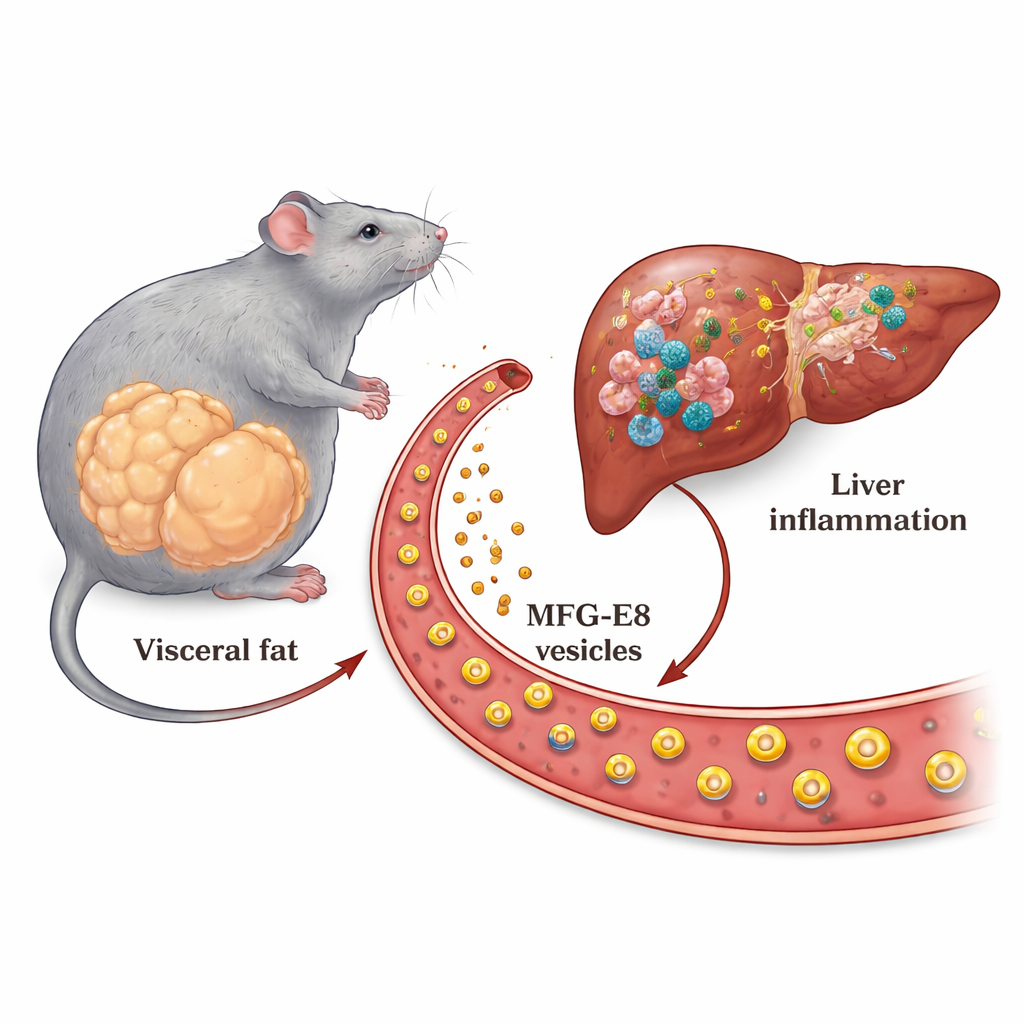
Adipozyten erhöhen MFG‑E8 bei Fettleibigkeit
Das Team fragte zunächst, woher MFG‑E8 in erkrankten Tieren stammt. Sie zeigten, dass Mäuse mit fettreicher Diät und besonders jene im beschleunigten MASH‑Modell deutlich höhere Mfge8‑Genlevels in ihren Bauchfettpolstern aufwiesen, jedoch nicht in der Leber selbst. Mit zunehmender Vergrößerung der Fettzellen wurde dieses Protein verstärkt produziert. Durch die Trennung des Fettgewebes in Fettzellen und Stütz- bzw. Stromazellen sowie mittels Knochenmarktransplantationsversuchen demonstrierten die Forschenden, dass die Hauptquelle des zusätzlichen MFG‑E8 die Fettzellen und nicht die Immunzellen war. Sie bestätigten außerdem, dass mehr MFG‑E8 im Blut zirkulierte, gebunden an winzige Partikel, sogenannte extrazelluläre Vesikel, die als Transportvehikel zu entfernten Organen dienen können.
Das Blockieren des Signals mildert Leberschäden
Um zu prüfen, ob dieses Protein die Lebererkrankung tatsächlich verschlimmert, verwendeten die Wissenschaftler Mäuse, die das Mfge8‑Gen vollständig fehlten. Wenn diese Knockout‑Tiere dem gleichen MASH‑auslösenden Protokoll unterzogen wurden, entwickelten sie ähnliche Mengen an Leberfett, aber deutlich weniger Entzündungen, weniger verletzte und geschwollene Leberzellen sowie weit weniger Narbengewebe. Immunzellmarker und fibrosebezogene Gene in der Leber waren stark reduziert, und die Leberenzyme im Blut der Tiere lagen niedriger, was auf geringere Schädigung hinweist. Unter dem Mikroskop fanden sich deutlich weniger „kranzartige“ Ansammlungen von Immunzellen um abgestorbene Leberzellen, und die insgesamt vernarbte Fläche war kleiner. Diese Mäuse überlebten zudem länger als normale Mäuse im gleichen Modell, was darauf hindeutet, dass das Entfernen von MFG‑E8 vor lebensbedrohlichen Leberkomplikationen schützen kann.
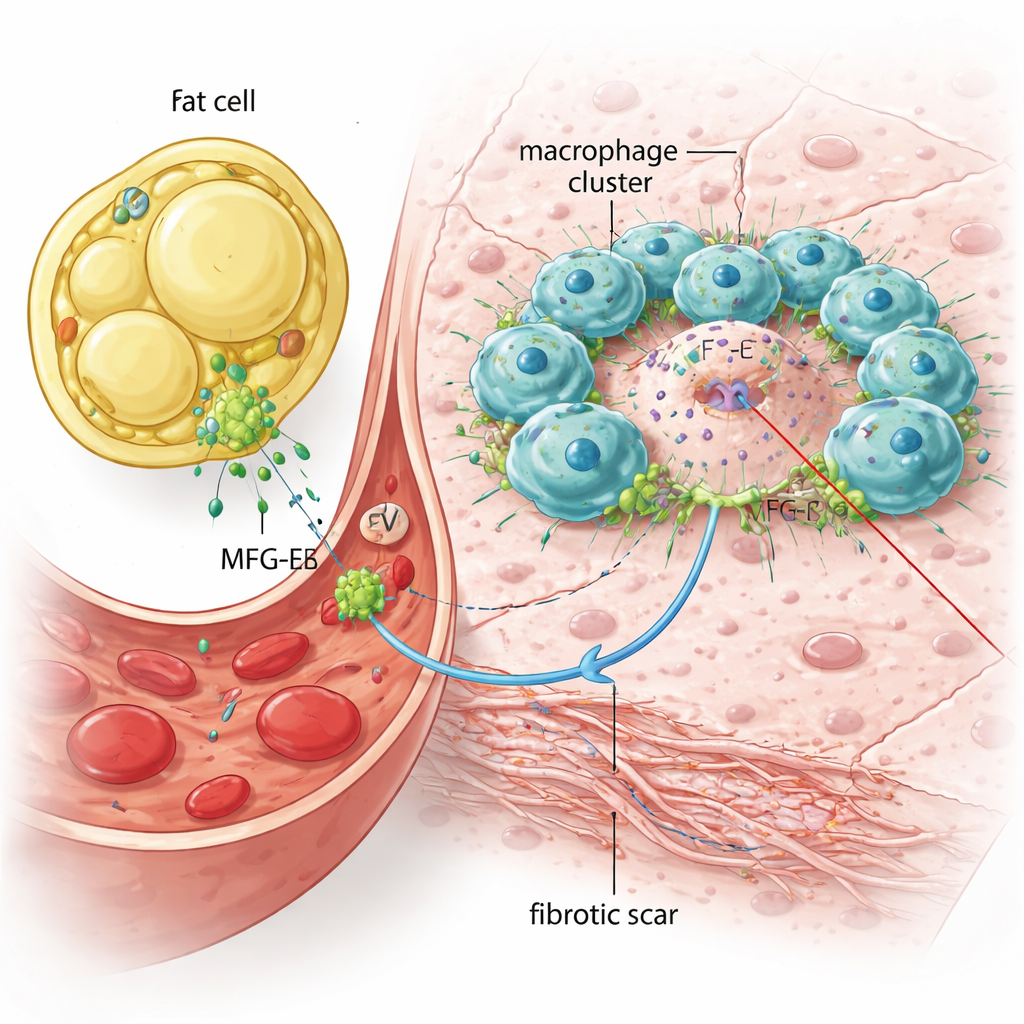
Wiederzuführung des Signals bringt die Entzündung zurück
Die Gruppe fragte anschließend, ob das Wiederzugeben von MFG‑E8 die Krankheitseigenschaften zurückbringt. Sie reinigten Vesikel aus kultivierten Immunzellen, die entweder MFG‑E8 enthielten oder nicht, und injizierten diese in Mfge8‑defiziente Mäuse in der frühen MASH‑Phase. Vesikel mit MFG‑E8 steigerten selektiv entzündliche und fibrotische Gene in der Leber und erhöhten die Zahl der Immunzellansammlungen um sterbende Leberzellen, während Vesikel ohne das Protein dies nicht taten. In einem separaten In‑vitro‑Experiment kultivierten sie Mausmakrophagen zusammen mit sterbenden Leberzellen. Die toten Leberzellen lösten eine Entzündungsreaktion aus, und die Zugabe von gereinigtem MFG‑E8 verstärkte diese Reaktion — jedoch nur, wenn die Immunzellen physischen Kontakt zu den sterbenden Zellen aufnehmen konnten. Wurden die beiden Zelltypen durch eine Membran getrennt, die direkten Kontakt verhinderte, verschwand der Verstärkungseffekt von MFG‑E8 größtenteils, was nahelegt, dass das Protein als physische Brücke wirkt, die die Interaktion zwischen Makrophagen und geschädigten Leberzellen verfestigt.
Was das für Menschen mit Fettleber bedeutet
Ausgehend von diesen Befunden schlagen die Autorinnen und Autoren vor, dass bei Fettleibigkeit übergroße Fettzellen große Mengen MFG‑E8 auf Vesikeln in den Blutkreislauf abgeben. Dieses Protein akkumuliert dann in der Leber, wo es Immunzellen dabei unterstützt, sich um abstorbene Leberzellen zu scharen, und entzündliche sowie fibrotische Signale verstärkt. Mit der Zeit kann dieser Prozess eine relativ stille Fettleber in gefährliche MASH mit Fibrose und einem erhöhten Risiko für Zirrhose und Leberkrebs treiben. Während MFG‑E8 in anderen Kontexten hilfreiche Rollen bei Gewebeauflösung und Reparatur spielen kann, deutet diese Studie darauf hin, dass es im Kontext von Fettleibigkeit Teil einer schädlichen Fett‑Leber‑Kommunikationsschleife wird. Das Verständnis und die spätere Unterbrechung dieser Schleife könnte zu neuen Möglichkeiten führen, die Leber bei Menschen mit überschüssigem viszeralem Fett zu schützen.
Zitation: Kuroda, M., Nomura, K., Wada, A. et al. Adipose tissue–derived MFG-E8 promotes hepatic inflammation and fibrosis through macrophage activation in a mouse MASH model. npj Metab Health Dis 4, 8 (2026). https://doi.org/10.1038/s44324-026-00099-0
Schlüsselwörter: Fettlebererkrankung, viszerales Fett, Leberfibrose, Entzündung, MFG-E8