Clear Sky Science · de
Maximierung der Photonenausbeute in spektroskopischer Einzelmolekül-Lokalisationsmikroskopie mittels symmetrisch dispergierender Doppelkeilprismen
Scharfere Einblicke in die winzige Welt
Viele der wichtigsten Akteure der Biologie — einzelne Moleküle in unseren Zellen — sind mit normalen Mikroskopen zu klein, um gesehen zu werden. In den letzten zehn Jahren haben neue „Superauflösungs“-Methoden das geändert, doch oft müssen Wissenschaftler dabei Bildschärfe gegen Farbinformation oder lange, komplizierte Experimente eintauschen. Dieser Artikel stellt ein raffiniertes optisches Zusatzmodul vor, das es Forschern ermöglicht, viele Molekülarten gleichzeitig in 3D mit besserer Detailerkennbarkeit und weniger Aufwand zu beobachten.
Einzelne Moleküle nacheinander sehen
Superauflösungsverfahren wie STORM und PALM funktionieren, indem nur wenige fluoreszierende Moleküle gleichzeitig blinken, dann jedes Aufblitzen mit hoher Präzision lokalisiert und tausende solcher Frames zu einem detaillierten Bild kombiniert werden. Die spektroskopische Einzelmolekül-Lokalisationsmikroskopie (sSMLM) geht einen Schritt weiter: Sie bestimmt nicht nur, wo sich jedes Molekül befindet, sondern misst auch dessen Farbspektrum. Diese zusätzliche spektrale Information ist sehr mächtig, weil sie Wissenschaftlern erlaubt, mehrere Farbstoffe mit überlappenden Spektren zu verwenden und trotzdem zu unterscheiden. Das Problem ist, dass herkömmliche sSMLM normalerweise kostbare Photonen zwischen einem Positionsbild und einem Spektralbild aufteilen muss, was das Endbild verwischt und lichtschwache Moleküle schwerer erkennbar macht.
Jedes Photon doppelt nutzen
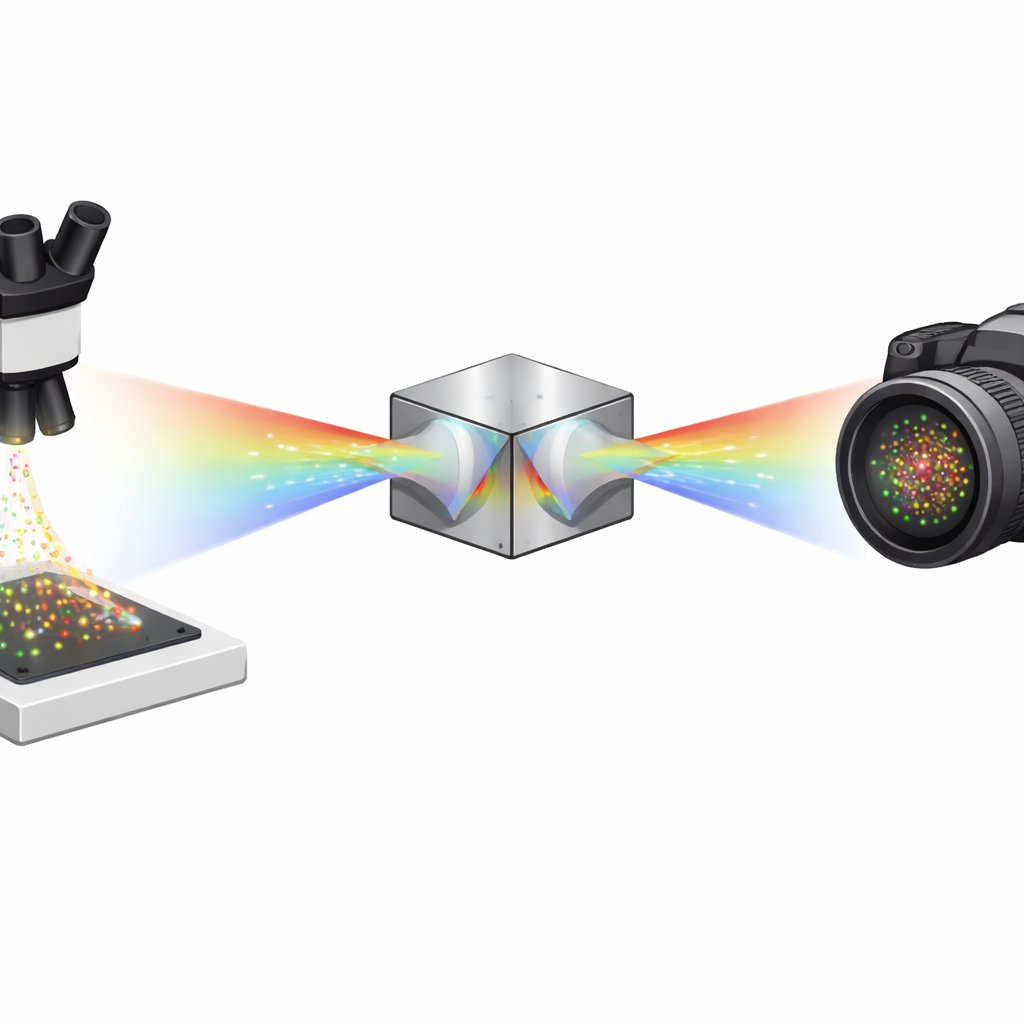
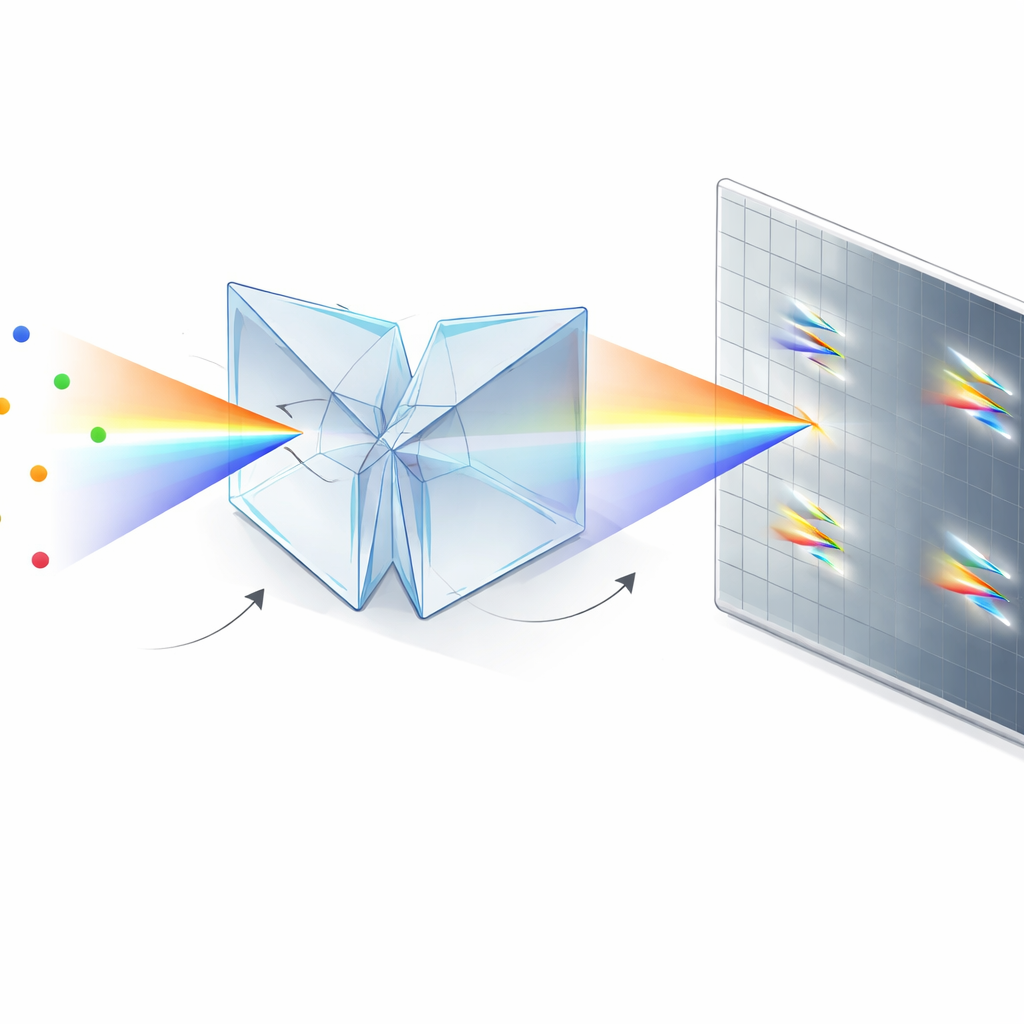
Die Autoren lösen dieses Problem mit einem kompakten optischen Modul, das auf zwei identischen Doppelkeilprismen und einem Strahlteiler basiert. Anstatt Photonen in einen „Positions“-Arm und einen separaten „Farb“-Arm zu schicken, erzeugt ihr symmetrisch dispergierendes Doppelkeilprismen-Design (SDDWP) zwei spiegelbildliche, spektral verbreiterte Kopien jedes blinkenden Moleküls auf derselben Kamera. Da diese beiden Bilder perfekt symmetrisch sind, kann eine einfache Berechnung sowohl die wahre Position des Moleküls (aus dem Mittelpunkt zwischen den beiden Punkten) als auch sein Spektrum (aus dem Abstand der Punkte) wiederherstellen. Effektiv tragen alle gesammelten Photonen sowohl zur räumlichen als auch zur spektralen Information bei, was die Präzision von Lokalisierung und Identifikation jedes Moleküls deutlich verbessert.
Scharfere, klarere Farben in drei Dimensionen
Mithilfe analytischer Modelle und sorgfältig kalibrierter Testproben zeigen die Autoren, dass SDDWP die laterale (in der Ebene) Präzision um etwa 27 % und die spektrale Präzision um etwa 48 % gegenüber ihrem vorherigen, prismatischen System verbessert. Sie erweitern das Design dann zur dreidimensionalen Bildgebung mit einem „Biplane“-Ansatz, bei dem die beiden spektralen Bilder leicht entgegengesetzt aus dem Fokus liegen. Durch Analysieren, wie sich die Größe jedes Punktes zwischen den beiden Ebenen verändert, kann das System bestimmen, wie weit ober- oder unterhalb der Fokusebene ein Molekül sitzt, und erreicht eine axiale Präzision in der Größenordnung von 18 Nanometern innerhalb eines nützlichen Tiefenbereichs von etwa einer halben Mikrometers. Trotz der zusätzlichen Komplexität der 3D-Bildgebung behält das neue Design nahezu 2D-ähnliche spektrale Schärfe bei, was eine sehr feine Trennung von Farbstoffen ermöglicht, deren Farbspektren stark überlappen.
Farbliche Trennung von Zellstrukturen und bewegten Partikeln
Um zu demonstrieren, was das in der Praxis bedeutet, nahmen die Forscher fixierte HeLa-Zellen in 3D mit einem einzelnen roten Laser und drei weitrotem Farbstoffen auf, die normalerweise überlappende Spektren haben. Sie markierten Peroxisomen, Mikrotubuli und Mitochondrien und zeigten, dass das System diese Strukturen zuverlässig anhand subtiler spektraler Unterschiede trennen konnte, während die räumlichen Details über die Tiefe hinweg hoch blieben. Außerdem verwendeten sie spektral unterscheidbare Quantenpunkte als winzige Marker, um viele Partikel gleichzeitig in einer viskosen Lösung zu verfolgen. Indem das System das Spektrum jedes Partikels als einzigartigen „Fingerabdruck“ behandelt, konnte das SDDWP-Setup hunderte dicht gepackter Trajektorien korrekt verfolgen, die andernfalls beim Kreuzen der Bahnen hoffnungslos verworren wären, und die Verfolgungsfehler selbst bei Partikeldichten nahe theoretischer Grenzen auf nur wenige Prozent reduzieren.
Von komplexer Optik zu einfachem Zusatzmodul
Über die Leistung hinaus ist ein wesentlicher Vorteil dieses Ansatzes die Praktikabilität. Die SDDWP-Einheit ist eine kleine, größtenteils monolithische Baugruppe, die an die Seitenöffnung eines standardmäßigen umgekehrten Fluoreszenzmikroskops geschraubt wird und nur eine moderate Ausrichtung erfordert. Ihr prismatisches Design verschwendet deutlich weniger Photonen als Beugungsgitter, und es ist mechanisch stabil genug, um über lange Zeiten mit nur routinemäßigen Kontrollen kalibriert zu bleiben. Das macht sie zu einem realistischen Upgrade-Pfad für viele bestehende Einzelmolekül-Labore.
Was das für die zukünftige Mikroskopie bedeutet
Indem die Art und Weise, wie Licht aufgeteilt und wieder kombiniert wird, neu durchdacht wird, zeigt diese Arbeit, dass es möglich ist, sowohl schärfere Positionen als auch klarere Farbinformationen aus dem gleichen begrenzten Photonenvorrat zu gewinnen. Im Alltag erlaubt dies Wissenschaftlern, mehr Molekülarten in dichten, dreidimensionalen Umgebungen zu unterscheiden und viele markierte Partikel gleichzeitig zu verfolgen, ohne die Bildqualität zu opfern. Wenn die Technik übernommen und angepasst wird — möglicherweise sogar für Lebendzellaufnahmen mit schonendem roten Licht — könnte sie zu einem vielseitigen Werkzeug werden, um zu erforschen, wie komplexe molekulare Assemblies und Organellen organisiert sind und wie sie sich in lebenden Zellen bewegen, und zwar alles im Nanometerbereich.
Zitation: Yeo, WH., Brenner, B., Shi, M. et al. Maximizing photon utilization in spectroscopic single-molecule localization microscopy using symmetrically dispersed dual-wedge prisms. npj Imaging 4, 20 (2026). https://doi.org/10.1038/s44303-026-00152-z
Schlüsselwörter: Einzelmolekülmikroskopie, Superauflösungsbildgebung, Spektrale Bildgebung, 3D-Zellbildgebung, Einzelteilchenverfolgung