Clear Sky Science · de
Fortschrittliche Bildgebungstechniken für die intraoperative Tumornavigation
Krebs im Operationssaal klarer sehen
Krebsoperationen sind oft ein feines Abwägen: alle Krebszellen entfernen und gleichzeitig möglichst viel gesundes Gewebe erhalten. Dieser Übersichtsartikel erklärt, wie eine neue Generation von Bildgebungswerkzeugen Chirurgen ermöglicht, Tumoren und ihre Ränder während der Operation in Echtzeit zu sehen. Für einen Laien ist die Attraktivität offensichtlich – diese Technologien versprechen weniger Folgeoperationen, präzisere Tumorresektionen und bessere Chancen auf langfristiges Überleben, weil sie Chirurgen während des Eingriffs eine klarere „Karte“ liefern.
Warum bessere Sicht im OP wichtig ist
Krebs gehört zu den weltweit führenden Todesursachen, und die Chirurgie bleibt eine Säule der Behandlung. Dennoch waren selbst die erfahrensten Chirurgen lange Zeit durch das begrenzt, was sie sehen und ertasten können, sowie durch bildgebende Verfahren, die Tage oder Wochen vor der Operation aufgenommen wurden. Traditionelle Werkzeuge wie Ultraschall, CT, MRT und PET helfen bei der Operationsplanung, sind aber oft sperrig, langsam oder nicht für den kontinuierlichen Einsatz während eines Eingriffs geeignet. Daher ist es schwierig festzustellen, wo ein Tumor endet und gesundes Gewebe beginnt, was das Risiko erhöht, Krebs zurückzulassen oder zu viel normales Gewebe zu entfernen. Der Übersichtsartikel zeigt auf, wie die „intraoperative Bildgebung“ – also Live-Bildgebung direkt im Operationssaal – dieses Bild verändert.
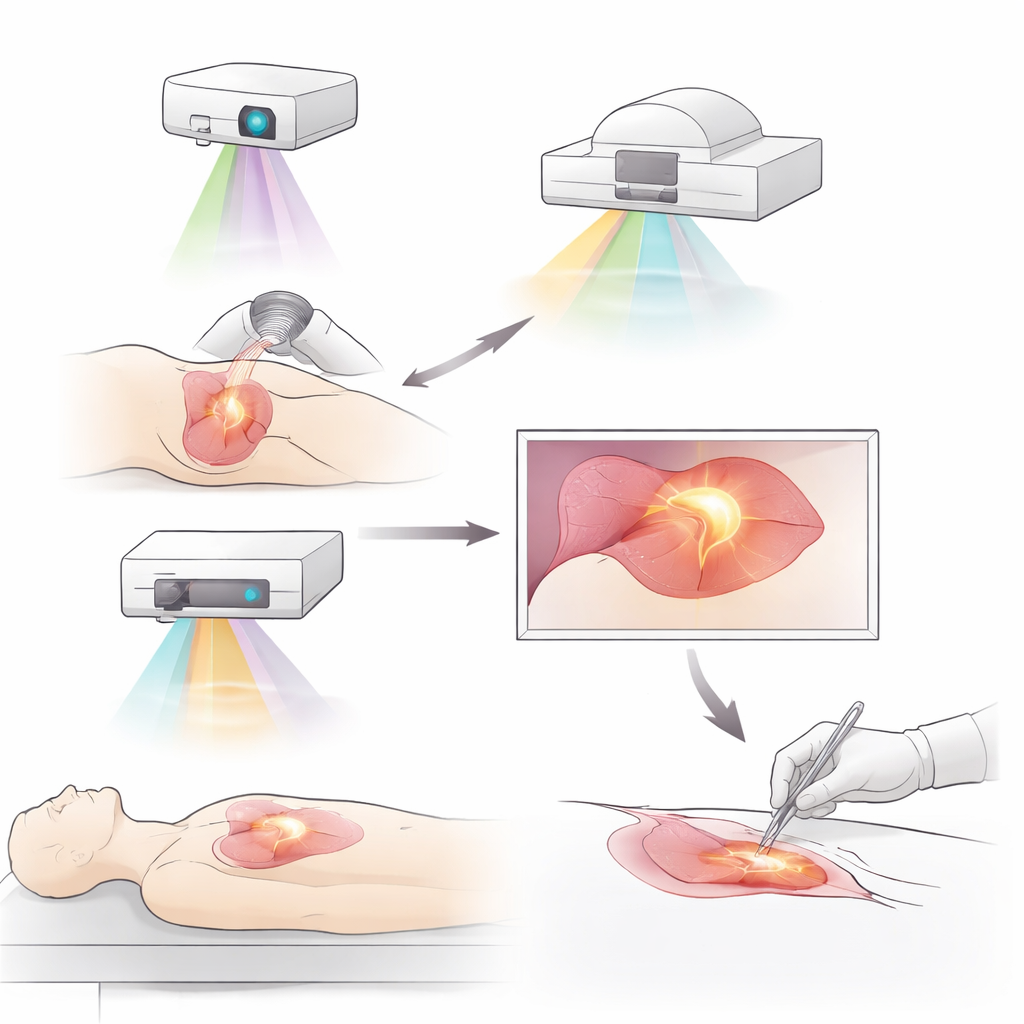
Leuchtende Tumoren und neue Möglichkeiten, sie sichtbar zu machen
Ein wichtiger Fortschritt ist die Fluoreszenzbildgebung, bei der spezielle Farbstoffe oder molekulare Sonden Tumoren unter nahinfrarotem Licht zum Leuchten bringen. Ältere, nicht zielgerichtete Farbstoffe wie Indocyaningrün haben Chirurgen bereits geholfen, Tumoren zu umreißen, Lymphgefäße zu verfolgen und wichtige Lymphknoten bei Brust-, Leber-, Lungen- und Magenkrebs zu finden. Neuer entwickelte, zielgerichtete Sonden gehen weiter, indem sie sich an Moleküle binden, die von Tumorzellen oder ihrem Umfeld vermehrt produziert werden. Beispiele sind Sonden, die an Wachstumsfaktor-Rezeptoren, Immun-Checkpoints oder an Proteine binden, die im Tumorstroma oder in hypoxischen Regionen reichlich vorhanden sind. Einige dieser Wirkstoffe können sogar an Krebsmedikamente gekoppelt werden, sodass präzise Visualisierung und Therapie in einem Molekül kombiniert werden. Erste klinische Studien zeigen, dass solche Tracer verborgene Tumorherde aufdecken und den Bedarf an Folgeoperationen nach brusterhaltenden Eingriffen reduzieren können.
Mehr als Leuchten: Schall, Licht und viele Farben
Obwohl Fluoreszenz zentral ist, hebt die Übersichtsarbeit mehrere komplementäre Ansätze hervor, die unterschiedliche Aspekte eines Tumors sichtbar machen. Die photoakustische Bildgebung nutzt Lichtpulse, um Schallwellen im Gewebe zu erzeugen, verbindet die Auflösung optischer Methoden mit der Eindringtiefe des Ultraschalls und konnte sehr kleine Metastasen aufdecken, die andere Untersuchungen übersehen. Multispektrale und hyperspektrale Bildgebung zerlegen Licht in viele Banden und erfassen feine Unterschiede in Absorption und Reflexion von Geweben; dadurch lassen sich Krebs und normales Gewebe in Brust-, Zervix- und gastrointestinalen Tumoren mit hoher Genauigkeit unterscheiden. Fortschritte im Ultraschall – einschließlich Verfahren zur Messung der Gewebesteifigkeit – liefern Tiefeninformationen und zeigen, wie weit der Krebs infiltriert hat. Raman-Spektroskopie, die das chemische „Fingerabdruck“-Muster von Gewebe anhand der Lichtstreuung liest, bietet eine kennzeichnungsfreie, hochspezifische Identifikation von Krebs während der Operation, besonders in Kombination mit anderen Modalitäten.
3D-Karten erstellen und mehrere Blickwinkel kombinieren
Ein weiteres Thema des Artikels ist die Zusammenführung von Bildern zu dreidimensionalen und multimodalen Darstellungen, die Chirurgen intuitiv nutzen können. Dreidimensionale Rekonstruktionen von Blutgefäßen, Lymphbahnen und Organen, überlagert mit fluoreszenten Signalen, helfen bei der Planung präziser segmentaler Resektionen von Leber und Lunge und leiten schwierige Lymphknotendissektionen. Hybridsysteme, die PET mit optischer Bildgebung verbinden oder nuklearmedizinische Tracer mit Fluoreszenz paaren, erlauben es, dieselbe Sonde für präoperative Ganzkörperscans und intraoperative Führung zu verwenden. Neue Plattformen integrieren Laserablation, optische Kohärenztomographie und Robotik, um Läsionen automatisch zu lokalisieren und mit hoher Präzision zu behandeln. Ziel dieser Ansätze ist es, Chirurgen sowohl das „große Ganze“ der Tumorausbreitung als auch die feinen Details zu liefern, die für saubere, sichere Schnittränder nötig sind.
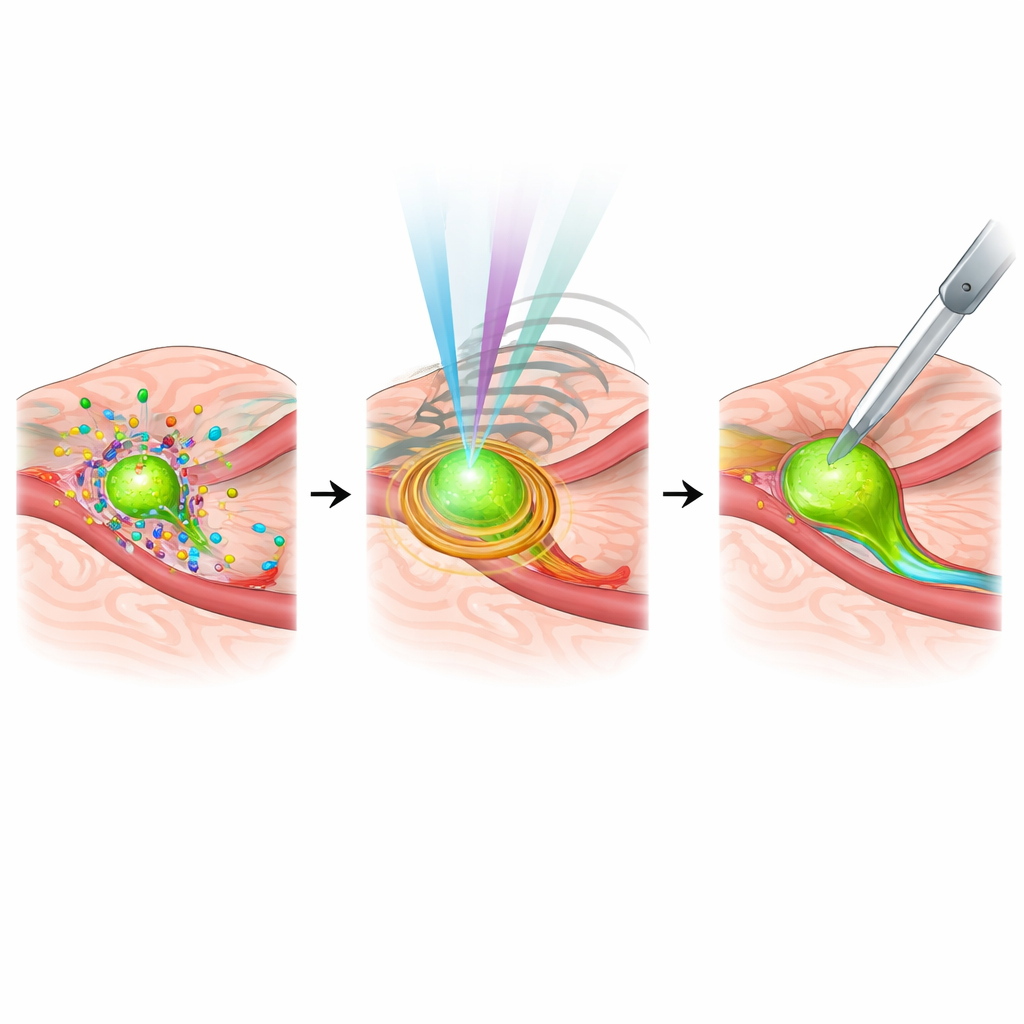
Intelligentere Systeme, personalisierte Zielstrukturen und verbleibende Hürden
Der Artikel blickt auch auf die Rolle von künstlicher Intelligenz und personalisierter Medizin. Maschinelle Lernmodelle helfen bereits dabei, in Echtzeit zwischen tumorigem und normalem Gewebe zu unterscheiden, kritische anatomische Strukturen zu erkennen und sogar die Ausbreitung in Lymphknoten bei Pankreasoperationen vorherzusagen, was die Abhängigkeit von Schnellpathologie reduzieren könnte. Gleichzeitig werden Bildgebungssonden so gestaltet, dass sie zu den einzigartigen molekularen Signaturen des Tumors jedes Patienten passen und intraoperative Bilder mit genetischen und molekularen Profilen verknüpfen. Dennoch bestehen Hindernisse: Viele Systeme sind teuer, komplex und schwer in Routineabläufe zu integrieren; einige erfordern spezialisierte Kontrastmittel mit sorgfältig zu überwachenden Sicherheitsprofilen; und Standards zur Integration all dieser Daten in Navigationssysteme sind noch im Entstehen begriffen.
Was das für Patientinnen und Patienten bedeutet
In verständlicher Sprache lautet das Fazit des Artikels, dass Chirurgen etwas gewinnen, das sie bisher nicht wirklich hatten: die Fähigkeit, lebenden Krebs während der Operation mit hoher Klarheit zu sehen. Indem Tumoren zum Leuchten gebracht, ihre Chemie gelesen, sie in 3D kartiert und mehrere Bildtypen kombiniert werden – oft unterstützt durch KI – können diese Werkzeuge dazu beitragen, mehr Tumor zu entfernen und mehr gesundes Gewebe zu erhalten. Obwohl Kosten, Ausbildung und technologische Lücken adressiert werden müssen, bevor solche Systeme weit verbreitet sind, ist die Richtung klar. Fortschrittliche intraoperative Bildgebung steht kurz davor, ein zentraler Bestandteil der Standardkrebschirurgie zu werden und Patientinnen und Patienten präzisere Eingriffe, weniger Rückfälle und bessere Chancen auf langfristige Kontrolle zu bieten.
Zitation: Li, K., Zhang, Y., Yang, H. et al. Advanced imaging techniques for tumor intraoperative navigation imaging. npj Imaging 4, 18 (2026). https://doi.org/10.1038/s44303-026-00150-1
Schlüsselwörter: intraoperative Bildgebung, fluoreszenzgeführte Chirurgie, Erkennung von Tumorrändern, multimodale Krebsbildgebung, photoakustische Bildgebung