Clear Sky Science · de
Korrelative multimodale Bildgebung zur mikroskaligen räumlichen Kartierung von Wechselwirkungen zwischen Kollagen und Genaktivität in menschlichem Gewebe
Warum ein Blick ins Muskelinnere wichtig ist
Krankheiten, die unsere Organe langsam vernarben, wie die Duchenne‑Muskeldystrophie (DMD), spielen sich auf Maßstäben ab, die mit bloßem Auge nicht erkennbar sind. Genaktivität findet in einzelnen Zellen statt, während das sie umgebende Stützgewebe aus winzigen Proteinfasern besteht. Bislang konnten Forschende diese beiden Welten selten gemeinsam in genau derselben Gewebescheibe beobachten. Diese Studie stellt eine Methode vor, die genau das ermöglicht und aufzeigt, wie genetische Signale und das strukturelle Gerüst des Körpers auf Mikromaßstab miteinander interagieren.
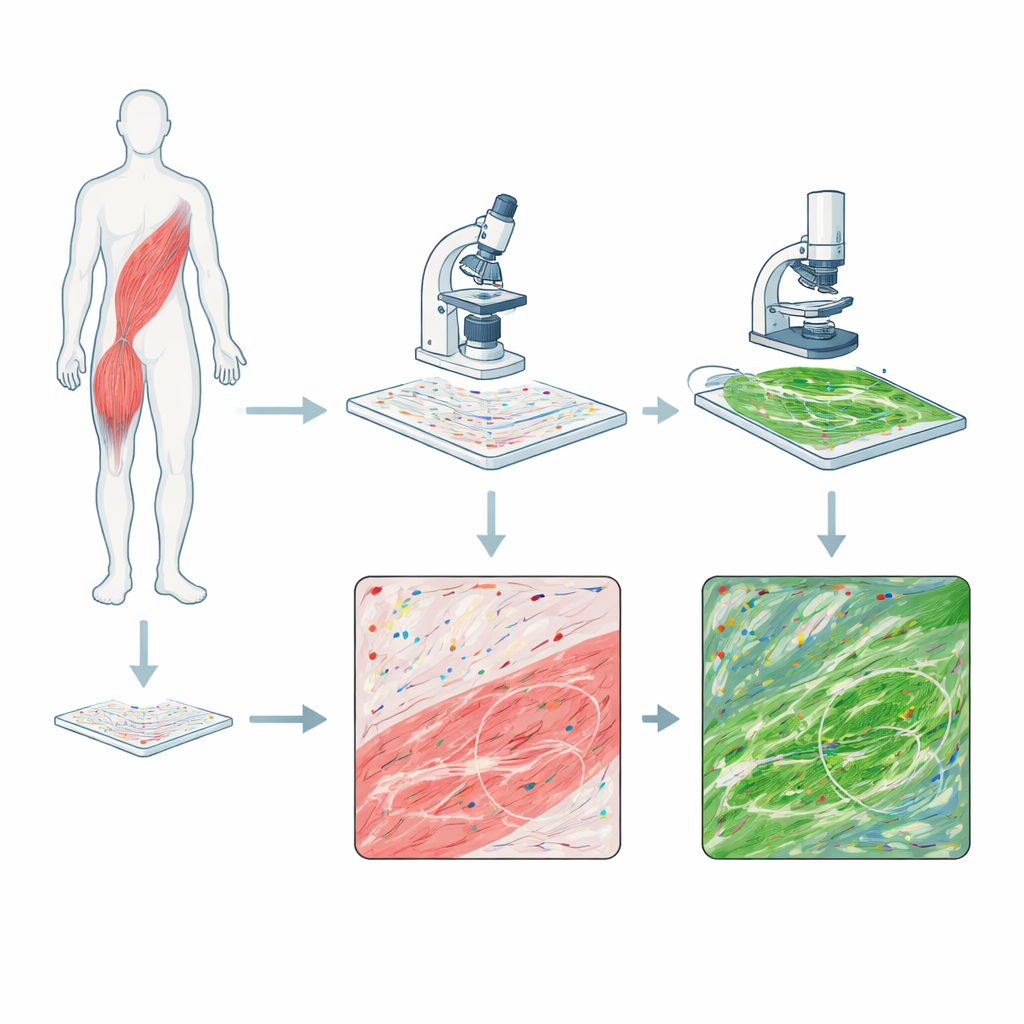
Zwei Kameras auf demselben Gewebestück
Die Forschenden kombinierten zwei leistungsfähige Bildgebungsverfahren an einzelnen Schnitten menschlicher Skelettmuskelbiopsien von Personen mit DMD und von einer gesunden Versuchsperson. Ein Verfahren, RNAscope genannt, markiert einzelne RNA‑Moleküle – die aktiven Kopien von Genen – als farbige Punkte und zeigt, wo bestimmte genetische Botschaften vorkommen. Das zweite Verfahren, Multiphotonenmikroskopie, nutzt Laserlicht, um Kollagenfasern im Gewebe ohne Zusatzfarbstoff zum Leuchten zu bringen und damit die Architektur des Bindegewebes abzubilden, das sich bei Vernarbung und Fibrose verdickt. Indem zuerst die RNA‑Signale und anschließend die Kollagen‑Signale auf derselben Objektträgerfläche aufgenommen wurden, ließen sich die beiden Bilder so ausrichten, dass jeder Genaktivitäts‑Punkt pixelgenau mit dem umliegenden Faser‑Netz verglichen werden konnte.
Was die einzelnen Ansichten bereits verraten
Die Betrachtung der einzelnen Bildgebungsverfahren für sich zeigte bereits deutliche Unterschiede zwischen erkranktem und gesundem Muskel. RNAscope ergab, dass die Muskeln der DMD‑Patienten weniger Dystrophin‑Transkripte enthielten – die RNA‑Botschaften, die zur Herstellung des fehlenden Dystrophin‑Proteins nötig sind – als die gesunde Probe. Die verbleibenden Signale unterschieden sich außerdem in der Größe, je nachdem welcher Teil des Gens adressiert wurde, was auf Unterschiede bei der Verarbeitung der langen Dystrophin‑Botschaft hindeutet. Gleichzeitig zeigten die Multiphotonenaufnahmen, dass DMD‑Muskeln mit langen, dichten Kollagenfasern durchsetzt waren, ein sichtbares Zeichen fibrotischer Vernarbung, während der gesunde Muskel weniger und gleichmäßiger verteilte Fasern aufwies. Diese Befunde stimmen mit der klinischen Erfahrung überein: Bei DMD wird Muskelgewebe allmählich durch Fett und Narbengewebe ersetzt.
Rauszoomen: breitflächige Muster im Gewebe
Nachdem die beiden Bildtypen digital registriert worden waren, unterteilte das Team jeden Gewebeschnitt in ein Gitter und behandelte jedes Quadrat als winzige Nachbarschaft. In jedem Quadrat maßen sie sowohl Kollagenmerkmale – Faserlänge, Orientierung und wie gewunden oder gerade die Fasern waren – als auch die lokale Dichte der Dystrophin‑RNA‑Punkte. Diese „Heatmap“-Ansicht offenbarte fleckige, regionsabhängige Variationen sowohl in der Genaktivität als auch in der Kollagenstruktur innerhalb des DMD‑Muskels. Als diese Messwerte jedoch statistisch verglichen wurden, zeigten Transkriptmengen und Kollagenmerkmale auf dieser groben Skala nahezu keine konsistente Beziehung. Anders gesagt: Beim Mittelwertbild über relativ große Bereiche waren Gebiete mit vielen Dystrophin‑RNA‑Signalen nicht verlässlich stärker oder schwächer fibrotisch als Gebiete mit weniger RNA‑Signalen.
Reinzoomen: Beziehungen auf zellulärer Skala
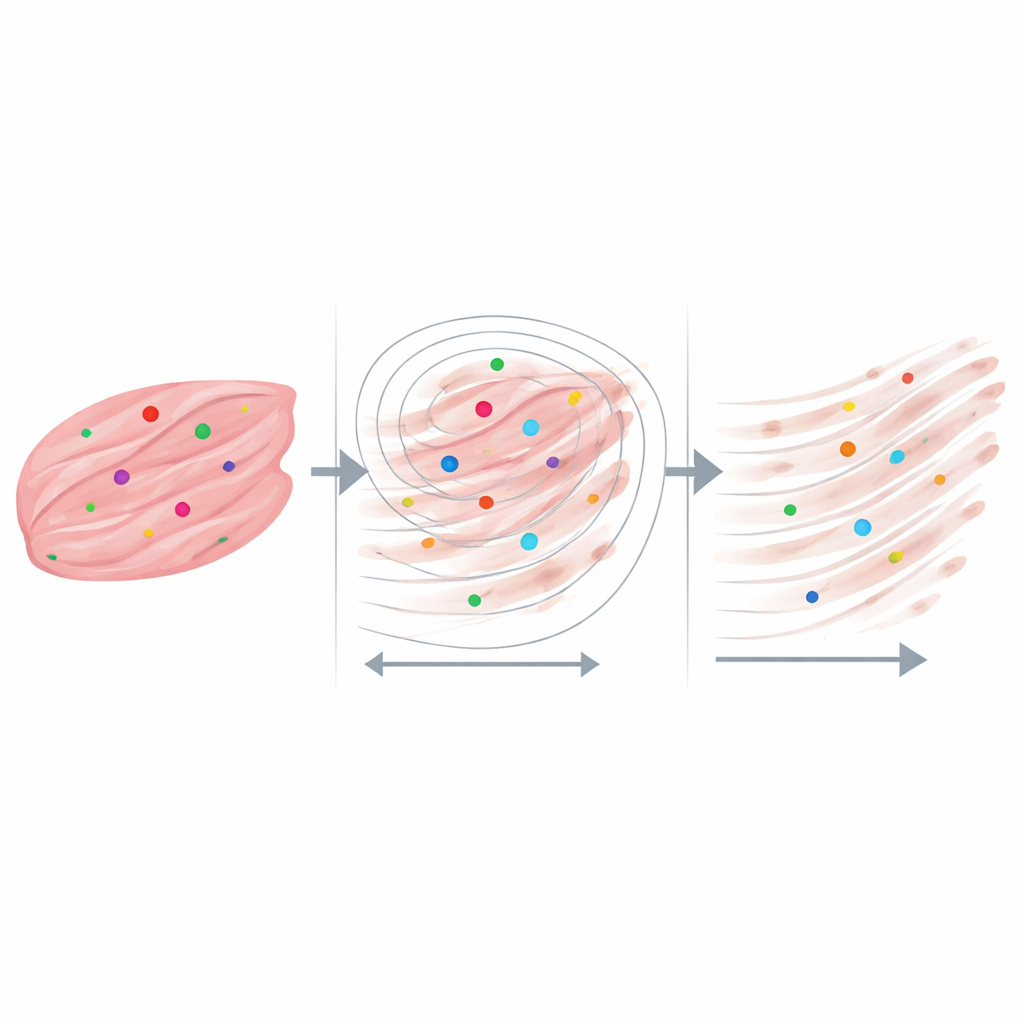
Die aufschlussreichsten Ergebnisse ergaben sich, als die Wissenschaftler auf Nachbarschaften fokussierten, die nur wenige Dutzend Mikrometer groß waren – ungefähr in der Größenordnung einzelner Muskelfasern und ihrer unmittelbaren Umgebung. Für jeden RNA‑Punkt zogen sie eine Serie wachsender Kreise und ermittelten, wie viele Kollagenfasern sich darin befanden und wie lang diese Fasern waren. Sowohl in DMD‑ als auch in gesunden Geweben waren die Kollagenfasern unmittelbar neben den Dystrophin‑RNA‑Signalen am längsten und wurden mit zunehmendem Abstand kürzer. In den am stärksten vernarbten Proben hatten Transkript‑Punkte fast immer Kollagen in der Nähe, selbst auf sehr kleinen Entfernungen, während in der gesunden Probe viele RNA‑Punkte in Bereichen mit wenig oder keinem nahen Kollagen lagen. Kontrollanalysen mit zufällig platzierten Punkten und leicht veränderten Bildverarbeitungsparametern zeigten, dass dieses Muster nicht einfach durch Zufall oder durch Software‑Eigenheiten erklärt werden kann.
Was das für Muskelerkrankungen und darüber hinaus bedeuten könnte
Diese Ergebnisse legen nahe, dass wichtige Zusammenhänge zwischen Genbotschaften und Gewebestruktur bei Betrachtung nur großer Mittelwerte verborgen bleiben, aber auf zellulärer Ebene sichtbar werden. In dieser Machbarkeitsstudie lagen Regionen, die reich an bestimmten Dystrophin‑Transkripten waren, tendenziell in der Nähe längerer, dichterer Kollagenfasern, was darauf hindeutet, dass lokale Genaktivität und fibrotischer Umbau sich innerhalb winziger Mikro‑Umgebungen des Muskels gegenseitig beeinflussen könnten. Die Autoren betonen, dass die Patientengruppe klein ist und die Arbeit noch kein klinischer Test ist. Vielmehr stellen sie eine flexible Plattform vor, die auf andere Gene, Gewebetypen und Bildgebungsverfahren ausgeweitet werden kann. Indem sie feststellt, wo Gene aktiv sind und wie das Gewebegerüst aufgebaut ist, eröffnet dieser Ansatz die Möglichkeit, neue räumliche Biomarker für Fibrose, Regeneration und Reaktionen auf aufkommende RNA‑basierte Therapien zu entdecken.
Zitation: Scodellaro, R., Mietto, M., Ferlini, A. et al. Correlative multimodal imaging for microscale spatial mapping of collagen-gene activity interactions in human tissues. npj Imaging 4, 17 (2026). https://doi.org/10.1038/s44303-026-00149-8
Schlüsselwörter: multimodale Bildgebung, Duchenne-Muskeldystrophie, Kollagenfibrose, räumliche Genexpression, Skelettmuskelbiopsie