Clear Sky Science · de
Eine einstufige Radiomarkierungsstrategie für PET, SPECT und therapeutische Radionuklide unter Verwendung von Nanopartikeln als universeller Chelator
Warum winzige radioaktive Teilchen wichtig sind
Die moderne Krebsbehandlung stützt sich zunehmend darauf, Tumore mit radioaktiven Wirkstoffen sichtbar zu machen und in manchen Fällen von innen zu zerstören. Die Entwicklung jeder neuen radioaktiven Arznei ist jedoch langsam und umständlich, weil die meisten Konzepte speziell für ein bestimmtes Radiometall maßgeschneidert werden müssen. Diese Studie untersucht einen ganz anderen Ansatz: die Verwendung eines einheitlichen eisenbasierten Nanopartikels als „universelle Fassung“, die verschiedene medizinische Isotope für Bildgebung und Therapie aufnehmen kann und so die Erstellung und Feinabstimmung solcher Wirkstoffe beschleunigen könnte.
Von vielen Schlüsseln zu einem Schloss
Die heutigen radioaktiven Arzneien beruhen meist auf chemischen Greifern, sogenannten Chelatoren, die Metallatome festhalten und an Antikörper oder andere Zielmoleküle binden. Jedes radioaktive Metall benötigt oft seinen eigenen Chelator und sein eigenes Rezept — Bedingungen wie Temperatur, Säuregrad und Reaktionszeit ändern sich. Für einige medizinisch wichtige Metalle, insbesondere jene, die für potente Alphastrahlentherapien verwendet werden, existiert noch kein idealer Chelator. Die Autoren argumentieren, dass dieses Metall‑für‑Metall‑Vorgehen zum Engpass geworden ist: Die Liste nützlicher Isotope wächst, aber die passende Chemie, um sie sicher zu handhaben, kann nicht mithalten.
Nanopartikel als universelle Fassung
Um dieses Problem anzugehen, wandten sich die Forscher sehr kleinen Eisenoxid‑Nanopartikeln zu, einem Material, das bereits als MRT‑Kontrastmittel untersucht wurde. Sie konstruierten Partikel mit einem Eisenoxidkern von etwa drei Nanometern Durchmesser, umhüllt von einer Citratbeschichtung, die sie im Blut stabil hält. In einem einzigen, zehnminütigen, mikrowellenunterstützten Syntheseschritt versetzten sie den Kern mit jeweils einem von zehn verschiedenen radioaktiven Metallen, die häufig für PET, SPECT oder interne Radiotherapie verwendet werden. Dieser One‑Pot‑Prozess ergab gleichmäßig große Partikel mit hohen Ausbeuten und — entscheidend — ausgezeichneter Stabilität in Humanserum, selbst für herausfordernde Therapieisotope wie Radium‑223 und Actinium‑225, deren Zerfallsprodukte bei traditionellen Chelatoren oft entweichen.
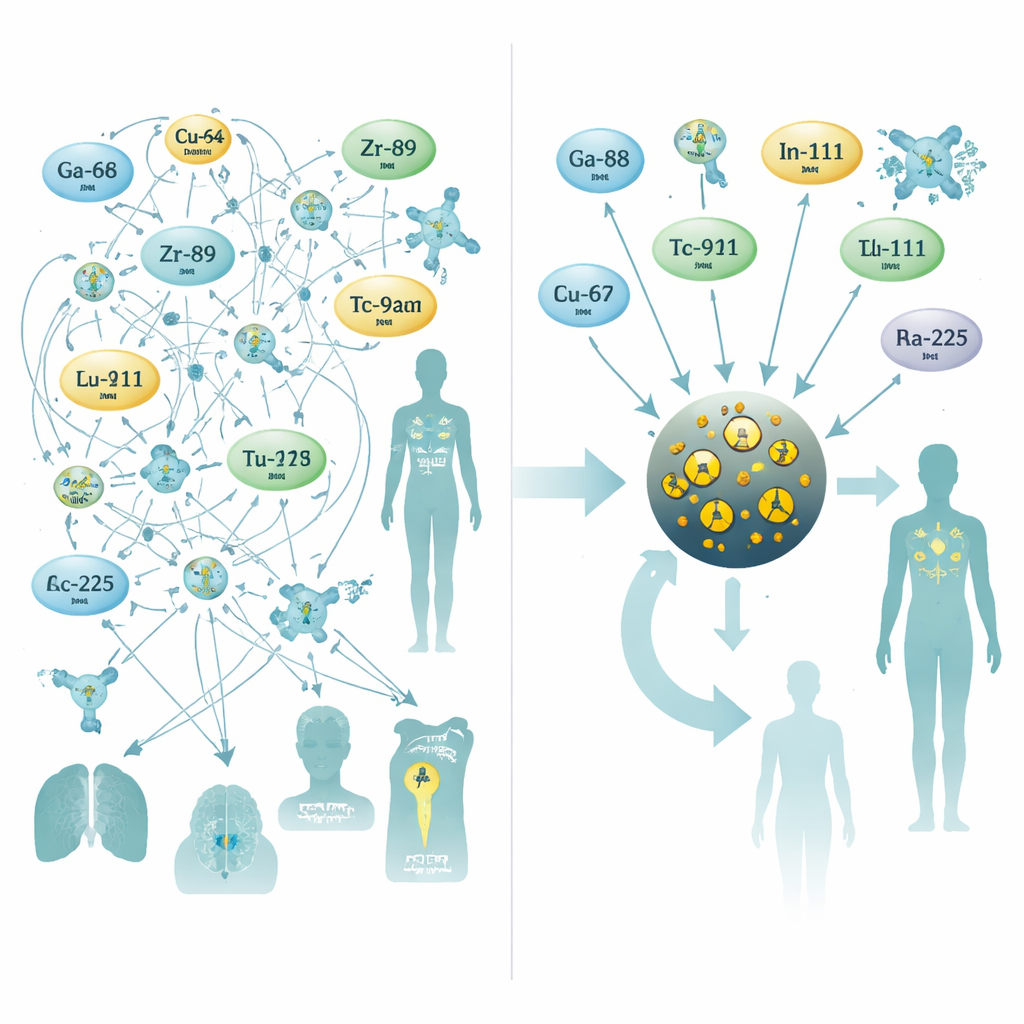
Gerinnsel und Hirntumore bildlich darstellen
Nachdem sie gezeigt hatten, dass sich viele unterschiedliche Isotope im gleichen Nanopartikel‑Design binden lassen, prüfte das Team, was diese „Nanotracer" in lebenden Tieren leisten können. In einem Mausmodell des Glioblastoms, einem tödlichen Hirntumor, wurden mit Gallium‑68 markierte Partikel in den Blutkreislauf injiziert und mittels kombinierter PET‑ und MRT‑Aufnahmen dargestellt. Die Partikel reichten in Tumore hinein, die ausreichend groß waren, um die Blut‑Hirn‑Schranke zu stören, und lieferten so sowohl starken MRT‑Kontrast als auch ein sensibles PET‑Signal. In einem separaten Experiment wurden die Partikel chemisch so modifiziert, dass sie über eine hochselektive Click‑Reaktion an einen Antikörper gekoppelt werden konnten, der aktivierte Thrombozyten in Blutgerinnseln ansteuert. In Mäusen mit verletzter Halsschlagader erzeugte diese zweistufige „Pretargeting“-Strategie deutliche PET‑Signale am Gerinnselort, während Kontrolltiere keinen solchen Hotspot zeigten.
Von der Diagnose zur Behandlung und sicherer Ausscheidung
Die gleiche Plattform wurde auch zur Abgabe von Therapien genutzt. Wenn mit Lutetium‑177 beladene Nanopartikel direkt in Glioblastomtumore bei Mäusen injiziert wurden, blieben die Partikel für mindestens zwei Wochen größtenteils im Tumormasse eingeschlossen. In dieser Zeit wuchsen unbehandelte Tumore auf das Mehrfache ihres Ausgangsvolumens, während behandelte Tumore ihr Wachstum einstellten — ein Hinweis darauf, dass die lokale Strahlendosis ausreichte, das Fortschreiten zu stoppen. Da wiederholte Anwendungen zu einer Eisenüberladung von Leber und Milz führen könnten, passte das Team die Syntheseparameter an, um noch kleinere Partikel von etwa vier bis fünf Nanometern Durchmesser herzustellen, die klein genug sind, um renal gefiltert zu werden. Diese verkleinerten Partikel hielten ihre radioaktive Fracht weiterhin sicher, wurden jedoch schnell über die Blase ausgeschieden und reduzierten so die langfristige Anreicherung in wichtigen Organen.
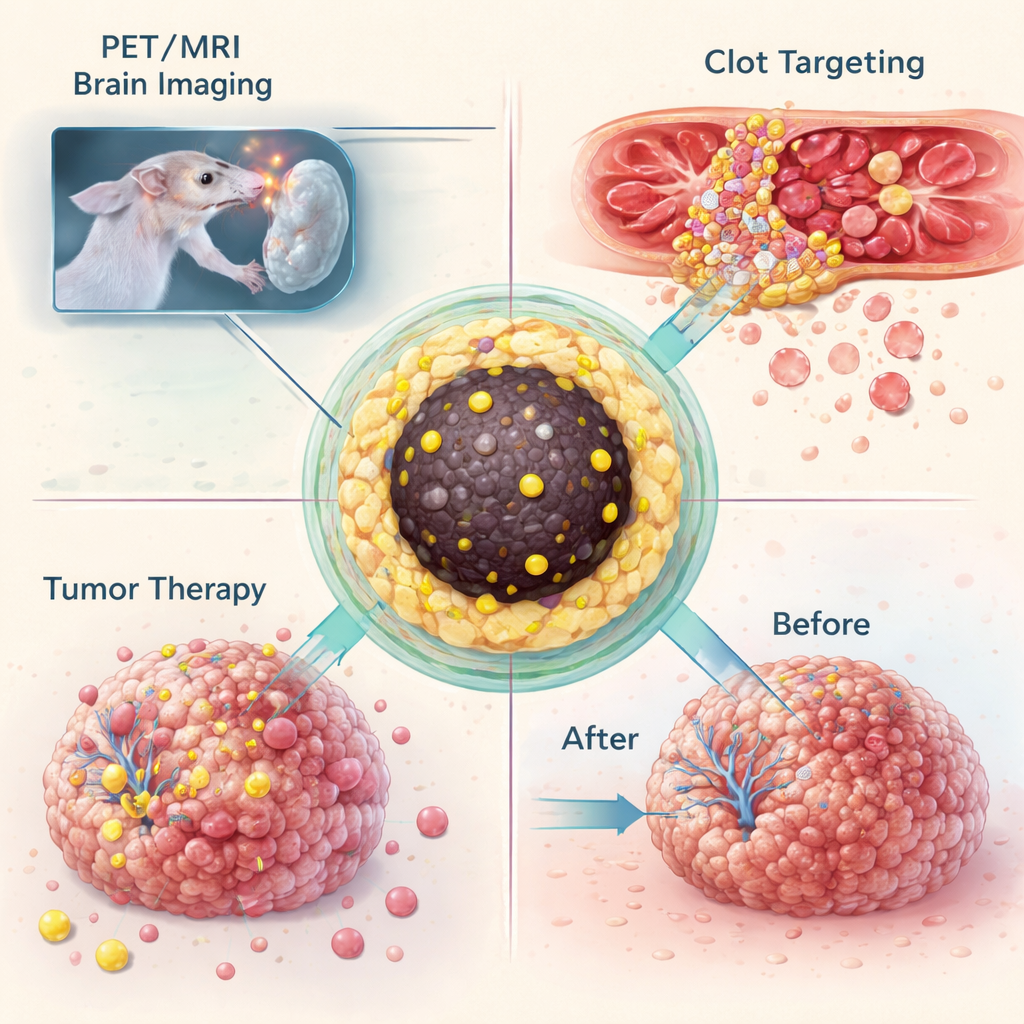
Was das für die zukünftige Krebsversorgung bedeuten könnte
Für Nichtfachleute lautet die Kernbotschaft: Die Forscher haben eine einzelne, flexible Nanopartikelplattform entwickelt, die mit vielen verschiedenen radioaktiven Metallen kombiniert werden kann, ohne die Chemie jedes Mal neu erfinden zu müssen. In Tiermodellen kann derselbe Basispartikel helfen, Hirntumore zu erkennen, Blutgerinnsel hervorzuheben, Strahlung direkt in Tumoren abzugeben und sogar so angepasst zu werden, dass er über die Nieren ausgeschieden wird. Obwohl vor einer Anwendung am Menschen noch weitere Arbeiten nötig sind, bietet dieser Ansatz einen vielversprechenden Weg, Diagnose‑ und Therapieagentienfamilien zu entwerfen, die im Körper dasselbe Verhalten zeigen und sich nur durch die Art der getragenen Strahlung unterscheiden. Diese Konsistenz könnte die Entwicklung vereinfachen, Sicherheitsprüfungen verbessern und schließlich anspruchsvolle nuklearmedizinische Verfahren breiter verfügbar machen.
Zitation: Herraiz, A., Rodríguez-San-Pedro, A., Casquero-Veiga, M. et al. A single-step radiolabeling strategy for PET, SPECT, and therapeutic radionuclides using nanoparticles as a universal chelator. npj Imaging 4, 8 (2026). https://doi.org/10.1038/s44303-026-00142-1
Schlüsselwörter: Radiotheranostik, Nanopartikel, PET‑Bildgebung, Glioblastom, zielgerichtete Strahlentherapie